Плотность электролита в аккумуляторе (АКБ)
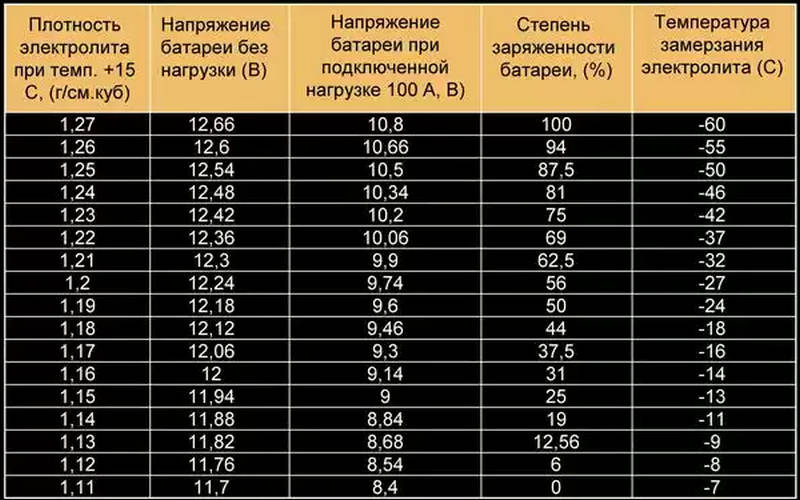
Концентрация серной кислоты в электролите характеризуется плотностью электролита. Плотность любой жидкости определяется как отношение ее удельного веса к удельному весу воды. Иными словами, чем удельный вес вещества (жидкости) больше, тем выше ее плотность. Эталоном плотности выбрана дистиллированная вода, плотность которой принята равной 1,000 при температуре 80°Ф (27°С). Плотность чистой серной кислоты составляет 1,835. Нормальная концентрация водного раствора серной кислоты (раствора, состоящего на 64% из воды и на 36% из серной кислоты, называемого электролитом) характеризуется плотностью электролита в пределах от 1,260 до 1,280 при температуре 80°Ф (27°С). Чем выше плотность электролита в аккумуляторной батарее, тем выше степень ее заряженности.
Рис. В процессе разряда аккумуляторной батареи плотность электролита снижается
Индикаторы степени заряженности аккумулятора
Некоторые типы аккумуляторных батарей оснащены встроенным индикатором степени заряженности. Такой индикатор представляет собой просто небольшой ареометр шарикового типа, вмонтированный в одну из ячеек аккумуляторной батареи. В этом ареометре используется пластмассовый шарик, который всплывает в электролите нормальной плотности (когда аккумулятор заряжен примерно на 65%). Когда шарик всплывает, он появляется в окошке ареометра, изменяя его цвет.
Такой индикатор представляет собой просто небольшой ареометр шарикового типа, вмонтированный в одну из ячеек аккумуляторной батареи. В этом ареометре используется пластмассовый шарик, который всплывает в электролите нормальной плотности (когда аккумулятор заряжен примерно на 65%). Когда шарик всплывает, он появляется в окошке ареометра, изменяя его цвет.
Рис. Типичный индикатор степени заряженности аккумуляторной батареи. При низкой плотности электролита (разряженная аккумуляторная батарея) шарик-поплавок тонет, соскальзывая с отражательной призмы. При достаточной степени заряженности аккумуляторной батареи шарик всплывает, и его цвет (обычно зеленый) приводит к изменению света, отражаемого призмой в сторону окошка индикатора, — оно темнеет
Рис. Аккумуляторная батарея с частично удаленным корпусом, в котором виден вмонтированный индикатор степени заряженности аккумулятора. Если уровень электролита опускается ниже дна призмы, окошко индикатора становится прозрачным (светлым).
Производители аккумуляторных батарей предупреждают о том, что в случае снижения уровня электролита в герметизированной аккумуляторной батарее, такая аккумуляторная батарея подлежит немедленной замене. Попытка зарядить аккумуляторную батарею, имеющую недостаточный уровень электролита, может привести к скоплению в ней газов и закончиться взрывом аккумуляторной батареи
Поскольку ареометр контролирует плотность электролита только в одной из ячеек аккумуляторной батареи (а в 12-вольтовой аккумуляторной батарее их — шесть), и поскольку шарик ареометра может легко застрять в одном положении, полагаться на его показания, как на достоверную информацию о степени заряженности аккумуляторной батареи, не следует.
Связь между плотностью электролита, степенью заряженности и напряжением аккумуляторной батареи
Ниже в таблице приведены значения плотности электролита и соответствующие им значения степени заряженности и напряжения аккумуляторной батареи при температуре 80°Ф (27°С).
| Плотность электролита | Степень заряженности аккумуляторной батареи | Напряжение аккумуляторной батареи (В) |
| 1,265 | Полностью заряжена | Не ниже 12,6 |
| 1,225 | Заряжена на 75% | 12,04 |
| 1,19 | Заряжена на 50% | 12,2 |
| 1.155 | Заряжена на 25% | 12 |
| Ниже 1.120 | Разряжена | 11,9 и ниже |
Крепление аккумуляторной батареи в автомобиле
Аккумуляторная батарея, во избежание ее повреждения, должна быть обязательно надежно закреплена в автомобиле. Под действием нормальной вибрации автомобиля активная масса может осыпаться с пластин аккумуляторной батареи. Зажимы и кронштейны крепления аккумуляторной батареи обеспечивают ослабление ее вибрации, которая может стать причиной значительного снижения емкости и ресурса любой аккумуляторной батареи.
Как часто нужно проверять уровень электролита в аккумуляторе?
- Главная /
- Статьи /
- Как часто нужно проверять уровень электролита в аккумуляторе?
Аккумулятор в системе автомобиля выполняет примерно ту же функцию, что и сердце. Именно он запускает мотор, а за ним – генератор, без которых невозможно никакое движение в принципе. Поэтому аккумулятор должен быть всегда исправен и заряжен, за этим следует следить. Одним из самых важных факторов правильной работы аккумулятора является уровень электролита. Во время работы аккумулятора, когда он отдаёт накопленный заряд, электролит теряет густоту, а часть его содержимого испаряется, что особенно заметно в тёплый сезон.
Характерным признаком отсутствия должного уровня является ситуация, когда машина не заводится. Причиной может быть разрядка аккумулятора, и проверить это можно по двум критериям – померить выходное напряжение и проверить плотность электролита. Чем меньше плотность – тем меньше заряд, и его, в конце концов может стать недостаточно для запуска двигателя.
Простейшая форма проверки – ареометром. Это прибор, который и предназначен для определения плотности электролита. Он похож на пипетку со специальным наконечником и специфическим поплавком внутри. Проводить проверку с помощью ареометра имеет смысл исключительно, если аккумулятор последний раз заряжался не ранее, чем шесть часов назад. Наиболее точные измерения получаются, когда температура воздуха вовне машины достигает +20 градусов Цельсия.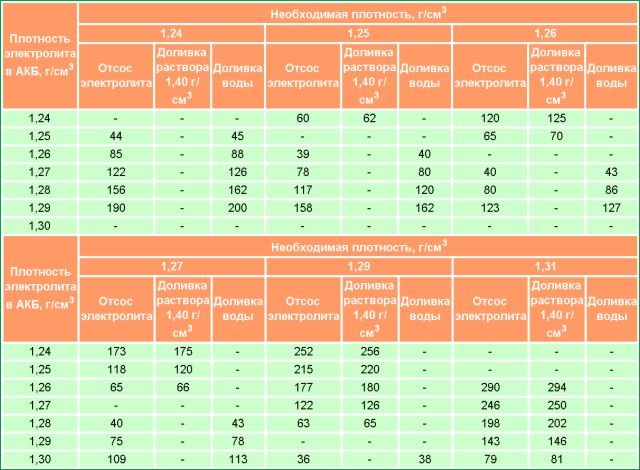 Если условия отличаются, проводить промер нужно в доме или в гараже, где они ближе к этой отметке. Это и делает данную проверку неудобной при поездках. Проводить такую проверку необходимо по крайней мере раз в месяц, если автомобиль работает нормально и эксплуатируется не ежедневно. При ежедневной эксплуатации необходимо проверять уровень хотя бы раз в неделю, а в зимнее время – лучше 2–3 раза в неделю.
Если условия отличаются, проводить промер нужно в доме или в гараже, где они ближе к этой отметке. Это и делает данную проверку неудобной при поездках. Проводить такую проверку необходимо по крайней мере раз в месяц, если автомобиль работает нормально и эксплуатируется не ежедневно. При ежедневной эксплуатации необходимо проверять уровень хотя бы раз в неделю, а в зимнее время – лучше 2–3 раза в неделю.
Когда проверку нужно проводить чаще, её делают мультиметром или тестером – после того, как автомобиль уже несколько часов не двигался. Поэтому самые достоверные показания будут после ночи. Показатели напряжённости аккумулятора с полным зарядом равны 12.66 В. 11.8 В – это состояние полной разрядки. Если напряжение падает меньше 11 В, необходимо менять аккумулятор, а старый утилизировать как непригодный.
Тщательное соблюдение режима проверки позволяет вовремя заряжать батарею зарядным устройством до полного заряда, а значит, значительно повышать ресурс её эксплуатации.
Войти
—
- О компании
- Адреса магазинов
- Клиентам
- Каталоги
- Франшиза
Название:
Номер:
Примечание:
ОК Отмена
- Самара, ул. Авроры, д. 30 квартира/офис » data-phone=»»> Самара г. Самара, ул. Авроры, д. 30 квартира/офис
- Екатеринбург г. Екатеринбург ул. Сибирский тракт, д. 8Н, 2 этаж квартира/офис
Экспериментальные измерения и моделирование вязкости и плотности тройных растворов хлоридов кальция и калия
1. Руис-Лламас А., Масиас-Салинас Р. Моделирование динамической вязкости ионных растворов. Инд.Инж. хим. Рез. 2015;54:7169–7179. doi: 10.1021/acs.iecr.5b01664. [CrossRef] [Google Scholar]
2. Магомедов Ю.Б., Алхасов А.Б. Динамическая вязкость водных растворов солей при высоких температурах, давлениях и концентрациях. Дж. Инж. физ. Термофиз. 2007; 80: 1216–1222. дои: 10.1007/s10891-007-0157-й. [CrossRef] [Google Scholar]
Дж. Инж. физ. Термофиз. 2007; 80: 1216–1222. дои: 10.1007/s10891-007-0157-й. [CrossRef] [Google Scholar]
3. Qiblawey H, Abu Jdayil B. Вязкость и плотность тройного раствора хлорида магния + хлорид натрия + вода от (293,15 до 318,15 K) J. Chem. англ. Данные. 2010;55:3322–3326. дои: 10.1021/je100111w. [CrossRef] [Google Scholar]
4. Васкес-Кастильоа Г., Иглесиас-Сильва Г.В., Холл К.Р. Расширение модели Макаллистера для корреляции кинематической вязкости растворов электролитов. Равновесие жидкой фазы. 2013; 58:44–49. doi: 10.1016/j.fluid.2013.07.052. [Перекрестная ссылка] [Академия Google]
5. Голдсак Д., Франкетто Р. Вязкость концентрированных растворов электролитов I. Концентрационная зависимость при фиксированной температуре. Может. Дж. Хим. 1977; 55: 1062–1072. дои: 10.1139/v77-148. [CrossRef] [Google Scholar]
6. Majali F, Ettouney H, Abdel-Jabbar N, Qiblawey H. Конструкция и эксплуатационные характеристики установок обратного осмоса пилотного масштаба. Опреснение. 2008; 222:441–450. doi: 10.1016/j.desal.2007.01.169. [CrossRef] [Google Scholar]
Опреснение. 2008; 222:441–450. doi: 10.1016/j.desal.2007.01.169. [CrossRef] [Google Scholar]
7. Qiblawey H, Banat F, Al-Nasser Q. Лабораторная установка для очистки воды с использованием бытовой установки обратного осмоса с фотоэлектрическим приводом. Десалин. Водное лечение. 2009 г.;7:53–59. doi: 10.5004/dwt.2009.695. [CrossRef] [Google Scholar]
8. Панагопулос А., Хараламбус К.Дж., Лоизиду М. Методы утилизации рассола и технологии очистки опреснения — обзор. науч. Общая окружающая среда. 2019;693:133545. doi: 10.1016/j.scitotenv.2019.07.351. [PubMed] [CrossRef] [Google Scholar]
9. Menon AK, Haechler I, Kaur S, et al. Усиленное солнечное испарение с использованием фототермического зонта для управления сточными водами. Нац. Поддерживать. 2020;3:144–151. doi: 10.1038/s41893-019-0445-5. [CrossRef] [Google Scholar]
10. Mohameed H, Ulrich J. Влияние значения pH на скорость роста и растворения хлорида калия. Кристалл. Рез. Технол. 1996; 31: 27–31. doi: 10. 1002/crat.2170310107. [CrossRef] [Google Scholar]
1002/crat.2170310107. [CrossRef] [Google Scholar]
11. Mohameed H, Abdel-Jabbar N, Takrouri K, Nasr A. Оптимальная стратегия охлаждения на основе моделей для периодических процессов кристаллизации. хим. англ. Рез. Дес. 2003; 81: 578–584. doi: 10.1205/026387603765444528. [CrossRef] [Google Scholar]
12. Ахмад Н., Баддур Р. Обзор источников, эффектов, методов утилизации и правил попадания рассола в морскую среду. Океанское побережье. Управление 2014;87:1–7. doi: 10.1016/j.ocecoaman.2013.10.020. [Перекрестная ссылка] [Академия Google]
13. Эрреро-Гонсалес М., Ной Адмон Н., Домингес-Рамос А., Ибаньес Р., Вольфсон А., Ирабиен А. Оценка экологической устойчивости валоризации рассола методом обратного осмоса морской воды с помощью электродиализа с биполярными мембранами. Окружающая среда. науч. Загрязн. Рез. 2020;27:1256–1266. doi: 10.1007/s11356-019-04788-w. [PubMed] [CrossRef] [Google Scholar]
14. Pollyea R, Chapman M, Jayne R, Hao WuH. Сброс сточных вод с нефтяных месторождений с высокой плотностью вызывает более глубокие, сильные и продолжительные землетрясения. Нац. коммун. 2019;10:3077. doi: 10.1038/s41467-019-11029-8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Нац. коммун. 2019;10:3077. doi: 10.1038/s41467-019-11029-8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Kim B, et al. Очистка высокоминерализованных солевых растворов многоступенчатым ионно-концентрационным поляризационным опреснением. науч. Отчет 2016; 6: 31850. doi: 10.1038/srep31850. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
16. Джованни Г., Пабло С. Эффекты кинетической вязкости растворителя как зонды для изучения механизмов действия ферментов. Биохимия. 2018;57:3445–3453. doi: 10.1021/acs.biochem.8b00232. [PubMed] [CrossRef] [Академия Google]
17. Huitian J, Walid E, Aboudheir A, Mahinpey N. Плотность, вязкость, показатель преломления и электропроводность деградированных растворов моноэтаноламина при стандартных температурах. Дж. Хим. англ. Данные. 2018; 63:1969–1976. doi: 10.1021/acs.jced.7b01101. [CrossRef] [Google Scholar]
18. Qiblawey H, Arshad MH, Easa A, Atilhan M. Вязкость и плотность тройного раствора хлорида кальция + хлорид натрия + вода от T = (293,15 до 323,15) K. J. Chem. англ. Данные. 2014;59:2133–2143. doi: 10.1021/je500070k. [Перекрестная ссылка] [Академия Google]
J. Chem. англ. Данные. 2014;59:2133–2143. doi: 10.1021/je500070k. [Перекрестная ссылка] [Академия Google]
19. Чжан Х.Л., Чен Г.Х., Хань С.Дж. Вязкость и плотность H 2 O + NaCl + CaCl 2 и H 2 O + KCl + CaCl 2 при 298,15 К. J. Chem. англ. Данные. 1997; 42: 526–530. doi: 10.1021/je9602733. [CrossRef] [Google Scholar]
20. Out DJP, Los JM. Вязкость водного раствора одновалентных электролитов от 5 до 95 °С. Дж. Солют. хим. 1980; 9:19–35. doi: 10.1007/BF00650134. [CrossRef] [Google Scholar]
21. Цзян Дж., Стэнли И.С. Новая модель вязкости растворов электролитов. Инд.Инж. хим. Рез. 2003;42:6267–6272. doi: 10.1021/ie0210659. [CrossRef] [Google Scholar]
22. Кестин Дж., Шенкленд И.Р., Пол Р. Вязкость водных растворов KCl в диапазоне температур 25–200 и диапазоне давлений 0,1–30 МПа. Междунар. Дж. Термофиз. 1981;2(4):301–314. doi: 10.1007/BF00498761. [CrossRef] [Google Scholar]
23. Каминский М. Концентрация и температурная зависимость вязкости водных растворов сильных электролитов. III. KCl, K 2 SO 4 , MgCl 2 , BeSO 4 и MgSO 4 растворы. З. Физ. хим. 1957; 12: 206–231. doi: 10.1524/зпч.1957.12.3_4.206. [CrossRef] [Google Scholar]
III. KCl, K 2 SO 4 , MgCl 2 , BeSO 4 и MgSO 4 растворы. З. Физ. хим. 1957; 12: 206–231. doi: 10.1524/зпч.1957.12.3_4.206. [CrossRef] [Google Scholar]
24. Маркус Ю. Влияние ионов на структуру воды: создание и разрушение структуры. хим. 2009; 109:1346–1370. doi: 10.1021/cr8003828. [PubMed] [CrossRef] [Google Scholar]
25. Leyendekkers JV. Вязкость водных растворов электролитов и модель ТТГ. Дж. Солют. хим. 1979;8(12):853–859. doi: 10.1007/BF00644882. [Перекрестная ссылка] [Академия Google]
26. Goldsack DE, Franchetto RC. Вязкость концентрированных растворов электролитов. II. Температурная зависимость. Может. Дж. Хим. 1978; 56: 1442–1450. дои: 10.1139/v78-236. [CrossRef] [Google Scholar]
27. Zafarani-Moattar MT, Majdan-Cegincara RM. Моделирование и прогнозирование вязкости водных смешанных растворов электролитов. Инд.Инж. хим. Рез. 2009; 48: 5833–5844. doi: 10.1021/ie801933u. [CrossRef] [Google Scholar]
28. Hu Y, Zhang X, Jin C, Peng X. Теория полуидеального решения. 3. Расширение вязкости многокомпонентных водных растворов. Дж. Солют. хим. 2010;39: 1828–1844. doi: 10.1007/s10953-010-9565-2. [CrossRef] [Google Scholar]
Hu Y, Zhang X, Jin C, Peng X. Теория полуидеального решения. 3. Расширение вязкости многокомпонентных водных растворов. Дж. Солют. хим. 2010;39: 1828–1844. doi: 10.1007/s10953-010-9565-2. [CrossRef] [Google Scholar]
29. Абдулагатов ИМ, Азизов НД. Вязкость водных растворов хлорида кальция при высоких температурах и высоких давлениях. Равновесие жидкой фазы. 2006; 240:204–219. doi: 10.1016/j.fluid.2005.12.036. [CrossRef] [Google Scholar]
30. Zhang J, Moosavi M, Rostami AA, Vargas MM. Моделирование вязкости смесей вода + алкандиолы. Дж. Мол. жидкость 2018; 249:326–333. doi: 10.1016/j.molliq.2017.11.005. [Перекрестная ссылка] [Академия Google]
31. Лалиберте М. Модель расчета теплоемкости водных растворов с обновленными данными о плотности и вязкости. Дж. Хим. англ. Данные. 2009; 54: 1725–1760. doi: 10.1021/je8008123. [CrossRef] [Google Scholar]
32. Гонсалвес Ф.А., Кестин Дж. Вязкость растворов CaCl 2 в диапазоне 20–50 °C. Бер. Бунзенгес. физ.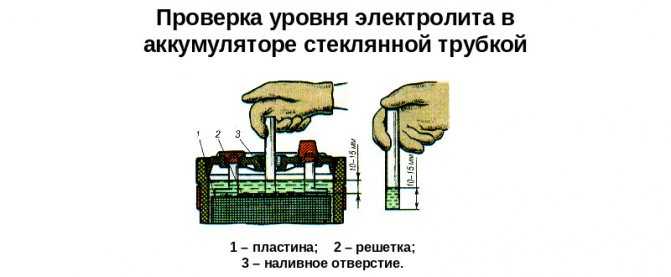 хим. 1979; 83: 24–27. doi: 10.1002/bbpc.19790830105. [CrossRef] [Google Scholar]
хим. 1979; 83: 24–27. doi: 10.1002/bbpc.19790830105. [CrossRef] [Google Scholar]
33. Александров А.А., Джураева Е.В., Утенков В.Ф. Вязкость водного раствора хлорида натрия. Высокий темп. 2012;50:354–358. дои: 10.1134/S0018151X12030029. [CrossRef] [Google Scholar]
34. Кестин Дж., Халифа Х.Э., Коррейя Р.Дж. Таблицы динамической и кинематической вязкости водных растворов NaCl в интервале температур 20–150 °С и диапазоне давлений 0,1–35 МПа. Дж. Физ. хим. Ссылка Данные. 1981; 10: 71–80. дои: 10.1063/1.555641. [CrossRef] [Google Scholar]
35. Hu YF, Lee H. Прогнозирование вязкости смешанного раствора электролита на основе абсолютной теории Эрвина и полуидеальной модели гидратации. Электрохим. Акта. 2003;48:1789–1796. doi: 10.1016/S0013-4686(03)00226-3. [CrossRef] [Google Scholar]
36. Glasstone S, Laidler KJ, Eyring H. Theory of Rate Process. Нью-Йорк: Макгроу-Хилл; 1941. [Google Scholar]
37. Кумар А. Простые уравнения для прогнозирования объемных свойств водных концентрированных смесей электролитов. проц. Индийская акад. науч. хим. науч. 1986; 96: 97–101. [Google Scholar]
проц. Индийская акад. науч. хим. науч. 1986; 96: 97–101. [Google Scholar]
38. Yang J, et al. Систематическое изучение простых подходов к прогнозированию термодинамических и транспортных свойств многокомпонентных растворов. Инд.Инж. хим. Рез. 2010;49: 7671–7677. doi: 10.1021/ie100752w. [CrossRef] [Google Scholar]
39. Махиуддин С., Исмаил К. Зависимость вязкости системы Mg(NO3) 2 –H 2 O от температуры и концентрации. Может. Дж. Хим. 1982; 60: 2883–2888. дои: 10.1139/v82-413. [CrossRef] [Google Scholar]
40. Махиуддин С., Исмаил К. Концентрационная зависимость вязкости водных растворов электролитов от более высокой концентрации. Дж. Физ. хим. 1983; 87: 5241–5244. doi: 10.1021/j150643a036. [Перекрестная ссылка] [Академия Google]
41. Афзал М., Салим М., Махмуд М.Т. Температурная и концентрационная зависимость вязкости водных электролитов от 20 до 50 °С. Хлориды Na+, K+, Mg2+, Ca2+, Ba2+, Sr2+, Co2+, Ni2+, Cu2+ и Cr3+ J. Chem. англ. Данные. 1989; 34: 339–346. doi: 10.1021/je00057a023. [CrossRef] [Google Scholar]
Данные. 1989; 34: 339–346. doi: 10.1021/je00057a023. [CrossRef] [Google Scholar]
42. Goldsack DE, Franchetto AA. Вязкость концентрированных растворов электролитов. III. Закон смеси. Электрохим. Акта. 1977; 22: 1287–1294. doi: 10.1016/0013-4686(77)87012-6. [Перекрестная ссылка] [Академия Google]
43. Новлан М.Ф. Прогнозирование вязкости растворов смешанных электролитов по данным по одной соли. Может. Дж. Хим. англ. 1980; 58: 637–642. doi: 10.1002/cjce.5450580514. [CrossRef] [Google Scholar]
44. Патвардхан В.С., Кумар А. Единый подход к прогнозированию термодинамических свойств водных растворов смешанных электролитов. Часть I: давление пара и теплота парообразования. Айше Дж. 1986; 32:1419–1428. doi: 10.1002/aic.690320903. [CrossRef] [Google Scholar]
45. Патвардхан В.С., Кумар А. Единый подход к прогнозированию термодинамических свойств водных растворов смешанных электролитов. Часть II: объемные, тепловые и другие свойства. Айше Дж. 1986;32:1429–1438. doi: 10. 1002/aic.690320904. [CrossRef] [Google Scholar]
1002/aic.690320904. [CrossRef] [Google Scholar]
46. Sun, Y. et al. Экспериментальные и модельные исследования плотности водных растворов хлорида 1-карбоксиметил-3-метилимидазолия, хлорида 1-карбоксиметил-3-пропилимидазолия и хлорида 1-(2-гидроксиэтил)-3-пропилимидазолия при (29315, 29815 и 30315) ) К. J. Chem. англ. Данные 59 , 250–249 (2014).
Руководство для начинающих по обслуживанию аккумулятора гольф-кара
Электрические тележки для гольфа работают от аккумуляторов. Небольшое упреждающее техническое обслуживание может иметь большое значение для продления срока службы батареи, снижения потребности в ремонте батареи и даже для оптимизации производительности вашей электрической тележки для гольфа.
Но знание важности обслуживания аккумуляторной батареи тележки для гольфа — это одно. Знать, какие задачи решать, это другое! Именно поэтому мы собрали следующие задания своими руками, с которыми справятся даже новички. Если у вас есть какие-либо вопросы или вы хотите купить тележки для гольфа на продажу, отправляйтесь в Connecticut Trailers. Наш дилерский центр находится в Болтоне, штат Коннектикут, мы также обслуживаем тех, кто находится в Хартфорде и по всей Новой Англии.
Если у вас есть какие-либо вопросы или вы хотите купить тележки для гольфа на продажу, отправляйтесь в Connecticut Trailers. Наш дилерский центр находится в Болтоне, штат Коннектикут, мы также обслуживаем тех, кто находится в Хартфорде и по всей Новой Англии.
Получить базовый уровень
Когда вы впервые покупаете электрическую тележку для гольфа, убедитесь, что она полностью заряжена, прежде чем отправиться в свое первое путешествие. Затем обратите особое внимание на то, как быстро разряжается батарея. Это дает вам базовую оценку времени автономной работы, которая может служить полезным сравнением в будущем. Если вы вдруг заметили, что аккумулятор вашего гольф-кара разряжается намного быстрее, чем обычно, это может указывать на проблему технического обслуживания, которую необходимо решить.
Используйте надлежащую практику зарядки
Лучше не допускать полной разрядки аккумулятора электромобиля для гольфа. Вместо этого попытайтесь зарядить его до того, как он достигнет этой точки. Вы не хотите часто видеть мигающий индикатор заряда батареи!
Вы не хотите часто видеть мигающий индикатор заряда батареи!
Очистка аккумулятора от кислоты
В процессе зарядки аккумулятора тележки для гольфа происходит выделение газообразного водорода, воды и кислоты. Эта смесь может осесть на различных компонентах тележки для гольфа. Оставленный слишком долго, он начнет разъедать эти части.
Важно регулярно очищать аккумуляторную батарею от электролита, чтобы избежать повреждения дорогостоящего гольф-мобиля. Начните с закрытия всех вентиляционных крышек и закройте все электрические части. Затем смешайте столовую ложку пищевой соды со стаканом горячей воды. Используя старую зубную щетку, нанесите эту смесь на клеммы аккумулятора тележки для гольфа. Как только коррозия будет удалена, смойте пищевую соду струей прохладной воды. Затем протрите батарею, пока она не станет полностью чистой.
Добавить нужное количество воды
Аккумуляторы тележки для гольфа вырабатывают электричество с использованием электролитов и воды, а это означает, что время от времени вам нужно будет добавлять еще немного воды. Но будьте осторожны с количеством! Слишком много воды может привести к переливу электролитов. Слишком мало воды может вызвать сульфатацию, которая повреждает свинцовые пластины.
Но будьте осторожны с количеством! Слишком много воды может привести к переливу электролитов. Слишком мало воды может вызвать сульфатацию, которая повреждает свинцовые пластины.
Используйте пистолет для полива, чтобы повысить точность при добавлении воды, что поможет вам добавить нужное количество. Не забывайте всегда использовать дистиллированную воду. Если возможно, попробуйте залить воду после того, как батарея будет заряжена. Это поможет повысить уровень электролитов.
Периодически проверяйте аккумулятор тележки для гольфа
Время от времени проверяйте батарею тележки для гольфа в течение минуты или двух. Все, что вам нужно, это ареометр для проверки элементов батареи, который измеряет плотность электролитов по сравнению с весом. Более высокий удельный вес говорит о более высоком уровне заряда и более плотном присутствии электролитов. По мере использования аккумулятор тележки для гольфа разряжается, и вес электролита уменьшается.
Используйте прибор для измерения уровня заряда батареи
Датчики уровня заряда батареи являются полезным инструментом для контроля глубины разрядки. Использование этой информации может помочь вам своевременно перезарядить аккумулятор (до того, как он полностью разрядится).
Однако, если у вас более старая модель, индикаторы заряда батареи не всегда дают самые точные показания. Лучшим инструментом для вас будет тестер нагрузки аккумулятора.
Используйте правильные стратегии замены
В конце концов, придет время заменить аккумулятор тележки для гольфа. Часто вы будете замечать повторяющиеся проблемы с производительностью, которые указывают на необходимость замены батареи.
Заманчиво заменить только одну батарею, которая больше не работает, но постарайтесь сопротивляться этому желанию. Когда новые и старые батареи заряжаются одновременно, они заряжаются с разной скоростью. Старые заряжаются медленнее, что приводит к перезарядке новых аккумуляторов (и из-за этого сокращается срок их службы).
