Электрический аккумулятор — это… Что такое Электрический аккумулятор?
{б{redirect|Аккумулятор|Аккумулятор (значения)}}

Электри́ческий аккумуля́тор — химический источник тока многоразового действия, основная специфика которого заключается в обратимости внутренних химических процессов, что обеспечивает его многократное циклическое использование (через заряд-разряд[1]) для накопления энергии и автономного электропитания различных электротехнических устройств и оборудования[2].
Принцип действия
 Замена аккумуляторной батареи на электропогрузчике
Замена аккумуляторной батареи на электропогрузчикеПринцип действия аккумулятора основан на обратимости химической реакции. Работоспособность аккумулятора может быть восстановлена путём заряда, то есть пропусканием электрического тока в направлении, обратном направлению тока при разряде.
Несколько аккумуляторов, объединённых в одну электрическую цепь, составляют
Характеристики
Максимально возможный полезный заряд аккумулятора называется зарядной ёмкостью, или просто ёмкостью. Ёмкость аккумулятора — это заряд, отдаваемый полностью заряженным аккумулятором при разряде до наименьшего допустимого напряжения. В системе СИ ёмкость аккумуляторов измеряют в кулонах, на практике часто используется внесистемная единица — ампер-час. 1 А⋅ч = 3600 Кл.
Реже на аккумуляторах указывается энергетическая ёмкость — энергия, отдаваемая полностью заряженным аккумулятором при разряде до наименьшего допустимого напряжения. В системе СИ она измеряется в джоулях, на практике иногда используется внесистемная единица — ватт-час. 1 Вт⋅ч = 3600 Дж.
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы:
| Тип | ЭДС (В) | Область применения |
|---|---|---|
| свинцово-кислотные (Lead Acid) | 2,1 | троллейбусы, трамваи, воздушные суда, автомобили, мотоциклы, электропогрузчики, штабелеры, электротягачи, аварийное электроснабжение, источники бесперебойного питания |
| никель-кадмиевые (NiCd) | 1,2 | замена стандартного гальванического элемента, строительные электроинструменты, троллейбусы, воздушные суда |
| никель-металл-гидридные (NiMH) | 1,2 | замена стандартного гальванического элемента, электромобили |
| литий-ионные (Li‑ion) | 3,7 | мобильные устройства, строительные электроинструменты, электромобили |
| литий-полимерные (Li‑pol) | 3,7 | мобильные устройства, электромобили |
| никель-цинковые (NiZn) | 1,6 | замена стандартного гальванического элемента |
По мере исчерпания химической энергии напряжение и ток падают, аккумулятор перестаёт действовать. Зарядить аккумулятор (батарею аккумуляторов) можно от любого источника постоянного тока с бо́льшим напряжением при ограничении тока. Стандартным считается зарядный ток (в амперах) в 1/10 номинальной ёмкости аккумулятора (в ампер⋅часах). Многие типы аккумуляторов имеют различные ограничения, которые необходимо учитывать при зарядке и последующей эксплуатации, например NiMH-аккумуляторы чувствительны к перезаряду, литиевые — к переразряду, напряжению и температуре. NiCd- и NiMH-аккумуляторы имеют так называемый эффект памяти, заключающийся в снижении ёмкости, в случае когда зарядка осуществляется при не полностью разряженном аккумуляторе. Также эти типы аккумуляторов обладают заметным саморазрядом, то есть они постепенно теряют заряд, даже не будучи подключенными к нагрузке. Для борьбы с этим эффектом может применяться капельная подзарядка.
Типы аккумуляторов
См. также
Примечания
Ссылки
dic.academic.ru
Электрический аккумулятор — Википедия
Зарядное устройство «Duracell», позволяющее заряжать, как обычные пальчиковые аккумуляторы (видны пружинные прижимы для них), так и аккумуляторы типа «Крона». Во время зарядки горят индикаторыЭлектри́ческий аккумуля́тор — химический источник тока, источник ЭДС многоразового действия, основная специфика которого заключается в обратимости внутренних химических процессов, что обеспечивает его многократное циклическое использование (через заряд-разряд) для накопления энергии и автономного электропитания различных электротехнических устройств и оборудования, а также для обеспечения резервных источников энергии в медицине, производстве, транспорте и в других сферах.
Значение и употребление слова
Термин «аккумулятор» используется для обозначения:
- отдельного элемента: например, аккумулятор, аккумуляторная банка, аккумуляторная ячейка.
- нескольких отдельных элементов, соединённых последовательно (для увеличения напряжения) или параллельно (для увеличения силы тока) друг с другом: например, аккумуляторная батарея.
История
Первый прообраз аккумулятора, который в отличие от батареи Алессандро Вольты можно было многократно заряжать, был создан в 1803 году Иоганном Вильгельмом Риттером. Его аккумуляторная батарея представляла собой столб из пятидесяти медных кружочков, между которыми было проложено влажное сукно. После пропускания через данное устройство тока от вольтова столба, оно само стало вести себя как источник электричества[1].
Принцип действия
Принцип действия аккумулятора основан на обратимости химической реакции. Работоспособность аккумулятора может быть восстановлена путём заряда, то есть пропусканием электрического тока в направлении, обратном направлению тока при разряде. Несколько аккумуляторов, объединённых в одну электрическую цепь, составляют аккумуля́торную батаре́ю.
Свинцово-кислотный аккумулятор
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в растворе серной кислоты.
Химическая реакция (слева направо — разряд, справа налево — заряд):
- Pb+SO42−−2e−⇆PbSO4{\displaystyle Pb+SO_{4}^{2-}-2e^{-}\leftrightarrows PbSO_{4}}
- PbO2+SO42−+4H++2e−⇆PbSO4+2h3O{\displaystyle PbO_{2}+SO_{4}^{2-}+4H^{+}+2e^{-}\leftrightarrows PbSO_{4}+2H_{2}O}
Литий-ионный аккумулятор
Литий-ионный аккумулятор состоит из электродов (катодного материала на алюминиевой фольге и анодного материала на медной фольге), разделённых пропитанными электролитом пористыми сепараторами. Переносчиком заряда в литий-ионном аккумуляторе является положительно заряженный ион лития, который внедряется (интеркалируется) в кристаллическую решетку других материалов (например, в графит, оксиды и соли металлов) с образованием химической связи (например: в графит с образованием LiC6, оксиды (LiMO2) и соли (LiMRON) металла).
Алюминий-ионный аккумулятор состоит из металлического алюминиевого анода, катода из графита в виде пены и жидкого ионного невоспламеняющегося электролита. Батарея работает по принципу электрохимического осаждения: происходит растворение алюминия на аноде, далее в среде жидкого электролита анионы хлоралюмината интеркалируют в графит. Количество возможных перезарядок батареи — более 7,5 тыс. циклов без потери мощности[2][3].
Характеристики
Ёмкость аккумулятора
За ёмкость аккумулятора чаще всего принимают количество электричества равное 1 Кл, при силе тока 1 А в течение 1 с, (при переводе времени в часы получаем 1 А*ч=3600 Кл). Однако принимают, а не измеряют. Существует распространенное заблуждение, что ёмкость аккумулятора измеряется в А*ч, это не совсем так, т. к. в 1 А*с=1 Кл или 1 А*ч=3600 Кл измеряется количество электричества или электрический заряд; по формуле Q= I*t, где Q -количество электричества или электрический заряд, I — сила тока, t — время протекания электрического тока. Например, обозначение «12 В на 55 А*ч» означает, что аккумулятор выдаёт количество электричества 198 кКл (кило Кулон) по какому-либо контуру, при токе разряда 55 А за 1 ч (3600 с) до порогового напряжения 10,8 В. Расчёт показывает, что при токе разряда в 255 А аккумулятор разрядится за 12,9 минут. Как видно 55 А*ч — это не ёмкость (электрическая ёмкость измеряется в Фарадах, 1 Ф= 1 Кл/В). Поэтому на аккумуляторе написано количество электричества Q, которое он выдаёт при определённом токе разряда и определённом времени его прохождения.[источник не указан 610 дней]
Плотность энергии
Плотность энергии — количество энергии на единицу объёма или единицу веса аккумулятора (см. ст. Плотность энергии).
Саморазряд
Саморазряд — это потеря аккумулятором заряда после полной зарядки при отсутствии нагрузки. Саморазряд проявляется по-разному у разных типов аккумуляторов, но всегда максимален в первые часы после заряда, а после — замедляется.
Для Ni-Cd аккумуляторов считают допустимым не более 10 % саморазряда за первые 24 часа после проведения зарядки. Для Ni-MH саморазряд чуть меньше. У Li-ion он пренебрежимо мал и значительно себя проявляет только в течение нескольких месяцев.
В свинцово-кислотных герметичных аккумуляторах саморазряд составляет около 40 % за 1 год хранения при 20°С, 15 % — при 5°С. Если температуры хранения более высокие, то саморазряд возрастает: батареи при 40°С теряют ёмкости 40 % всего за 4-5 месяцев.
Температурный режим
Следует беречь аккумуляторы от огня и воды, чрезмерного нагревания и охлаждения, резких перепадов температур.
Не следует использовать аккумуляторы при температурах выше +50°С и ниже −25°С. При эксплуатации аккумулятора в условиях «холодной зимы» рекомендуется его снимать и хранить в тёплом помещении. Нарушение температурного режима может привести к сокращению срока службы или потере работоспособности.
Тип аккумулятора
Тип аккумулятора определяется используемыми материалами. Различают следующие:
- Cn-Po — Графен-полимерный аккумулятор.
- La-Ft — лантан-фторидный аккумулятор
- Li-Ion — литий-ионный аккумулятор (3,2-4,2 V), общее обозначение для всех литиевых аккумуляторов
- Li-Co — литий-кобальтовый аккумулятор, (3,6 V), на базе LiCoO2, технология в процессе освоения
- Li-Po — литий-полимерный аккумулятор (3,7 V), полимер в качестве электролита
- Li-Ft — литий-фторный аккумулятор
- Li-Mn — литий-марганцевый аккумулятор (3,6 V) на базе LiMn2O4
- LiFeS — литий-железно-сульфидный аккумулятор (1,35 V)[источник не указан 209 дней]
- LiFeP или LFP — Литий-железно-фосфатный аккумулятор (3,3 V) на базе LiFePO4
- LiFeYPO4 — литий-железо-иттрий-фосфатный (Добавка иттрия для улучшения свойств)
- Li-Ti — литий-титанатный аккумулятор (3,2 V) на базе Li4Ti5О12
- Li-Cl — литий-хлорный аккумулятор (3,99 V)
- Li-S — литий-серный аккумулятор (2,2 V)
- LMPo — литий-металл-полимерный аккумулятор
- Fe-air — железо-воздушный аккумулятор
- Na/NiCl — никель-солевой аккумулятор (2,58 V)
- Na-S — натрий-серный аккумулятор, (2 V), высокотемпературный аккумулятор
- Ni-Cd — никель-кадмиевый аккумулятор (1,2 V)
- Ni-Fe — железо-никелевый аккумулятор (1,2-1,9 V)
- Ni-H2 — никель-водородный аккумулятор (1,5 V)
- Ni-MH — никель-металл-гидридный аккумулятор (1,2 V)
- Ni-Zn — никель-цинковый аккумулятор (1,65 V)
- Pb — свинцово-кислотный аккумулятор (2 V)
- Pb-H — свинцово-водородный аккумулятор
- Ag-Zn — серебряно-цинковый аккумулятор (1,85 V)
- Ag-Cd — серебряно-кадмиевый аккумулятор (1,6 V)
- Zn-Br — цинк-бромный аккумулятор (1,8 V)
- Zn-air — цинк-воздушный аккумулятор
- Zn-Cl — цинк-хлорный аккумулятор
- RAM (Rechargeable Alkaline Manganese) — перезаряжаемая разновидность марганцево-цинкового щелочного гальванического элемента (1,5 V)[источник не указан 537 дней]
- Ванадиевый аккумулятор (1,41 V)[источник не указан 537 дней]
- Алюминиево-графитный аккумулятор (2 V)[источник не указан 537 дней]
- Алюминиево-ионный аккумулятор (2 V)[4]
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы:
| Тип | ЭДС (В) | Область применения |
|---|---|---|
| свинцово-кислотные Pb | 2,1 | троллейбусы, трамваи, воздушные суда, автомобили, мотоциклы, электропогрузчики, штабелеры, электротягачи, аварийное электроснабжение, источники бесперебойного питания |
| никель-кадмиевые Ni-Cd | 1,2 | замена стандартного гальванического элемента, строительные электроинструменты, троллейбусы, воздушные суда |
| никель-металл-гидридные Ni-MH | 1,2 | замена стандартного гальванического элемента, электромобили |
| литий-ионные Li‑ion | 3,7 | мобильные устройства, строительные электроинструменты, электромобили |
| литий-полимерные Li‑pol | 3,7 | мобильные устройства, электромобили |
| никель-цинковые Ni-Zn | 1,6 | замена стандартного гальванического элемента |
По мере исчерпания химической энергии напряжение и ток падают, аккумулятор перестаёт действовать. Зарядить аккумулятор (батарею аккумуляторов) можно от любого источника постоянного тока с бо́льшим напряжением при ограничении тока. Наиболее распространённым считается зарядный ток (в амперах), пропорциональный 1/10 условной номинальной ёмкости аккумулятора (в ампер⋅часах).
Однако, основываясь на техническом описании, распространяемом изготовителями широко применяемых электрических аккумуляторов (NiMH, NiCd), можно сделать предположение о том, что данный режим заряда, обычно именуемый стандартным, рассчитывается исходя из продолжительности восьмичасового рабочего дня, когда разряженный в конце рабочего дня аккумулятор подключается к сетевому зарядному устройству до начала нового рабочего дня. Применение такого режима заряда для этих типов аккумуляторов при систематическом использовании позволяет соблюсти качественно-стоимостной баланс эксплуатации изделия. Таким образом, с подачи изготовителя данный режим можно применять только для никель-кадмиевых и никель-металл-гидридных аккумуляторов.
Многие типы аккумуляторов имеют различные ограничения, которые необходимо учитывать при зарядке и последующей эксплуатации, например NiMH-аккумуляторы чувствительны к перезаряду, литиевые — к переразряду, напряжению и температуре. NiCd- и NiMH-аккумуляторы имеют так называемый эффект памяти, заключающийся в снижении ёмкости в случае, когда зарядка осуществляется при не полностью разряженном аккумуляторе. Также эти типы аккумуляторов обладают заметным саморазрядом, то есть они постепенно теряют заряд, не будучи подключенными к нагрузке. Для борьбы с этим эффектом может применяться капельная подзарядка.
В большинстве случаев возможность систематического использования аккумуляторов есть только в портативных устройствах радиосвязи и иной цифровой технике, где используются литий-ионные аккумуляторы и система контроля заряда-разряда встроена в устройство. В бюджетном сегменте «простые» никель-металл-гидридные и никель-кадмиевые аккумуляторы используются в качестве бюджетной замены щелочных элементов питания. В качестве источника тока для бюджетного аккумуляторного электроинструмента используются никель-кадмиевые аккумуляторы. Если в первом случае обычно есть возможность выбирать между бюджетным устройством «стандартного» заряда и зарядным устройством с контролем заряда (капельный заряд, импульсный заряд, ускоренный заряд с контролем напряжения и т. д.), то во втором случае изделие комплектуется, как правило, с трансформаторным источником питания для зарядки постоянным током, что при несоблюдении технических условий эксплуатации аккумулятора снижает срок его службы.
Форм-факторы
Внешний аккумулятор
Внешний аккумулятор (аккумуляторная батарея) — устройство для многократной подзарядки мобильного устройства (телефона, смартфона, планшетного компьютера) при отсутствии источника переменного тока (электросети).
Причиной появления этих устройств стало то, что при активном использовании современных смартфонов и планшетов заряда их аккумуляторов хватает на сравнительно короткое время — полдня или день. Для их зарядки в полевых условиях и были разработаны портативные аккумуляторы[5][6]. Типичный вес таких устройств — от нескольких сотен грамм, ёмкость от нескольких тысяч мА*ч до 10-20 А*ч[7]. С их помощью можно зарядить телефон 2-3 раза. Чаще всего они предоставляют для подключения порт USB. Некоторые из них имеют разъёмы или переходники для популярных разъёмов мобильных телефонов. Внешние аккумуляторы больших ёмкостей могут иметь переходники для зарядки ноутбуков. Иногда на внешних аккумуляторах имеется индикатор заряда или встроенный светодиодный фонарик.
Методы заряда аккумуляторов
Для заряда аккумуляторов применяется несколько методов. Как правило, метод заряда зависит от типа аккумулятора и обеспечивается зарядным устройством[8].
Медленный заряд постоянным током
Заряд постоянным током, пропорциональным 0.1-0.2 условной номинальной ёмкости Q в течение примерно 15-7 часов соответственно.
Самый длительный и безопасный метод заряда. Подходит для большинства типов аккумуляторов.
Быстрый заряд
Заряд постоянным током, пропорциональным 1/3 Q в течение примерно 3—5 часов.
Ускоренный или «дельта-V» заряд
Заряд с начальным током заряда, пропорциональным величине условной номинальной ёмкости аккумулятора, при котором постоянно измеряется напряжение аккумулятора и заряд заканчивается после того, как аккумулятор полностью заряжен. Время заряда — примерно час-полтора. Возможен разогрев аккумулятора и даже его разрушение.
Реверсивный заряд
Выполняется чередованием длинных импульсов заряда с короткими импульсами разряда. Реверсивный метод наиболее полезен для заряда NiCd и NiMH аккумуляторов, для которых характерен т. н. «эффект памяти».
См. также
Примечания
Литература
Ссылки
wikipedia.green
Электрический аккумулятор — Википедия. Что такое Электрический аккумулятор
 Зарядное устройство «Duracell», позволяющее заряжать, как обычные пальчиковые аккумуляторы (видны пружинные прижимы для них), так и аккумуляторы типа «Крона». Во время зарядки горят индикаторы
Зарядное устройство «Duracell», позволяющее заряжать, как обычные пальчиковые аккумуляторы (видны пружинные прижимы для них), так и аккумуляторы типа «Крона». Во время зарядки горят индикаторыЭлектри́ческий аккумуля́тор — химический источник тока, источник ЭДС многоразового действия, основная специфика которого заключается в обратимости внутренних химических процессов, что обеспечивает его многократное циклическое использование (через заряд-разряд) для накопления энергии и автономного электропитания различных электротехнических устройств и оборудования, а также для обеспечения резервных источников энергии в медицине, производстве, транспорте и в других сферах.
Значение и употребление слова
Термин «аккумулятор» используется для обозначения:
- отдельного элемента: например, аккумулятор, аккумуляторная банка, аккумуляторная ячейка.
- нескольких отдельных элементов, соединённых последовательно (для увеличения напряжения) или параллельно (для увеличения силы тока) друг с другом: например, аккумуляторная батарея.
История
Первый прообраз аккумулятора, который в отличие от батареи Алессандро Вольты можно было многократно заряжать, был создан в 1803 году Иоганном Вильгельмом Риттером. Его аккумуляторная батарея представляла собой столб из пятидесяти медных кружочков, между которыми было проложено влажное сукно. После пропускания через данное устройство тока от вольтова столба, оно само стало вести себя как источник электричества[1].
Принцип действия

Принцип действия аккумулятора основан на обратимости химической реакции. Работоспособность аккумулятора может быть восстановлена путём заряда, то есть пропусканием электрического тока в направлении, обратном направлению тока при разряде. Несколько аккумуляторов, объединённых в одну электрическую цепь, составляют аккумуля́торную батаре́ю.
Свинцово-кислотный аккумулятор
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в растворе серной кислоты.
Химическая реакция (слева направо — разряд, справа налево — заряд):
- Pb+SO42−−2e−⇆PbSO4{\displaystyle Pb+SO_{4}^{2-}-2e^{-}\leftrightarrows PbSO_{4}}
- PbO2+SO42−+4H++2e−⇆PbSO4+2h3O{\displaystyle PbO_{2}+SO_{4}^{2-}+4H^{+}+2e^{-}\leftrightarrows PbSO_{4}+2H_{2}O}
Литий-ионный аккумулятор
Литий-ионный аккумулятор состоит из электродов (катодного материала на алюминиевой фольге и анодного материала на медной фольге), разделённых пропитанными электролитом пористыми сепараторами. Переносчиком заряда в литий-ионном аккумуляторе является положительно заряженный ион лития, который внедряется (интеркалируется) в кристаллическую решетку других материалов (например, в графит, оксиды и соли металлов) с образованием химической связи (например: в графит с образованием LiC6, оксиды (LiMO2) и соли (LiMRON) металла).
Алюминий-ионный аккумулятор состоит из металлического алюминиевого анода, катода из графита в виде пены и жидкого ионного невоспламеняющегося электролита. Батарея работает по принципу электрохимического осаждения: происходит растворение алюминия на аноде, далее в среде жидкого электролита анионы хлоралюмината интеркалируют в графит. Количество возможных перезарядок батареи — более 7,5 тыс. циклов без потери мощности[2][3].
Характеристики
Ёмкость аккумулятора
За ёмкость аккумулятора чаще всего принимают количество электричества равное 1 Кл, при силе тока 1 А в течение 1 с, (при переводе времени в часы получаем 1 А*ч=3600 Кл). Однако принимают, а не измеряют. Существует распространенное заблуждение, что ёмкость аккумулятора измеряется в А*ч, это не совсем так, т. к. в 1 А*с=1 Кл или 1 А*ч=3600 Кл измеряется количество электричества или электрический заряд; по формуле Q= I*t, где Q -количество электричества или электрический заряд, I — сила тока, t — время протекания электрического тока. Например, обозначение «12 В на 55 А*ч» означает, что аккумулятор выдаёт количество электричества 198 кКл (кило Кулон) по какому-либо контуру, при токе разряда 55 А за 1 ч (3600 с) до порогового напряжения 10,8 В. Расчёт показывает, что при токе разряда в 255 А аккумулятор разрядится за 12,9 минут. Как видно 55 А*ч — это не ёмкость (электрическая ёмкость измеряется в Фарадах, 1 Ф= 1 Кл/В). Поэтому на аккумуляторе написано количество электричества Q, которое он выдаёт при определённом токе разряда и определённом времени его прохождения.[источник не указан 602 дня]
Плотность энергии
Плотность энергии — количество энергии на единицу объёма или единицу веса аккумулятора (см. ст. Плотность энергии).
Саморазряд
Саморазряд — это потеря аккумулятором заряда после полной зарядки при отсутствии нагрузки. Саморазряд проявляется по-разному у разных типов аккумуляторов, но всегда максимален в первые часы после заряда, а после — замедляется.
Для Ni-Cd аккумуляторов считают допустимым не более 10 % саморазряда за первые 24 часа после проведения зарядки. Для Ni-MH саморазряд чуть меньше. У Li-ion он пренебрежимо мал и значительно себя проявляет только в течение нескольких месяцев.
В свинцово-кислотных герметичных аккумуляторах саморазряд составляет около 40 % за 1 год хранения при 20°С, 15 % — при 5°С. Если температуры хранения более высокие, то саморазряд возрастает: батареи при 40°С теряют ёмкости 40 % всего за 4-5 месяцев.
Температурный режим
Следует беречь аккумуляторы от огня и воды, чрезмерного нагревания и охлаждения, резких перепадов температур.
Не следует использовать аккумуляторы при температурах выше +50°С и ниже −25°С. При эксплуатации аккумулятора в условиях «холодной зимы» рекомендуется его снимать и хранить в тёплом помещении. Нарушение температурного режима может привести к сокращению срока службы или потере работоспособности.
Тип аккумулятора
Тип аккумулятора определяется используемыми материалами. Различают следующие:
- Cn-Po — Графен-полимерный аккумулятор.
- La-Ft — лантан-фторидный аккумулятор
- Li-Ion — литий-ионный аккумулятор (3,2-4,2 V), общее обозначение для всех литиевых аккумуляторов
- Li-Co — литий-кобальтовый аккумулятор, (3,6 V), на базе LiCoO2, технология в процессе освоения
- Li-Po — литий-полимерный аккумулятор (3,7 V), полимер в качестве электролита
- Li-Ft — литий-фторный аккумулятор
- Li-Mn — литий-марганцевый аккумулятор (3,6 V) на базе LiMn2O4
- LiFeS — литий-железно-сульфидный аккумулятор (1,35 V)[источник не указан 201 день]
- LiFeP или LFP — Литий-железно-фосфатный аккумулятор (3,3 V) на базе LiFePO4
- LiFeYPO4 — литий-железо-иттрий-фосфатный (Добавка иттрия для улучшения свойств)
- Li-Ti — литий-титанатный аккумулятор (3,2 V) на базе Li4Ti5О12
- Li-Cl — литий-хлорный аккумулятор (3,99 V)
- Li-S — литий-серный аккумулятор (2,2 V)
- LMPo — литий-металл-полимерный аккумулятор
- Fe-air — железо-воздушный аккумулятор
- Na/NiCl — никель-солевой аккумулятор (2,58 V)
- Na-S — натрий-серный аккумулятор, (2 V), высокотемпературный аккумулятор
- Ni-Cd — никель-кадмиевый аккумулятор (1,2 V)
- Ni-Fe — железо-никелевый аккумулятор (1,2-1,9 V)
- Ni-H2 — никель-водородный аккумулятор (1,5 V)
- Ni-MH — никель-металл-гидридный аккумулятор (1,2 V)
- Ni-Zn — никель-цинковый аккумулятор (1,65 V)
- Pb — свинцово-кислотный аккумулятор (2 V)
- Pb-H — свинцово-водородный аккумулятор
- Ag-Zn — серебряно-цинковый аккумулятор (1,85 V)
- Ag-Cd — серебряно-кадмиевый аккумулятор (1,6 V)
- Zn-Br — цинк-бромный аккумулятор (1,8 V)
- Zn-air — цинк-воздушный аккумулятор
- Zn-Cl — цинк-хлорный аккумулятор
- RAM (Rechargeable Alkaline Manganese) — перезаряжаемая разновидность марганцево-цинкового щелочного гальванического элемента (1,5 V)[источник не указан 529 дней]
- Ванадиевый аккумулятор (1,41 V)[источник не указан 529 дней]
- Алюминиево-графитный аккумулятор (2 V)[источник не указан 529 дней]
- Алюминиево-ионный аккумулятор (2 V)[4]
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы:
| Тип | ЭДС (В) | Область применения |
|---|---|---|
| свинцово-кислотные Pb | 2,1 | троллейбусы, трамваи, воздушные суда, автомобили, мотоциклы, электропогрузчики, штабелеры, электротягачи, аварийное электроснабжение, источники бесперебойного питания |
| никель-кадмиевые Ni-Cd | 1,2 | замена стандартного гальванического элемента, строительные электроинструменты, троллейбусы, воздушные суда |
| никель-металл-гидридные Ni-MH | 1,2 | замена стандартного гальванического элемента, электромобили |
| литий-ионные Li‑ion | 3,7 | мобильные устройства, строительные электроинструменты, электромобили |
| литий-полимерные Li‑pol | 3,7 | мобильные устройства, электромобили |
| никель-цинковые Ni-Zn | 1,6 | замена стандартного гальванического элемента |
По мере исчерпания химической энергии напряжение и ток падают, аккумулятор перестаёт действовать. Зарядить аккумулятор (батарею аккумуляторов) можно от любого источника постоянного тока с бо́льшим напряжением при ограничении тока. Наиболее распространённым считается зарядный ток (в амперах), пропорциональный 1/10 условной номинальной ёмкости аккумулятора (в ампер⋅часах).
Однако, основываясь на техническом описании, распространяемом изготовителями широко применяемых электрических аккумуляторов (NiMH, NiCd), можно сделать предположение о том, что данный режим заряда, обычно именуемый стандартным, рассчитывается исходя из продолжительности восьмичасового рабочего дня, когда разряженный в конце рабочего дня аккумулятор подключается к сетевому зарядному устройству до начала нового рабочего дня. Применение такого режима заряда для этих типов аккумуляторов при систематическом использовании позволяет соблюсти качественно-стоимостной баланс эксплуатации изделия. Таким образом, с подачи изготовителя данный режим можно применять только для никель-кадмиевых и никель-металл-гидридных аккумуляторов.
Многие типы аккумуляторов имеют различные ограничения, которые необходимо учитывать при зарядке и последующей эксплуатации, например NiMH-аккумуляторы чувствительны к перезаряду, литиевые — к переразряду, напряжению и температуре. NiCd- и NiMH-аккумуляторы имеют так называемый эффект памяти, заключающийся в снижении ёмкости в случае, когда зарядка осуществляется при не полностью разряженном аккумуляторе. Также эти типы аккумуляторов обладают заметным саморазрядом, то есть они постепенно теряют заряд, не будучи подключенными к нагрузке. Для борьбы с этим эффектом может применяться капельная подзарядка.
В большинстве случаев возможность систематического использования аккумуляторов есть только в портативных устройствах радиосвязи и иной цифровой технике, где используются литий-ионные аккумуляторы и система контроля заряда-разряда встроена в устройство. В бюджетном сегменте «простые» никель-металл-гидридные и никель-кадмиевые аккумуляторы используются в качестве бюджетной замены щелочных элементов питания. В качестве источника тока для бюджетного аккумуляторного электроинструмента используются никель-кадмиевые аккумуляторы. Если в первом случае обычно есть возможность выбирать между бюджетным устройством «стандартного» заряда и зарядным устройством с контролем заряда (капельный заряд, импульсный заряд, ускоренный заряд с контролем напряжения и т. д.), то во втором случае изделие комплектуется, как правило, с трансформаторным источником питания для зарядки постоянным током, что при несоблюдении технических условий эксплуатации аккумулятора снижает срок его службы.
Форм-факторы
Внешний аккумулятор
Внешний аккумулятор (аккумуляторная батарея) — устройство для многократной подзарядки мобильного устройства (телефона, смартфона, планшетного компьютера) при отсутствии источника переменного тока (электросети).
Причиной появления этих устройств стало то, что при активном использовании современных смартфонов и планшетов заряда их аккумуляторов хватает на сравнительно короткое время — полдня или день. Для их зарядки в полевых условиях и были разработаны портативные аккумуляторы[5][6]. Типичный вес таких устройств — от нескольких сотен грамм, ёмкость от нескольких тысяч мА*ч до 10-20 А*ч[7]. С их помощью можно зарядить телефон 2-3 раза. Чаще всего они предоставляют для подключения порт USB. Некоторые из них имеют разъёмы или переходники для популярных разъёмов мобильных телефонов. Внешние аккумуляторы больших ёмкостей могут иметь переходники для зарядки ноутбуков. Иногда на внешних аккумуляторах имеется индикатор заряда или встроенный светодиодный фонарик.
Методы заряда аккумуляторов
Для заряда аккумуляторов применяется несколько методов. Как правило, метод заряда зависит от типа аккумулятора и обеспечивается зарядным устройством[8].
Медленный заряд постоянным током
Заряд постоянным током, пропорциональным 0.1-0.2 условной номинальной ёмкости Q в течение примерно 15-7 часов соответственно.
Самый длительный и безопасный метод заряда. Подходит для большинства типов аккумуляторов.
Быстрый заряд
Заряд постоянным током, пропорциональным 1/3 Q в течение примерно 3—5 часов.
Ускоренный или «дельта-V» заряд
Заряд с начальным током заряда, пропорциональным величине условной номинальной ёмкости аккумулятора, при котором постоянно измеряется напряжение аккумулятора и заряд заканчивается после того, как аккумулятор полностью заряжен. Время заряда — примерно час-полтора. Возможен разогрев аккумулятора и даже его разрушение.
Реверсивный заряд
Выполняется чередованием длинных импульсов заряда с короткими импульсами разряда. Реверсивный метод наиболее полезен для заряда NiCd и NiMH аккумуляторов, для которых характерен т. н. «эффект памяти».
См. также
Примечания
Литература
Ссылки
wiki.sc
Электрический аккумулятор Википедия
Зарядное устройство «Duracell», для заряжания как аккумуляторов типоразмеров AA и AAA (видны пружинные прижимы для них), так и аккумуляторные батареи типа «Крона». Во время зарядки горят индикаторыЭлектри́ческий аккумуля́тор — химический источник тока, источник ЭДС многоразового действия, основная специфика которого заключается в обратимости внутренних химических процессов, что обеспечивает его многократное циклическое использование (через заряд-разряд) для накопления энергии и автономного электропитания различных электротехнических устройств и оборудования, а также для обеспечения резервных источников энергии в медицине, производстве, транспорте и в других сферах.
Значение и употребление слова
Термин «аккумулятор» используется для обозначения отдельного элемента: например, аккумулятор, аккумуляторная банка, аккумуляторная ячейка. Но, разговорной речи на бытовом уровне может также применяться в отношении нескольких отдельных элементов, соединённых последовательно (для увеличения напряжения) или параллельно (для увеличения силы тока) друг с другом, то есть для обозначения аккумуляторной батареи.
История
Первый прообраз аккумулятора, который, в отличие от батареи Алессандро Вольты, можно было многократно заряжать, был создан в 1803 году Иоганном Вильгельмом Риттером. Его аккумуляторная батарея представляла собой столб из пятидесяти медных кружочков, между которыми было проложено влажное сукно. После пропускания через данное устройство тока от вольтова столба оно само начинало вести себя как источник электричества[1].
Принцип действия
Принцип действия аккумулятора основан на обратимости химической реакции. Работоспособность аккумулятора может быть восстановлена путём заряда, то есть пропусканием электрического тока в направлении, обратном направлению тока при разряде. Несколько аккумуляторов, объединённых в одну электрическую цепь, составляют аккумуля́торную батаре́ю.
Свинцово-кислотный аккумулятор
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в растворе серной кислоты.
Химическая реакция (слева направо — разряд, справа налево — заряд):
- Pb+SO42−−2e−⇆PbSO4{\displaystyle Pb+SO_{4}^{2-}-2e^{-}\leftrightarrows PbSO_{4}}
- PbO2+SO42−+4H++2e−⇆PbSO4+2h3O{\displaystyle PbO_{2}+SO_{4}^{2-}+4H^{+}+2e^{-}\leftrightarrows PbSO_{4}+2H_{2}O}
Литий-ионный аккумулятор
Литий-ионный аккумулятор состоит из электродов (катодного материала на алюминиевой фольге и анодного материала на медной фольге), разделённых пропитанными электролитом пористыми сепараторами. Переносчиком заряда в литий-ионном аккумуляторе является положительно заряженный ион лития, который внедряется (интеркалируется) в кристаллическую решетку других материалов (например, в графит, оксиды и соли металлов) с образованием химической связи (например: в графит с образованием LiC6, оксиды (LiMO2) и соли (LiMRON) металла).
Алюминий-ионный аккумулятор состоит из металлического алюминиевого анода, катода из графита в виде пены и жидкого ионного невоспламеняющегося электролита. Батарея работает по принципу электрохимического осаждения: происходит растворение алюминия на аноде, далее в среде жидкого электролита анионы хлоралюмината интеркалируют в графит. Количество возможных перезарядок батареи — более 7,5 тыс. циклов без потери мощности[2][3].
Характеристики
Ёмкость аккумулятора
За ёмкость аккумулятора чаще всего принимают количество электричества равное 1 Кл, при силе тока 1 А в течение 1 с, (при переводе времени в часы получаем 1 А*ч=3600 Кл). Однако принимают, а не измеряют. Существует распространенное заблуждение, что ёмкость аккумулятора измеряется в А*ч, это не совсем так, т. к. в 1 А*с=1 Кл или 1 А*ч=3600 Кл измеряется количество электричества или электрический заряд; по формуле Q= I*t, где Q -количество электричества или электрический заряд, I — сила тока, t — время протекания электрического тока. Например, обозначение «12 В на 55 А*ч» означает, что аккумулятор выдаёт количество электричества 198 кКл (кило Кулон) по какому-либо контуру, при токе разряда 55 А за 1 ч (3600 с) до порогового напряжения 10,8 В. Расчёт показывает, что при токе разряда в 255 А аккумулятор разрядится за 12,9 минут. Как видно 55 А*ч — это не ёмкость (электрическая ёмкость измеряется в Фарадах, 1 Ф= 1 Кл/В). Поэтому на аккумуляторе написано количество электричества Q, которое он выдаёт при определённом токе разряда и определённом времени его прохождения.[источник не указан 1033 дня]
Плотность энергии
Плотность энергии — количество энергии на единицу объёма или единицу веса аккумулятора (см. ст. Плотность энергии).
Саморазряд
Саморазряд — это потеря аккумулятором заряда после полной зарядки при отсутствии нагрузки. Саморазряд проявляется по-разному у разных типов аккумуляторов, но всегда максимален в первые часы после заряда, а после — замедляется.
Для Ni-Cd аккумуляторов считают допустимым не более 10 % саморазряда за первые 24 часа после проведения зарядки. Для Ni-MH саморазряд чуть меньше. У Li-ion он пренебрежимо мал и значительно себя проявляет только в течение нескольких месяцев.
В свинцово-кислотных герметичных аккумуляторах саморазряд составляет около 40 % за 1 год хранения при 20°С, 15 % — при 5°С. Если температуры хранения более высокие, то саморазряд возрастает: батареи при 40°С теряют ёмкости 40 % всего за 4-5 месяцев.
Температурный режим
Следует беречь аккумуляторы от огня и воды, чрезмерного нагревания и охлаждения, резких перепадов температур.
Не следует использовать аккумуляторы при температурах выше +50°С и ниже −25°С. При эксплуатации аккумулятора в условиях «холодной зимы» рекомендуется его снимать и хранить в тёплом помещении. Нарушение температурного режима может привести к сокращению срока службы или потере работоспособности.
Тип аккумулятора
Тип аккумулятора определяется используемыми материалами. Различают следующие:
- Cn-Po — Графен-полимерный аккумулятор.
- La-Ft — лантан-фторидный аккумулятор
- Li-Ion — литий-ионный аккумулятор (3,2-4,2 V), общее обозначение для всех литиевых аккумуляторов
- Li-Co — литий-кобальтовый аккумулятор, (3,6 V), на базе LiCoO2, технология в процессе освоения
- Li-Po — литий-полимерный аккумулятор (3,7 V), полимер в качестве электролита
- Li-Ft — литий-фторный аккумулятор
- Li-Mn — литий-марганцевый аккумулятор (3,6 V) на базе LiMn2O4
- LiFeS — литий-железно-сульфидный аккумулятор (1,35 V)[источник не указан 632 дня]
- LiFeP или LFP — Литий-железно-фосфатный аккумулятор (3,3 V) на базе LiFePO4
- LiFeYPO4 — литий-железо-иттрий-фосфатный (Добавка иттрия для улучшения свойств)
- Li-Ti — литий-титанатный аккумулятор (3,2 V) на базе Li4Ti5О12
- Li-Cl — литий-хлорный аккумулятор (3,99 V)
- Li-S — литий-серный аккумулятор (2,2 V)
- LMPo — литий-металл-полимерный аккумулятор
- Fe-air — железо-воздушный аккумулятор
- Na/NiCl — никель-солевой аккумулятор (2,58 V)
- Na-S — натрий-серный аккумулятор, (2 V), высокотемпературный аккумулятор
- Ni-Cd — никель-кадмиевый аккумулятор (1,2 V)
- Ni-Fe — железо-никелевый аккумулятор (1,2-1,9 V)
- Ni-H2 — никель-водородный аккумулятор (1,5 V)
- Ni-MH — никель-металл-гидридный аккумулятор (1,2 V)
- Ni-Zn — никель-цинковый аккумулятор (1,65 V)
- Pb — свинцово-кислотный аккумулятор (2 V)
- Pb-H — свинцово-водородный аккумулятор
- Ag-Zn — серебряно-цинковый аккумулятор (1,85 V)
- Ag-Cd — серебряно-кадмиевый аккумулятор (1,6 V)
- Zn-Br — цинк-бромный аккумулятор (1,8 V)
- Zn-air — цинк-воздушный аккумулятор
- Zn-Cl — цинк-хлорный аккумулятор
- RAM (Rechargeable Alkaline Manganese) — перезаряжаемая разновидность марганцево-цинкового щелочного гальванического элемента (1,5 V)[источник не указан 960 дней]
- Ванадиевый аккумулятор (1,41 V)[источник не указан 960 дней]
- Алюминиево-графитный аккумулятор (2 V)[источник не указан 960 дней]
- Алюминиево-ионный аккумулятор (2 V)[4]
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы:
| Тип | ЭДС (В) | Область применения |
|---|---|---|
| свинцово-кислотные Pb | 2,1 | троллейбусы, трамваи, воздушные суда, автомобили, мотоциклы, электропогрузчики, штабелеры, электротягачи, аварийное электроснабжение, источники бесперебойного питания |
| никель-кадмиевые Ni-Cd | 1,2 | замена стандартного гальванического элемента, строительные электроинструменты, троллейбусы, воздушные суда |
| никель-металл-гидридные Ni-MH | 1,2 | замена стандартного гальванического элемента, электромобили |
| литий-ионные Li‑ion | 3,7 | мобильные устройства, строительные электроинструменты, электромобили |
| литий-полимерные Li‑pol | 3,7 | мобильные устройства, электромобили |
| никель-цинковые Ni-Zn | 1,6 | замена стандартного гальванического элемента |
Форм-факторы
Литий-ионный аккумулятор форм-фактора 18650Внешний аккумулятор
Внешний аккумулятор (аккумуляторная батарея) (англ. power bank) — устройство для многократной подзарядки мобильного устройства (телефона, смартфона, планшетного компьютера) при отсутствии источника переменного тока (электросети).
Причиной появления этих устройств стало то, что при активном использовании современных смартфонов и планшетов заряда их аккумуляторов хватает на сравнительно короткое время — полдня или день. Для их зарядки в полевых условиях и были разработаны портативные аккумуляторы[5][6]. Типичный вес таких устройств — от нескольких сотен грамм, ёмкость от нескольких тысяч мА*ч до 10-20 А*ч[7]. С их помощью можно зарядить телефон 2-3 раза. Чаще всего они предоставляют для подключения порт USB. Некоторые из них имеют разъёмы или переходники для популярных разъёмов мобильных телефонов. Внешние аккумуляторы больших ёмкостей могут иметь переходники для зарядки ноутбуков. Иногда на внешних аккумуляторах имеется индикатор заряда или встроенный светодиодный фонарик.
Применение
В большинстве случаев возможность систематического использования аккумуляторов есть только в портативных устройствах радиосвязи и иной цифровой технике, где используются литий-ионные аккумуляторы и система контроля заряда-разряда встроена в устройство. В бюджетном сегменте «простые» никель-металл-гидридные и никель-кадмиевые аккумуляторы используются в качестве бюджетной замены щелочных элементов питания (батареек). В качестве источника тока для бюджетного аккумуляторного электроинструмента используются никель-кадмиевые аккумуляторы.
Если в первом случае обычно есть возможность выбирать между бюджетным устройством «стандартного» заряда и зарядным устройством с контролем заряда (капельный заряд, импульсный заряд, ускоренный заряд с контролем напряжения и т. д.), то во втором случае изделие комплектуется, как правило, с трансформаторным источником питания для зарядки постоянным током, что при несоблюдении технических условий эксплуатации аккумулятора снижает срок его службы.
Зарядка аккумуляторов
По мере исчерпания химической энергии напряжение и ток падают, аккумулятор перестаёт действовать. Зарядить аккумулятор (батарею аккумуляторов) можно от любого источника постоянного тока с бо́льшим напряжением при ограничении тока. Наиболее распространённым считается зарядный ток (в амперах), пропорциональный 1/10 условной номинальной ёмкости аккумулятора (в ампер⋅часах).
Однако, основываясь на техническом описании, распространяемом изготовителями широко применяемых электрических аккумуляторов (NiMH, NiCd), можно сделать предположение о том, что данный режим заряда, обычно именуемый стандартным, рассчитывается исходя из продолжительности восьмичасового рабочего дня, когда разряженный в конце рабочего дня аккумулятор подключается к сетевому зарядному устройству до начала нового рабочего дня. Применение такого режима заряда для этих типов аккумуляторов при систематическом использовании позволяет соблюсти качественно-стоимостной баланс эксплуатации изделия. Таким образом, с подачи изготовителя данный режим можно применять только для никель-кадмиевых и никель-металл-гидридных аккумуляторов.
Многие типы аккумуляторов имеют различные ограничения, которые необходимо учитывать при зарядке и последующей эксплуатации, например NiMH-аккумуляторы чувствительны к перезаряду, литиевые — к переразряду, напряжению и температуре. NiCd- и NiMH-аккумуляторы имеют так называемый эффект памяти, заключающийся в снижении ёмкости в случае, когда зарядка осуществляется при не полностью разряженном аккумуляторе. Также эти типы аккумуляторов обладают заметным саморазрядом, то есть они постепенно теряют заряд, не будучи подключенными к нагрузке. Для борьбы с этим эффектом может применяться капельная подзарядка.
Методы заряда аккумуляторов
Для заряда аккумуляторов применяется несколько методов; как правило, метод заряда зависит от типа аккумулятора[8].
- Медленный заряд постоянным током
Заряд постоянным током, пропорциональным 0,1-0,2 условной номинальной ёмкости Q в течение примерно 15-7 часов соответственно.
Самый длительный и безопасный метод заряда. Подходит для большинства типов аккумуляторов.
- Быстрый заряд
Заряд постоянным током, пропорциональным 1/3 Q в течение примерно 3—5 часов.
- Ускоренный или «дельта-V» заряд
Заряд с начальным током заряда, пропорциональным величине условной номинальной ёмкости аккумулятора, при котором постоянно измеряется напряжение аккумулятора и заряд заканчивается после того, как аккумулятор полностью заряжен. Время заряда — примерно час-полтора. Возможен разогрев аккумулятора и даже его разрушение.
- Реверсивный заряд
Выполняется чередованием длинных импульсов заряда с короткими импульсами разряда. Реверсивный метод наиболее полезен для заряда NiCd и NiMH аккумуляторов, для которых характерен т. н. «эффект памяти».
См. также
Примечания
Литература
wikiredia.ru
Основные типы аккумуляторов
Наиболее распространенные типы аккумуляторов – для бытовой техники, радиотелефонов, фотоаппаратов, фонариков, ИБП, их особенности и лучшие производители. |
Электрический аккумулятор – специальное устройство, накапливающее электроэнергию и обеспечивающее автономное питание оборудования. При его эксплуатации происходит переход одного вида энергии в другой, а также обратимость описанного процесса.
В большинстве случаев используется электрохимический метод. Среди названий электрического аккумулятора – вторичный химический источник тока, так как перед эксплуатацией требуется его зарядка.
Типы аккумуляторов
По типу аккумуляторы разделяют в зависимости от их химсостава, который влияет на их эксплуатационные свойства.
- никель-кадмиевые (Ni-Cd) – наиболее старый тип аккумуляторных батареек, отличается необходимостью соблюдения цикла «полный разряд» – «полный заряд» (имеют эффект памяти) и чувствительны к холоду (плохо отдают энергию на морозе), но могут хранится разраженными и отличаются низким саморазрядом, сейчас используются в основном в электроинструменте
- никель-металл-гидридные (Ni-MH) – очень распространенный тип простых и дешевых компактных аккумуляторных батареек, эффект памяти и чувствительность к холоду несколько ниже, чем у никель-кадмиевых аккумуляторов, но их нужно хранить заряженными и у них выше саморазряд, сейчас они используются в основном в радиотелефонах
- литий-ионные (Li-Ion) – более современный тип аккумуляторов, почти не подвержены эффекту памяти (снижению емкости), что позволяет заряжать их в любое время и необязательно разряжать до конца, чувствительность к холоду есть, но не критична, нужно поддерживать заряд при хранении, они часто используются в фотоаппаратах
- литий-полимерные (Li-Pol) – облегченный вариант литий-ионных аккумуляторов, обладающий теми же свойствами, но со значительно меньшим весом, что нашло применение в компактных мобильных устройствах и дронах
- свинцово-кислотные (SLA) – большие мощные аккумуляторы, способные быстро отдавать огромную энергию (силу тока), что используется в пусковых установках двигателей (стартерах) и источниках бесперебойного питания, требуют периодической подзарядки во время хранения
Также аккумуляторы отличаются напряжением в вольтах (В), емкостью в ампер-часах (Ач) или миллиампер-часах (мАч) и физическим размером (типоразмером).
Классификация аккумуляторов
Все аккумуляторы можно условно разделить по назначению на несколько основных групп:
- бытовые (аккумуляторные батарейки)
- для радиотелефонов
- для фонариков
- автомобильные
- для ИБП
- промышленные
Теперь рассмотрим их немного подробней, включая типоразмеры и лучших производителей.
Аккумуляторные батарейки
Для обеспечения нормального функционирования техники применяются аккумуляторы разных типоразмеров. Основная сфера их использования – питание мелких устройств бытового назначения.
Аккумуляторные батарейки используются для самых различных устройств – радио мышек, клавиатур, фотоаппаратов, простых фонариков, часов, другой мелкой электроники.
Они имеют различные типоразмеры:
- AA (пальчик) – наиболее распространенный формат круглых батареек длиной 5 см, напряжением 1.2 В и емкостью 1000-3000 мАч
- AAA (мини-пальчик) – также широко распространены, имеют длину 4.4 см, такое же напряжение 1.2 В, но меньшую емкость 500-1500 мАч
- крона – более редкая прямоугольная батарейка с напряжением 9 В, используется в некоторых электроприборах (например, мультиметрах)
Существуют и другие, более редкие форматы аккумуляторных батареек:
- CS (Sub C) – короткая круглая батарейка
- C (R14) – средняя круглая батарейка
- D (R20) – большая круглая батарейка
Они мало распространены и используются в некоторых специфических устройствах и старых фотоаппаратах.
К лучшим популярным производителям аккумуляторных батареек можно отнести Panasonic, Varta, Ansmann, Sanyo. Есть также много других именитых брендов, но их чаще подделывают.
Аккумуляторы для радиотелефонов
Это может быть монолитная аккумуляторная батарея либо отдельные элементы. Подобные устройства отличаются небольшим размером и незначительным весом. Аккумуляторы для радиотелефонов часто представляют собой удобные готовые сборки обычных Ni-MH аккумуляторных батареек.
Также в некоторых телефонах используются нестандартные фирменные аккумуляторы. Из производителей можно порекомендовать Panasonic и Robiton.
Аккумуляторы для фонариков
Аккумуляторы для фонарика представлены на рынке в широком ассортименте и выбор зависит от конкретной модели.
Наибольшей популярностью пользуются:
- АА (14500) – аккумуляторы для больших фонариков (длина 5 см, диаметр 1.4 см)
- ААА – обычные Ni-MH элементы с номинальным напряжением 1.2 В и емкостью 500-1100 мАч
- CR123A 16340– созданы для компактных фонариков (длина 3.4 см)
Есть также специальные аккумуляторы для мощных фонариков и электрошокеров.
Они имеют свои уникальные типоразмеры, которые нужно подбирать в зависимости от модели фонарика:
Эти аккумуляторы отличаются физическими размерами и емкостью. В основном они являются литий-полимерными, что делает их очень легкими. Из производителей хорошо зарекомендовали себя Panasonic, Robiton, Fenix.
Автомобильные аккумуляторы
Об автомобильных аккумуляторах мы особо рассказывать не будем, коснемся только отличий от всех других, которые нужно знать.
Это большие обслуживаемые кислотно-свинцовые батареи с жидким электролитом. Они способны быстро отдавать огромный ток, но необходимо следить за их зарядом и уровнем электролита (доливать по необходимости). Хранить свинцовый аккумулятор разряженным нельзя, так как где-то через полгода он выйдет из строя.
Аккумуляторы для ИБП
Аккумуляторы для компьютерных ИБП призваны обеспечить недлительное питание техники в случае временного отключения электричества. Они также являются свинцово-кислотными, но в отличие от автомобильных необслуживаемыми, а электролит в них загущенный в виде геля, что предотвращает утечки.
В остальном эти аккумуляторы подобны автомобильным, они могут быстро отдать большой ток и требуют периодической подзарядки. В разных ИБП используются аккумуляторы с разным напряжением (12 или 24 В), разной емкости (7, 9, 12 Ач) и разного физического размера. Также есть модели, в которые устанавливается несколько соединенных вместе батарей.
Выбирайте аккумулятор такого же напряжения и размера как в вашем ИБП, емкость при желании можно чуть больше (например, 9 Ач вместо 7 Ач) – это продлит работу ПК от ИБП. Из производителей можно порекомендовать SCB, Yuasa и Delta.
Аккумуляторы в ИБП для газового котла и другой ответственной техники, отличаются большей емкостью по сравнению с моделями, применяемыми при работе компьютерного оборудования. Ведь они рассчитаны на поддержание функционирования отопительных приборов на протяжении суток и более.
Такие аккумуляторы часто являются внешними и подключаются к ИБП с помощью специальных клемм, а сами ИБП должны выдавать напряжение в форме чистой синусоиды, что важно для электронасосов, используемых в системах отопления и другой чувствительной к форме напряжения техники.
Промышленные аккумуляторы
Обычно огромные батареи большой емкости. Могут быть разного напряжения, в том числе высоковольтные. Больше мы о них ничего говорить не будем, так как это не тематика нашего сайта.
Заключение
Для того, чтобы аккумулятор хорошо держал заряд и прослужил достаточно долго, он должен быть от надежного проверенного производителя и само собой оригинальным, а не дешевой подделкой. Также важно в каких условиях и как долго хранятся аккумуляторы.
Поэтому лучше всего приобретать аккумуляторы в специализированных магазинах, которые уделяют особое внимание их качеству. Качественные аккумуляторы для самых различных целей от лучших производителей можно приобрести на сайте https://voltacom.ru/catalog/power/akkum.
Зарядное устройство Xiaomi Mi Power Bank 2C 20000mAh
Зарядное устройство Xiaomi Mi Power Bank 2 10000mAh
Зарядное устройство Xiaomi Mi Power Bank 5000mAh
ironfriends.ru
Электрические аккумуляторы — это… Что такое Электрические аккумуляторы?
Русский академик Якоби впервые (в 1860 г.) применил для телеграфных целей принцип вторичных батарей, т. е. батарей, которые становятся источниками Э. энергии после того, как через них пропущен ток от другого источника тока. Гастон Планте воспользовался идеей Якоби и устроил вторичный элемент, состоящий из двух свинцовых пластинок, погруженных в воду, подкисленную серной кислотой. Такой элемент при соединении обеих пластинок металлическим проводником не дает тока, но если мы соединим пластинку А (фиг. 1), например, с положительным полюсом, а пластинку В с отрицательным полюсом некоторого источника тока и если от этого последнего начнет проходить ток через пластинки и жидкость данного элемента, то, выключив после некоторого времени источник тока и замкнув обе пластинки металлическим проводником, мы заметим, что этот элемент будет давать ток тем более продолжительный, чем больше будет сопротивление проводника, соединяющего обе пластинки, и чем дольше от данного источника пропускался через элемент ток.
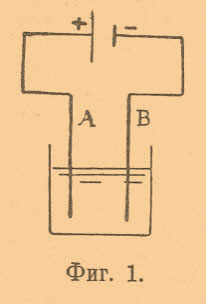
Элемент Планте назван вторичным элементом потому, что он становится источником тока только после того, как через него был пропущен ток от другого источника; аккумулятором же его назвали потому, что он как бы собирает, аккумулирует электрическую энергию от данного источника тока; действительно, если мы, пропустив через вторичный элемент ток от данного источника тока, выключим его и оставим на некоторое время, то, замкнув потом этот элемент, мы получим от него ток; следовательно, такой элемент способен сохранять полученную электрическую энергию более или менее продолжительное время. Однако элемент Планте может аккумулировать электрическую энергию в более или менее значительном количестве только после нескольких пропусканий через него тока и следующих за каждым пропусканием тока замыканий пластин металлическим проводником, т. е., как говорят, после нескольких взаимно чередующихся зарядов и разрядов элемента. Такой процесс последовательных взаимно чередующихся зарядов и разрядов называется формированием (формовкой) аккумулятора. При заряде аккумулятора электрическая энергия пропускаемого через элемент тока частью идет на нагревание жидкости (вода, подкисленная серной кислотой), частью на образование у одной пластинки перекиси свинца (PbO2), а у другой — свободно выделяющегося водорода; когда же элемент разряжается, то, как показали новейшие исследования, у обеих пластин получается сернокислый свинец. При второй зарядке (пропускание тока) на одной пластинке снова получается PbO2, а на другой — свинец Pb, при следующей разрядке снова получается у обеих пластин сернокислый свинец и т. д. В формированном элементе процесс аккумулирования Э. энергии можно объяснить следующим образом: по закону сохранения энергии произведенная данными силами работа идет на преобразование (превращение) энергии одного вида в другой: так, работа (см. Энергия), затраченная на подъем груза на некоторую высоту, идет на преобразование потенциальной энергии груза, находившегося на поверхности земли, в потенциальную энергию того же груза на данной высоте над землей; иначе говоря, затраченная работа пошла на увеличение потенциальной энергии данного груза. Точно так же и в аккумуляторах работа пропускаемого при заряде тока идет на увеличение потенциальной энергии химических соединений. Во время же разряда накопленная потенциальная химическая энергия переходит снова в Э. энергию, причем химические соединения у пластин переходят в тот же вид, как и до заряда. Пластинки А и В, соединяемые — первая с положительным полюсом, а вторая с отрицательным полюсом источника тока, называются электродами, причем А получает наименование положительного электрода, а В — отрицательного электрода. При заряде перекись свинца (PbO2) образуется у положительного электрода. Чем большее количество перекиси PbO2 выделится у электрода А, тем большей потенциальной энергией будет обладать данный аккумулятор, а следовательно, тем большую электрическую энергию он способен дать после разряда. Однако по мере того, как образуется слой перекиси, покрывающей свинец пластинки А, тем труднее будет идти образование новых слоев перекиси; таким образом, аккумулятор при данных его размерах может принять лишь определенный заряд и по истечении определенного промежутка времени дальнейшее пропускание через аккумулятор тока будет производить лишь разложение воды и нагревание жидкости. Ясно, что чем больше будет поверхность электродов, тем больше образуется перекиси PbO2 и тем, следовательно, больший заряд может воспринять данный аккумулятор. Вот почему в новейших конструкциях аккумуляторов типа Планте со свинцовыми электродами старались возможно больше развивать поверхность электродов. Необходимо, кроме того, чтобы образуемая перекись не отпадала от электрода, а держалась на этом последнем более или менее прочно, тем более, что при значительном разряде выделяемые у пластин газы, вырываясь наружу, стремятся оторвать частицы перекиси. Ввиду этого поверхности электродов придают такой вид и форму, чтобы, с одной стороны, выделяемые у электродов вещества удерживались прочно на их поверхности, а с другой стороны, выделяющиеся при разряде газы могли свободно циркулировать вдоль поверхности, не отрывая отложившихся продуктов. На фиг. 2 представлена пластинка аккумулятора акционерного общества в Гагена (Тюдор).
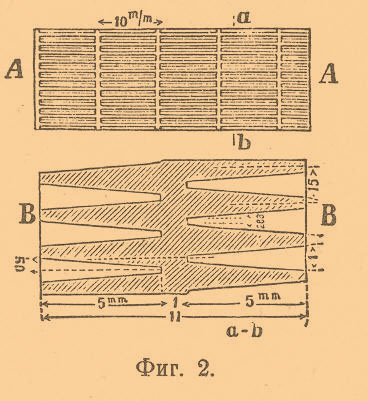
Ее поверхность АА изборождена желобками, глубина которых показана на чертеже под литерами ВВ, изображающем часть разреза пластинки АА по линии ab перпендикулярно к ее общей поверхности. На фиг. 3 представлена пластинка лондонской компании.
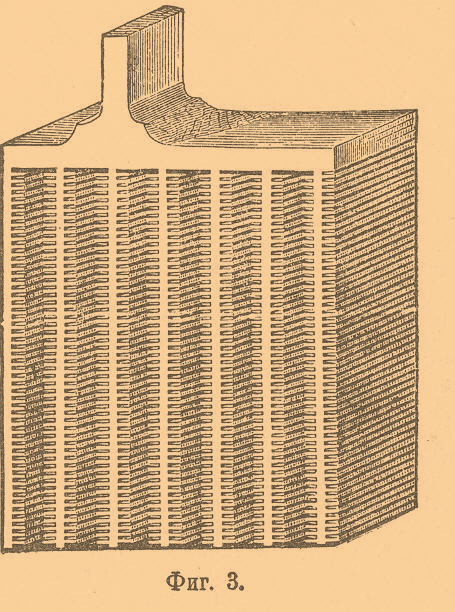
Поверхность электрода, как видно, развита до значительных пределов, а вместе с тем выделяющиеся газы могут свободно циркулировать, не повреждая накопляющейся в желобках перекиси свинца. Выше мы сказали, что аккумулятор типа Планте может накоплять Э. энергию в более или менее значительном количестве только после нескольких чередующихся между собой зарядов и разрядов. Это объясняется тем, что после последовательных зарядов и разрядов поверхности пластинок все глубже и глубже разрыхляются и тем дают возможность химическим реакциям, вызываемым действием пропускаемого через аккумулятор тока, проникать все глубже и глубже, и таким образом получаются все большие и большие массы перекиси свинца. Фор предложил для избежания долгой формовки приготовлять электроды в таком виде, при котором уже после нескольких зарядов и разрядов в аккумуляторе может образовываться значительное количество перекиси PbO2. С этой целью он приготовлял электроды — положительный из теста, представляющего смесь из сурика Pb3О4, и серной кислоты H2SO4, а отрицательный из смеси глета PbO и серной кислоты H2SO4. В применяемых в настоящее время системах аккумуляторов эти массы намазываются на свинцовые остовы, форма которых приспосабливается к возможно лучшему укреплению теста. Аккумуляторы типа Фора называются аккумуляторами с наносными массами. Наиболее распространенными аккумуляторами подобного типа являются аккумуляторы Тюдора, остов пластинок которых показан на фиг. 4, причем под литерой А показан вид пластинки со стороны ее поверхности, а под литерой В — вид сбоку; в желоба b, b…. вмазывается тестообразная масса.

На фиг. 5 показан решетчатый остов электродов аккумуляторов известной английской фирмы Electrical Power Storage Company; масса вмазывается в отверстия решетки.
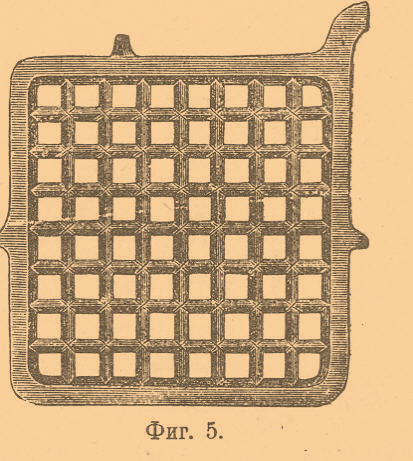
Зарядка, разряд и работа аккумуляторов. Во время заряда аккумулятора при накоплении в нем потенциальной энергии между его электродами развивается электродвижущая сила, противоположная электродвижущей силе (или напряжению) источника, от которого пропускается через аккумулятор ток, подобно тому, как при закручивании или сжатии пружины в этой последней развивается давление, противоположное внешнему усилию, действующему на пружину. Работа тока, идущая на преодоление этой противоположной его направлению электродвижущей силы, измеряет собой как раз ту энергию, которая накопляется в каждую единицу времени в аккумуляторе. Так, если электродвижущая сила, развиваемая аккумулятором, будет e, а сила проходящего через него тока i, то работа тока, идущая на накопление в каждую секунду энергии в аккумуляторе, будет: e·i. Но, кроме тока, работа, производимая зарядным током, затрачивается еще на нагревание в аккумуляторе вследствие того, что жидкость между его электродами представляет некоторое сопротивление. Пусть r — это сопротивление, тогда работа тока, расходуемая в секунду на нагревание в аккумуляторе, будет: ri2. Таким образом, в каждую секунду зарядным током в аккумуляторе будет затрачиваться работа: ei + ri2.
Пусть E напряжение, развиваемое у электродов А и В (фиг. 1) аккумулятора источником, заряжающим этот аккумулятор. Если i — сила зарядного тока, то работа, производимая упомянутым источником у электродов А и В, будет: Е·i; эта работа должна быть равна раньше вычисленной ei + ri2, а потому мы будем иметь:
Ei = ei + ri2,
откуда E = e + ri
i = (E — e)/r.
Отсюда мы видим, во-первых, что для того, чтобы через аккумулятор прошел ток, необходимо, чтобы развиваемое заряжающим источником напряжение E у электродов аккумулятора было больше, чем развиваемая этим аккумулятором электродвижущая сила, а во-вторых, чем больше будет E по отношению к e, тем больше будет и сила зарядного тока. Однако нельзя чрезмерно увеличивать силу этого последнего, ибо тогда чрезмерно будет нагреваться жидкость и часть тока пойдет просто на разложение воды, и следовательно, значительная доля Э. энергии заряда будет пропадать даром; вот почему соответственно размерам поверхности электродов определяются нормы зарядного тока и обыкновенно силу этого последнего относят на единицу поверхности электрода (положительного) и говорят, что на квадратный см сила зарядного тока должна быть столько-то ампер, иногда эту силу тока относят к единице веса электродов (положительного и отрицательного вместе). Чем большую силу тока можно допустить на 1 кг электродов, тем быстрее зарядится аккумулятор. Развиваемая аккумулятором при его заряде электродвижущая сила не остается все время постоянной: в начале она быстро растет до 1,8 вольт, затем медленно увеличивается до 2,1 или 2,15 вольт, после чего опять быстро поднимается до 2,5 вольт и, наконец, медленно возрастает до 2,6 или 2,7 вольт; когда электродвижущая сила аккумулятора достигла этого значения, то заряд можно считать оконченным, после этого аккумулятор, как говорят, начинает кипеть: в нем начинается сильное выделение газов, происходящих от разложения воды. Аккумуляторы заряжают током от динамо-машины; при этом необходимо наблюдать, чтобы напряжение динамо-машины было все время больше, чем развиваемая аккумуляторами электродвижущая сила, иначе может случиться, что к концу заряда ток от аккумуляторов пойдет обратно в эту последнюю и сожжет ее обмотки. Так, если мы хотим зарядить батарею аккумуляторов в 10 элементов, соединенных последовательно, и возьмем динамо-машину, развивающую 22 вольт, то сначала ток будет идти от динамо в аккумуляторы до тех пор, пока электродвижущая сила каждого элемента не дойдет до 2,15 вольт (см. выше), а следовательно, для 10 элементов до 21,5 вольта; после этого электродвижущая сила аккумуляторов сразу поднимется до 2,5 x 10 = 25 вольт, и тогда ток пойдет уже не от динамо, а обратно, от аккумуляторов к динамо, и если эта последняя будет динамо с последовательным возбуждением (см. Динамо-машины), то этот ток, проходя через обмотки электромагнитов в обратном направлении, размагнитит ее, затем в зависимости от его силы сожжет все обмотки. Применяя шунтовую динамо-машину, нет опасения в размагничиваний, но возможны также случаи перегорания обмоток. Ввиду этого для зарядки аккумуляторов, во-первых, применяют преимущественно шунтовые динамо-машины, а во-вторых, между динамо и аккумуляторами вставляют автоматический прерыватель тока, размыкающий цепь в том случае, когда ток, направляющий от динамо к аккумуляторам станет равным нулю, ибо после этого момента, если цепь не прервана, может пойти ток обратного направления. При разряде электродвижущая сила аккумулятора также не остается постоянной, а уменьшается по мере истощения разряда; в первый же момент, когда элемент замкнут на рабочую цепь, электродвижущая сила быстро падает до 2,2 вольт, затем немного медленнее уменьшается до 2,05 вольта, далее весьма медленно понижается до 1,6 вольт, после чего уже быстро убывает почти до нуля; вот почему практически разрядку приостанавливают, когда электродвижущая сила дошла до 1,8 вольт. Предположим, что данная батарея аккумуляторов давала до конца практического разряда на данную цепь (например на цепь лампочек) в течение t часов силу тока i, причем электродвижущая сила батареи в среднем была е. Пусть e’ электродвижущая сила (или напряжение) у внешних зажимов батареи, т. е. у мест, где берет начало от крайних электродов данная рабочая цепь; предположим, что внутреннее сопротивление батареи равно r (сопротивление всей жидкости и соединительных частей между двумя крайними электродами). Энергия, вырабатываемая в секунду батареей, будет ei, энергия, расходуемая в рабочей цепи — e’i, а энергия, расходуемая на нагревание в батарее, — ri2; таким образом, мы будем иметь:
ei = e’i + ri2,
откуда е = е’ + ri,
или е’ = е — ri.
Это показывает, что напряжение у внешних зажимов батареи равно полной ее электродвижущей силе минус падение вольт внутри батареи. За время t часов батарея разовьет энергию ei∙t, полезная энергия, которая получится в цепи, будет e’i∙t. Если е, е’ выражены в вольтах, i в амперах, то произведения ei∙e’i будут выражать ватты, a eit и e’it — ватт-часы (при условии, что время t выражено в часах). Таким образом, e’it представляет собой количество полезных ватт-часов, которое может дать батарея при разряде. Эта величина называется полезной емкостью батареи по энергии, произведение же i’t, число ампер-часов, называется полезной емкостью по количеству или полезной емкостью в ампер-часах. Если при разряде от батареи брали сначала ток i1 в течение времени t1 часов, а затем до конца разряда ток i2 в течение времени t2, то полезная емкость по энергии будет: e’i1t1 + e’i2t2, а в ампер-часах: i1t1 + i2t2.
Предположим, что для зарядки батареи потребовалось Т часов, причем зарядный ток был все время I, а напряжение, которое необходимо было развивать от данного источника (например, динамо-машины) у зажимов внешних электродов батареи, было в среднем E; тогда энергия, которую сообщили батарее при ее заряде, будет в ватт-часах EI∙T, число же ампер-часов, сообщенных при заряде, будет I∙T. Если бы зарядка происходила при разных токах, например в течение времени Т1 шел ток I1, в течение времени T2 — ток I2 и до окончания заряда, в течение времени Т3, ток I3, то энергия, сообщенная батареей в ватт-часах, будет: EI1Т1 — EI2Т + EI3Т3, а число ампер-часов: I1Т1 — I2Т2 + I3Т3. Предположим, что для полной зарядки батареи необходимо было сообщить всего W ватт-часов, а получили от нее при разряде до практического истощения (т. е. когда электродвижущая сила каждого элемента дошла до 1,8 вольт) W’ ватт-часов. Отношение W’/W называется отдачей, или коэф. полезного действия по энергии. Если для зарядки потребовалось всего Н ампер-часов, а получили мы от батареи всего Н’ ампер-часов, то отдача по количеству или по ампер-часам выразится отношением Н’/Н. Отдача по энергии применяемых на практике свинцовых аккумуляторов колеблется от 70 до 75 %, а отдача по количеству — от 80 до 85 и редко до 90 %. Полезную емкость, как по энергии, так и по количеству, часто относят к единице веса электродов батареи, и такая емкость называется удельной емкостью. Так, если полезная емкость по энергии данной батареи равна W ватт-часов, а вес всех пластин (электродов) равен Р килограммов, то удельная емкость по энергии будет W1 =W/P; точно так же удельная емкость в ампер-часах (по количеству) будет: H1 = H/P, где H полезная емкость батареи в ампер-часах. Для переносных целей, для автомобилей, электрических трамваев и т. п. удельная емкость должна быть возможно больше. Приведем теперь некоторые практические данные. Каждый элемент может состоять из нескольких пластин (электродов). Положительные электроды соединяются вместе параллельно; то же делают и с отрицательными электродами, причем эти последние вставляются в промежутки, образуемые положительными электродами. Общая полоса, соединяющая положительные электроды, представит собой положительный полюс элемента, а такая же полоса, соединяющая отрицательные электроды, представит отрицательный полюс. Собранные таким образом группы электродов вставляются в стеклянный или обитый свинцом деревянный сосуд, но так, чтобы пластинки не касались дна и чтобы не было металлического соединения между положительными и отрицательными электродами. На фиг. 6 показан один из таких элементов в собранном виде, в стеклянном сосуде.

Отростки А, А’ полос, соединяющих положительные и отрицательные электроды, служат для присоединения проводов внешней цепи. Элементы аккумуляторов, подобно гальваническим элементам, можно соединять последовательно и параллельно (на фиг. 7 схематически показано последовательное соединение трех элементов, состоящих каждый из 5-ти положительных электродов и 4 отрицательных).
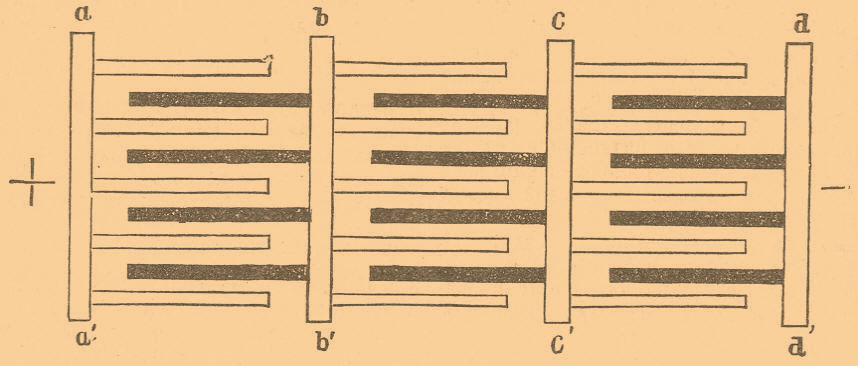
Как видно, отрицательная электродная полоса bb’ первого элемента соединена с положительными электродами 2-го элемента и т. д.
Элементный коммутатор. Мы уже показали выше, что при разрядке аккумуляторов Э.-движ. сила уменьшается: вначале ее можно считать равной 2,2 вольта (ибо в первый же момент она падает до этого значения), а в конце — 1,8 вольт. Если, следовательно, нам необходимо поддерживать во время разряда в данной цепи постоянное напряжение, например, 100 вольта, то необходимо, чтобы вначале было всего элементов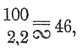 , а в конце разряда
, а в конце разряда 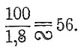 . Отсюда ясно, что аккумуляторы необходимо включать в данную цепь при посредстве такого коммутатора, который давал бы возможность постепенно (по мере того, как Э.-движ. сила падает) включать добавочные элементы, начиная от 46 до 56. Принцип такого коммутатора изображен на схеме фиг. 8.
. Отсюда ясно, что аккумуляторы необходимо включать в данную цепь при посредстве такого коммутатора, который давал бы возможность постепенно (по мере того, как Э.-движ. сила падает) включать добавочные элементы, начиная от 46 до 56. Принцип такого коммутатора изображен на схеме фиг. 8. 
Переставляя рукоятку В, можно вводить в данную цепь АА’ от 46 по 56 элементов. Для того, чтобы при передвижении ручки не было перерыва в цепи, пластинки коммутатора отделяют промежутками меньшими, чем ширина ручки В. Но в таком случае всегда будет момент, когда ручка В замкнет тот или другой элемент на короткое, например, когда рукоятка В будет лежать одновременно на двух смежных пластинках коммутатора. Для устранения такого короткого замыкания устраивают промежуточные пластинки а’ b’ с’… (фиг. 9), соединенные с пластинками a, b, с… сопротивлениями x.
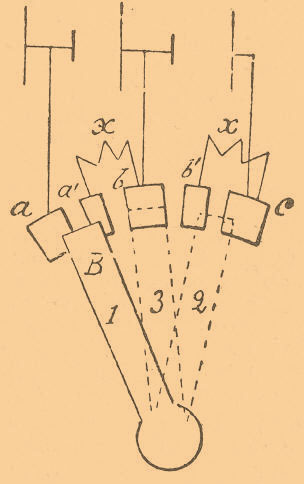
При таком приспособлении во время перехода рукоятки В от одного контакта к другому соответствующие элементы будут замыкаться через эти сопротивления x, как это видно на чертеже в положении 1 ручки В. В положении 2, когда ручка В касается одновременно пластинки с и добавочной пластинки b’, сопротивление x замкнуто на короткое ручкой же В и, следовательно, ток от аккумуляторов пройдет прямо от пластинки с через рукоятку В, минуя сопротивление x. То же самое будет при всех аналогичных положениях рычага В, т. е. при положениях, когда этот последний будет одновременно лежать на главной и вспомогательной пластинках, соединенных между собой сопротивлением x. Положение 3 соответствует нормальному положению рычага В. Вместо того, чтобы включать сопротивления x между пластинками a’b, b’c и т. д., делают ручку В из двух изолированных одна от другой частей, между которыми и включают сопротивление x (фиг. 10).
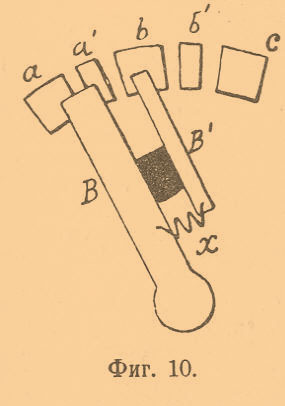
При зарядке, когда Э.-движущая сила батареи аккумуляторов возрастает, можно при посредстве элементного коммутатора выключать последовательно элементы один за другим. На больших установках батареи аккумуляторов применяют большею частью для параллельной работы с динамо-машинами с целью уравнять нагрузку этих последних: в часы наименьшей нагрузки в данной сети (например в осветительной сети), когда требуется небольшой ток, динамо-машина избыток энергии посылает в аккумуляторы, заряжая эти последние, а в часы наибольшей энергии батарея аккумуляторов вместе с динамо-машиной дает ток в данную сеть. Это дает возможность применять динамо-машины мощности меньшей, чем того требует данная установка, и, кроме того, динамо будет работать все время равномерно. Поясним это примером. Предположим, что у нас имеется установка на 200 ламп, требующих каждая по 50 ватт. Когда все лампы будут гореть, то необходимо давать энергию 50 x 200 = 10000 ватт и пришлось бы иметь динамо мощностью на 10000 ватт. Но допустим, что в определенные часы всего будет гореть только 50 ламп, тогда потребуется мощность только 50 x 50 = 2500 ватт; таким образом, динамо-машина будет работать всего только на 1/4 полной ее мощности. Возьмем динамо не на 10000, а только на 5000 ватт и присоединим к ней батарею, которая могла бы давать остальные 5000 ватт. В то время, когда будут гореть только 50 ламп, динамо-машина будет давать в цепь 2500 ватт, остальные же 2500 ватт пойдут на зарядку батареи; когда же в цепи зажгут, напр., 150 ламп, динамо-машина будет давать в цепь 5000 ватт, а остальные 2500 ватт (ибо всего нужно при 150 лампах 7500 ватт) будет давать батарея. Точно так же при 200 лампах динамо будет давать 5000 ватт, а остальные 5000 ватт добавит батарея. Отсюда видно, что, применяя батарею для данной установки на 200 ламп, можно взять динамо-машину только на 5000 ватт (вместо 10000) и, кроме того, эта динамо будет работать все время на одинаковую нагрузку, т. е. равномерно, что гораздо выгоднее как для работы динамо-машины, так и приводящей ее в движение паровой машины. На фиг. 11 приведена схема параллельного включения динамо-машины и батареи аккумуляторов.
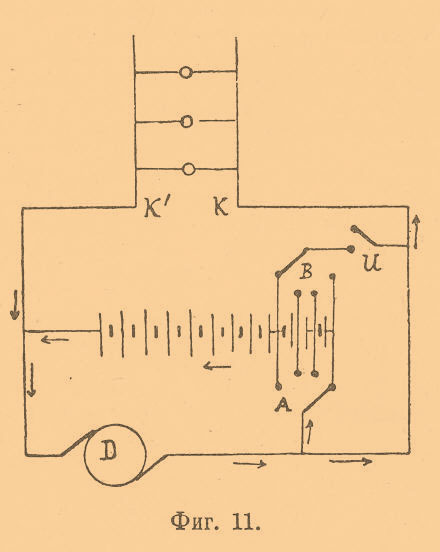
Элементный коммутатор А служит для зарядки батареи от динамо-машины, а коммутатор В для разрядки в цепь kk’. Когда рукоятка переключателя и поставлена на контакт а, то батарея и динамо-машина работают совместно на цепь kk’, при положении же рукоятки на контакте b, динамо-машина дает ток в сеть и заряжает батарею, а эта последняя отделена от сети kk’. Кроме свинцовых аккумуляторов, были сделаны попытки применять и другие вторичные элементы. Так, были предложены медно-цинковые элементы, в которых одним из электродов является цинк, другим — окись меди, жидкостью же служит раствор едкого кали. Эти аккумуляторы оказались малопригодными вследствие быстрой их порчи и вследствие сравнительно низкой электродвижущей силы (0,9 вольта на элемент). В последнее время Эдисон привлек внимание ученого и технического мира изобретением нового аккумулятора, состоящего из окиси никеля (положительный электрод) и порошкообразного железа (отрицательный электрод), причем жидкостью (электролитом) служит раствор едкого кали. Вот некоторые данные относительно этого аккумулятора: электродвижущая сила в конце заряда 1,5 вольта, средняя электродвижущая сила при разряде 1,1 вольта, удельная емкость по энергии 30,85 ватт-часов на килограмм, что является значительной удельной емкостью по сравнению со свинцовыми аккумуляторами. Однако до сих пор еще нет положительных данных о практических результатах испытаний этих аккумуляторов. Ср. Грюнвальд, «Устройство и употребление электрических аккумуляторов»; Норре, «Die Akkumulatoren für Elektricitat»; Shop, «Handbuch der elektrischen Akkumulatoren»; Sieg, «Die Akkumulatoren»; Zacharias, «Die Akkumulatoren»; Loppé, «Les accumulateurs électriques».
П. Войнаровский.
dic.academic.ru
Аккумуляторные батареи. Виды и устройство. Применение
АКБ или аккумуляторные батареи – это оборудование, которое состоит из нескольких аккумуляторов. Оно может накапливать, хранить и расходовать энергию. Благодаря обратимости химических процессов, происходящих внутри аккумулятора, такие устройства могут заряжаться и разряжаться многократно.
Сфера применения аккумуляторов весьма обширна. Они применяются в автомобилях и различной бытовой технике, например, в пультах ДУ и ноутбуках. Но также и в качестве резервных источников питания в медицинской сфере, производстве, космической отрасли, дата-центрах.
Виды и типы АКБ
Сегодня производят около 30 типов аккумуляторов. Такое большое количество обуславливается возможностью применять в качестве электродов и электролитов различные химические элементы. Именно от материала электрода и состава электролита зависят все характеристики аккумулятора.
Мы не будем приводить все типы, а лишь дадим небольшую таблицу с описанием наиболее распространенных:
Устройство
1 — Отрицательный электрод
2 — Разделительный слой
3 — Положительные электроды
4 — Отрицательный контакт
5 — Предохранительный клапан
6 — Положительные электроды
7 — Положительный контакт
Аккумуляторные батареи состоят из нескольких банок аккумуляторов, соединенных либо параллельно, либо последовательно. Последовательное соединение применяют в целях увеличения напряжения, а параллельное для увеличения силы тока.
Каждый из отдельно взятого аккумулятора в АКБ состоит из двух электродов и электролита, помещенных в корпус из специального материала.
Электрод с отрицательным зарядом – анод, с положительным зарядом – катод. Анод содержит восстановитель, катод – окислитель. Внутри корпуса аккумулятора стоит разделительная пластина, которая не позволяет электродам замыкаться.
Электролит – водный раствор, в который погружены оба электрода.
При разрядке аккумулятора восстановитель анода начинает окисляться и выделяются электроны. Электроны затем попадают в электролит и оттуда движутся к катоду, при этом создавая разрядный ток. Попадая в катод электроны восстанавливают его окислитель. Простыми словами можно описать процесс так: электроны идут от отрицательного электрода к положительному и создают разрядный ток.
При зарядке аккумулятора электроды меняются своим химическим составом и происходит обратная реакция. Электроны здесь двигаются от положительного анода к отрицательному катоду.
Особенности разных типов АКБ
Свинцово-кислотные аккумуляторы
Разработан Гастоном Планте в 19 веке. Эти аккумуляторные батареи сегодня наиболее актуальны благодаря дешевизне и универсальности. Сфера их применения обширна ввиду большого количества разновидностей этого типа. В качестве отрицательно заряженных электродов здесь используется оксид свинца. Положительные электроды выполняются из свинца. Электролит – серная кислота.
У свинцовых-кислотных батарей есть следующие разновидности:
- LA – аккумуляторы с напряжением 6 или 12 Вольт. Традиционное устройство для осуществления запуска двигателей автомобилей. Требуют постоянного обслуживания и вентиляции.
- VRLA – напряжением 2, 4, 6 или 12 Вольт. Клапанно-регулируемая свинцово-кислотная аккумуляторная батарея. Как видно из названия этот АКБ укомплектован разгрузочным клапаном. Его роль – минимизировать выделение газа и расход воды. Такие батареи можно устанавливать в жилых помещениях.
- AGM VRLA – как и предыдущий тип оснащен клапаном, но имеет совсем другие свойства. В аккумуляторах, сделанных по технологии AGM роль сепаратора играет стекловолокно. Его микропоры пропитаны жидким электролитом. Такие АКБ не требуют обслуживания и устойчивы к вибрациям.
- GEL VRLA – подвид свинцово-кислотных аккумуляторов с гелеобразным электролитом. Благодаря этому увеличен их ресурс заряда/разряда. Не требуют обслуживания.
- OPzV – герметичные аккумуляторы используемые в области телекоммуникации и для аварийного освещения. Электролит, как и в предыдущем случае гелевый. В электродах содержится кальций, благодаря которому срок службы такого типа батарей – 20 лет.
- OPzS – катод таких аккумуляторов имеет трубчатую структуру. Это существенно повышает циклический ресурс этого типа батарей. Служит также около 20 лет. Выпускается в виде АКБ с напряжением от 2 до 125 В.
Литий-ионные аккумуляторы
Был впервые выпущен Sony в 1991 году и с тех пор активно применяется в бытовой технике, электронных устройствах. Практически все мобильные телефоны, ноутбуки, фотоаппараты и видеокамеры оснащены таким видом батарей. Роль катода здесь играет литий-ферро-фосфатная пластина. Отрицательный анод – каменноугольный кокс. Положительный ион лития переносит заряд в таких батареях. Он может проникать в кристаллическую решетку других материй и образовывать с ними химическую связь. Преимуществом этого типа является высокая энергоемкость, низкий саморазряд и отсутствие нужды в обслуживании.
Литий-ионные аккумуляторные батареи также, как и их свинцовые аналоги имеют большое количество подтипов. В данном случае подтипы отличаются между собой составом катода и анода. Напряжение литий-ионных аккумуляторов варьируется в пределах от 2,4 до 3,7 В.
Одним из самых известных подтипов является литий-полимерные аккумуляторные батареи. Они появились сравнительно недавно и быстро завоевал популярность. Она обусловлена тем, что в литий-полимерных батареях используется твердый полимерный электролит. Это позволяет создавать батареи любой формы. При этом стоимость этих батарей всего лишь на 15% выше обычных литий-ионных.
Похожие темы:
electrosam.ru
