Что доливать в аккумулятор? | АКБ-сервис
Во время заряда и работы все аккумуляторные батареи теряют часть воды из электролита. При этом снижается уровень электролита над пластинами и увеличивается концентрация кислоты в электролите (плотность электролита). Если батарея эксплуатируется с низким уровнем электролита, это отрицательно влияет на ресурс батареи.
Скорость потери воды главным образом зависит от применяемых для производства аккумуляторной батареи материалов и от состояния электрооборудования.
Для восстановления уровня электролита доливайте в аккумулятор только дистиллированную или деионизированную воду. Своевременная доливка воды в батарею с пробками позволяет снизить негативное влияние высокой плотности электролита на ее последующий ресурс.
Уровень электролита должен быть на 10–15 мм выше верхней кромки сепараторов и не подниматься выше нижнего края заливной горловины.
Если точно установлено, что причиной низкого уровня является выплескивание, то доливайте электролит той же плотности и при той же температуре, что и оставшийся в батарее.
Если уровень электролита выше нормы, то откачайте электролит резиновой грушей с эбонитовым наконечником.
Чтобы не получить неправильных результатов, не замеряйте плотность электролита:
– если его уровень не соответствует норме;
– если электролит слишком горячий или холодный; оптимальная температура при измерении плотности +15+27° С;
– после доливки дистиллированной воды. Следует аккумулятор поставить на зарядку и подождать, пока электролит перемешается.
– после нескольких включений стартера. Надо подождать, чтобы установилась равномерная плотность электролита в элементе батареи;
При использовании технической серной кислоты или не дистиллированной воды, ускоряются саморазряд аккумуляторной батареи, происходит сульфатация, разрушение пластин и уменьшение ёмкости аккумуляторной батареи.
После долива воды лучше еще немного подзарядить аккумулятор для перемешивания электролита.
При сильном морозе (если Вы добавили воду после поездки) даже возможно замерзание верхнего слоя электролита. Зимой воду нужно добавлять перед поездкой, но тщательнее контролировать уровень, чтобы не переборщить.
Что нельзя делать с аккумулятором летом, чтобы он не «умер» зимой
Когда ваш автомобильный аккумулятор подводит и машина не заводится, это крайне неприятно. Между тем нередко виноват сам водитель, не выполнявший ряд простых правил. Разберемся, какие именно ошибки могут сократить жизнь АКБ даже летом.
Как можно убить аккумулятор быстрее всего
Самый простой путь вывести из строя аккумулятор — это долить в электролит обычную воду — электроды в таком случае выйдут из строя.
Жизнь АКБ может радикально сократить также заряд током чрезмерно большой силы, перегрев электролита и его повышенная плотность, повышенное и пониженное напряжение в бортовой сети автомобиля, загрязнение электролита и короткое замыкание (возможно при неосторожном обращении с инструментом вблизи контактов батареи, или при повреждения изоляции силового кабеля). Однако существуют и менее явные огрехи, которые также вредны для АКБ. Читайте о них ниже.
Не поддерживать чистоту
При эксплуатации автомобиля в особенности в условиях повышенной загрязненности (пыль, песок, пыльца деревьев и т.п.) следует уделять особое внимание чистоте корпуса АКБ. Ведь если грязь просочится в электролит, печальная судьба батареи по сути предрешена.
Загрязнения на корпусе следует регулярно устранять мягкой тряпкой, смоченной в растворе нашатырного спирта или кальцинированной соды.
Используйте зубную щетку или мелкую шкурку, чтобы удалить любые следы коррозии, если вы обнаружите их на клеммах аккумулятора. Лишняя грязь и следы окисления на клеммах провоцируют замыкание и разрядку АКБ. Не забывайте также проверять надежность крепления как самого аккумулятора, так и его клемм.
Игнорировать температурный режим
Не секрет, что аккумуляторы постепенно подсаживаются от скачков температуры в межсезонье и долгого отсутствия нагрузки. При падении плотности электролит замерзает — это вызывая деформации и осыпание пластин, равно как прожоги от коротких замыканий. Поэтому не следует оставлять ваш автомобиль на недели и месяцы на улице в мороз.
При падении плотности электролит замерзает — это вызывая деформации и осыпание пластин, равно как прожоги от коротких замыканий. Поэтому не следует оставлять ваш автомобиль на недели и месяцы на улице в мороз.
Регулярно заводите ваш автомобиль зимой, а еще лучше — совершайте хотя бы короткие поездки, чтобы батарея могла подзарядиться. Гаражное хранение — идеальный вариант, но даже в этом случае следует замерять тестером уровень заряда АКБ на заглушенном двигателе хотя бы раз в месяц. При полном заряде показания стремятся к значению 12.7 вольт. При почти полной разрядке будет примерно 12 вольт. При нормальной плотности электролита, которая должно составлять 1,27 г/см куб., образование льда начнется только при температуре ниже -65 град.
Перегружать батарею
Прежде всего, не перегружайте сеть. Различные усилители, доп.оборудование и девайсы типа видеорегистратора, радар-детектора и просто несколько подключенных к «мультимедийке» гаджетов — это, конечно, замечательно. Но такая прорва потребителей неизбежно повысит нагрузку на сеть.
Нередки также случаи запредельных разрядов, например, после пуска двигателя стартером. Или, скажем, если вы регулярно даете «прикурить» друзьям и соседям (особенно если потенциал их АКБ больше, чем у вашего), это также не идет на пользу батарее. Кроме того, помогая такому аккумулятору, который уже «дышит на ладан», донор может еще и спалить бортовую электронику.
Неправильное обслуживание
Если ваш аккумулятор обслуживаемый, то в рамках самостоятельного «ТО» следует долить нужное количество смести дистиллированной воды и электролита (у автомобильных аккумуляторов принято считать нормальным уровень заливки на 10-15 мм выше верхней кромки пластин) и убедиться в том что раствор имеют оптимальную плотность (1.27 г/см3).
Если в АКБ пониженная плотность смеси, то это может привести к быстрому разряду и замерзанию раствора. Если плотность повышенная — тоже плохо: чревато «обезвоживанием», и, как следствие, разъеданием пластин. Плотность состава измеряется специальным прибором — ареометром (денсиметром).
Плотность состава измеряется специальным прибором — ареометром (денсиметром).
Совет «подснежникам» — отнесите аккумулятор домой зимой
Есть категория водителей, которые по тем или иным причинам не ездят зимой. Для таких людей имеет прямой смысл позаботится об аккумуляторе. АКБ необходимо снять и отнести домой или в теплый гараж. Хранить батарею рекомендуется при комнатной температуре. При этом каждые два — три месяца аккумулятор рекомендуется подзаряжать, предварительно проверяя уровень зарядки с помощью вольтметра.
сколько доливать, если его стало мало
Аккумуляторная батарея (АКБ) в автомобиле используется в качестве дополнительного источника электроэнергии. С помощью неё производится запуск двигателя, и при включённом зажигании осуществляется работа всех бортовых приборов. Зачастую многие водители совершают большую ошибку, когда думают, что можно долить электролит в аккумулятор при его понижении, ведь, возможно, причина кроется в обычном испарении воды.
Дистиллированная вода или электролит
Если самостоятельно изучить техническую литературу, то можно без особого труда понять, что во время работы аккумулятора из него испаряется некая часть жидкости, благодаря чему снижается уровень электролита над пластинами, а плотность кислоты в несколько раз увеличивается.
Поэтому можно сделать вывод, что недостаточный уровень электролита в батарее при её ежедневной эксплуатации оказывает значительное влияние на состояние пластин и скоропостижно снижает срок годности. Только при постоянной поддержке необходимого уровня кислоты уменьшается негативное действие повышенной плотности на аккумуляторную батарею.
Многие опытные механики знают о том, когда можно добавить электролит в аккумулятор, но чаще всего они заливают туда дистиллированную воду, ведь кислота не имеет свойства испаряться при кипении, поэтому из аккумулятора выходит наружу лишь кислород с водородом.
Важно помнить о том, что если в аккумуляторе мало электролита из-за его потери, например, разлился при открытых крышках, то именно в этом случае можно смело заливать его в горловины.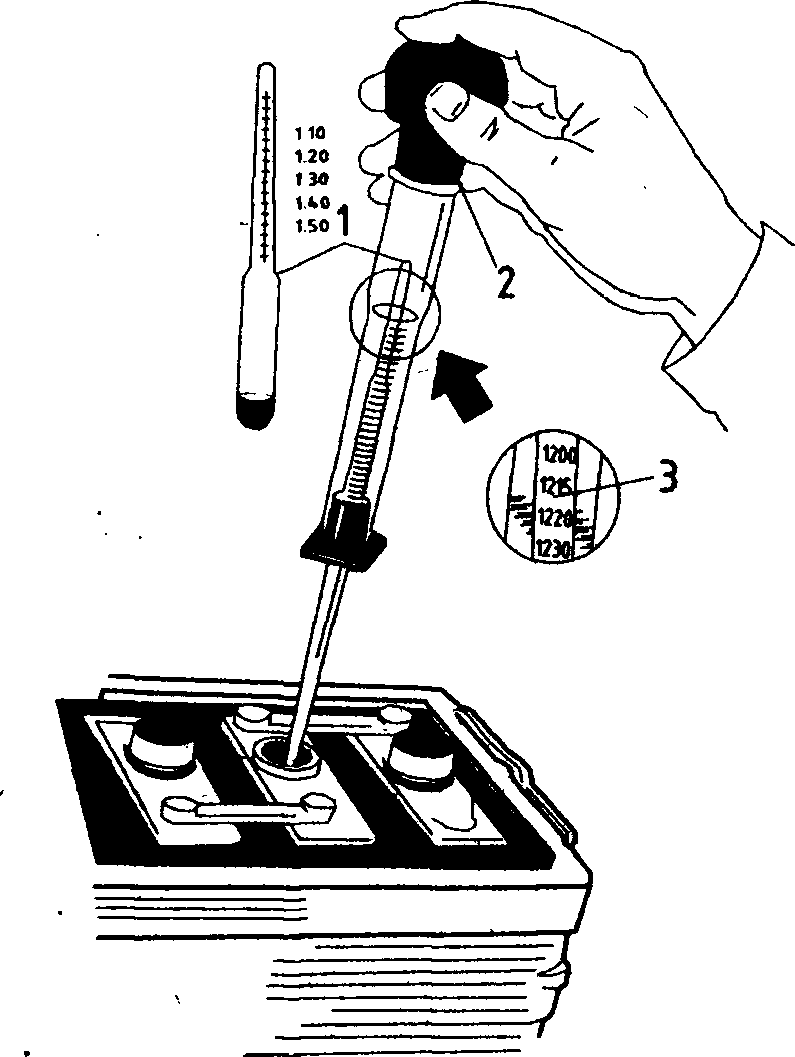
А также бывает, что проводя проверку плотности во всех отсеках аккумулятора, замечается её пониженное значение. Из этого можно с полной уверенностью сделать вывод о том, что произошла частичная сульфатация батареи. Когда количество электролита становится меньше за счёт кристаллизации серы на пластинах, то в этой ситуации аккумулятору просто необходимо срочное восстановление.
Подготовительные работы
Перед обслуживанием батареи следует изучить инструкцию, в которой полностью описано, как правильно доливать электролит в аккумулятор, а также важно прочитать инструкцию о зарядке.
Для того чтобы правильно долить электролит в аккумулятор, важно приготовить рабочее место, где будет проходить эта операция.
Также не стоит пренебрегать техникой безопасности:
- Первое, что нужно сделать — это надеть на себя спецодежду, которая включает в себя комплект штанов, куртки, прорезиненых перчаток и защитные очки.
- Поставить на верстак батарею и очистить её от различной грязи с помощью ветоши. Основное внимание нужно уделить плюсовому и минусовому контакту.
- Проверить батарею мультиметром.
- Аккуратно открыть крышки с помощью крестовой отвёртки.
Техническое обслуживание аккумулятора
После ряда этих манипуляций, обеспечивающих удобное обслуживание, специалисты проводят полную диагностику технического состояния аккумулятора. В основном они заключаются в шести пунктах:
- Перед тем как решить, что доливать в АКБ: электролит или воду, нужно обязательно полностью зарядить его специальным устройством.
- Далее произвести замер плотности во всех банках с помощью ареометра и зафиксировать все результаты в блокноте.
 При фиксировании показаний было бы удобнее проставить каждой банке свою цифру и напротив неё указать значение со шкалы.
При фиксировании показаний было бы удобнее проставить каждой банке свою цифру и напротив неё указать значение со шкалы. - Если показания плотности у заряженного аккумулятора в некоторых банках различаются и не входят в рекомендуемую норму (1.25−1.29 г/куб. см), то это означает, что водителю нужно провести корректировку. Она заключается в следующем: при пониженном показании плотности нужно рассчитать, сколько доливать электролита в аккумулятор и залить его, а при повышенном залить дистиллированную воду.
- Плотность каждой банки в предельных значениях, а уровень электролита по какой-то причине опускается всё ниже. Лучшим решением для этой проблемы будет банальная доливка воды.
- Иногда бывает так, что плотность в секциях ниже номинального значения (меньше 1.21 г/куб. см). Чтобы найти решение, нужно забрать с помощью специальной клизмы небольшой раствор кислоты и слить его в мерный стакан. Дальше записать показания объёма и перелить электролит в стеклянную кружку. Пользуясь технической таблицей, залить в мерный стакан нужное количество раствора серной кислоты с повышенной плотностью и с помощью клизмы влить в ту банку, из которой забирался электролит. В тех ситуациях, когда есть значительная разница в сторону уменьшения плотности, лучше всего доливать кислоту с плотностью 1.40 г/куб. см. Необходимый уровень важно достичь дистиллированной водой.
- После того как во всех банках плотность стала одинаковой, необходимо подключить аккумулятор на небольшую подзарядку. Это делается для того, чтобы недавно залитый раствор тщательно перемешался внутри. После этого снова измерить плотность, и если её уровень изменился, то провести повторную операцию.
Каждому автолюбителю нужно знать, что перед тем как перейти на зимнюю эксплуатацию автомобиля, важно повышать значения плотности в АКБ, а при переходе на летнее время — понижать.
А также ежедневно перед каждым выездом нужно проверять не только уровень масла в двигателе, но и чистоту клем батареи и надёжность крепления пробок на её корпусе.
Проверяем и восполняем уровень электролита в аккумуляторе. Сколько электролита должно быть в аккумуляторе? Какой уровень воды в аккумуляторе
От качества электролита сильно зависит долговечность и основные параметры аккумулятора. Поэтому если вы хотите, чтобы батарея служила вам верой и правдой не один год, предлагаем ознакомиться с основными нюансами ее обслуживания.
1 Почему электролит важен для аккумулятора?
Электролит – это раствор серной кислоты (Н2SO4) в воде, который способен накапливать и раздавать электрическую энергию в результате происходящих в нем химических реакций. Крайне важно, чтобы уровень этого раствора в (АКБ) находился в пределах нормы. Дело в том, что излишек жидкости приводит к окислению клемм, а это может стать причиной выхода из строя всей бортовой электроники.
Если же уровень электролита меньше положенной нормы, происходит пересыхание внутренних пластин и повышение плотности кислоты. В результате пластины начинают разрушаться, и АКБ окончательно выходит из строя. В таких случаях говорят: «В аккумуляторе «посыпались банки». Поэтому в интересах каждого автовладельца следить за уровнем электролита и поддерживать его на определенном уровне.
2 Проверка количества электролита в батарее
Аккумулятор, казалось бы, представляет собой замкнутую емкость, поэтому уровень жидкости в ней не должен изменяться. На практике же в процессе эксплуатации АКБ вода испаряется. Причем скорость уменьшения жидкости зависит от нескольких моментов:
- условий эксплуатации авто – перепады температур, часто включение и выключение зажигания, длительные поездки по трассе приводят к ускоренному испарению воды;
- исправности электрической системы – если имеются проблемы с электрикой, увеличивается нагрузка на АКБ.
 Особенно негативно на состоянии батареи сказываются проблемы с генератором.
Особенно негативно на состоянии батареи сказываются проблемы с генератором.
На аккумулятор оказывает влияние и манера вождения автомобиля, и некоторые другие факторы. При их сочетании уровень жидкости может упасть до критического в течение одного месяца. Но как его контролировать?
Проверка уровня может быть выполнена несколькими способами. Чаще всего корпус АКБ выполняют из полупрозрачного пластика и наносят метки «Min» и «Max». Соответственно, уровень раствора хорошо виден на глаз, особенно если поднять аккумулятор перед собой в солнечный день или в хорошо освещенном помещении.
Если пластик не просвечивается или на батарее отсутствуют метки, проверить уровень можно при помощи стеклянной трубки. Для этого нужно открутить пробку аккумулятора, затем опустить трубку до упора и закрыть верхнее отверстие пальцем. После этого надо вытащить трубку и замерить высоту столбика жидкости. Минимально допустимое значение составляет 12 мм, а максимальное – 15 мм. Подобным образом необходимо проверить уровень жидкости в каждой банке.
В современных дорогих моделях АКБ имеется специальный датчик уровня жидкости, так называемый «магический глаз». Чтобы проверить уровень, нужно аккуратно по нему постучать, после чего проявится определенный цвет. Каждый цвет имеет свое значение:
- зеленый – аккумулятор в норме;
- белый – уровень заряда меньше нормы, т.е. батарею нужно зарядить;
- красный – необходимо долить жидкость.
Надо сказать, что «магический глаз» не точно диагностирует состояние АКБ, поэтому желательно произвести дополнительную проверку.
3 Корректируем количество электролита
Если проверка показала, что уровень жидкости в банках низкий, его необходимо увеличить, путем доливки воды. Имейте в виду, что в аккумулятор можно заливать исключительно дистиллированную воду. Если вы зальете воду из-под крана, то АКБ разрядится полностью или вообще выйдет из строя, так как кислота вступит в реакцию с компонентами, которые имеются в водопроводной воде.
Температура дистиллированной воды, доливаемой в банку, должна быть в пределах 15-25 градусов.
Если уровень кислотного раствора превышает норму, его необходимо откачать. Для этих целей можно использовать шприц или спринцовку. После доливки жидкости желательно замерить уровень заряда. Если заряд низкий, АКБ нужно поставить заряжаться в течение нескольких часов.
4 Что еще нужно знать об электролите?
Важным параметром электролита является его плотность. Серная кислота сама по себе достаточно плотное вещество – этот параметр составляет 1,84 г/см³. Что касается плотности водяного раствора в аккумуляторе, показатель должен находиться в пределах 1,27–1,28 г/см³. Если плотность электролита в аккумуляторе будет отличаться от положенной, долговечность АКБ сильно снизится и изменятся основные параметры.
Среди автомобилистов «советской закалки» бытуем мнение, что зимой плотность электролита должна быть выше, чем летом. В действительности же в современные аккумуляторы и зимой, и летом заливают кислотный раствор плотностью 1,27 г/см³. При такой плотности жидкость начинает замерзать при температуре -60 градусов.
Для проверки плотности применяют специальный прибор, который называется ареометром. Он представляет собой стеклянную трубку со шкалой, внутри которой расположен поплавок. С одной стороны трубки расположена резиновая груша, которая позволяет набирать в трубку жидкость. После забора электролита поплавок свободно перемещается вдоль трубки и показывает уровень плотности.
При проверке плотности соблюдайте два правила:
- после доливки дистиллированной воды нельзя сразу проверять плотность. Должно пройти некоторое время, чтобы вода хорошо перемешалась с водой. Обычно для этого требуется 3-4 часа;
- измеряйте и корректируйте плотность после полной зарядки АКБ.
Если ареометр показал, что плотность слишком низкая, следует долить специальный корректирующий электролит, плотность которого составляет 1,4 г/см³. Корректирующий электролит можно купить или сделать самостоятельно, смешав серную кислоту с дистиллированной водой. Единственное, работайте с кислотой очень осторожно, соблюдая все правила техники безопасности. Причем заниматься этим лучше на улице, но не в домашних условиях. Учтите, что в процессе смешивания кислоты с дистиллированной водой выделяется тепло.
Корректирующий электролит можно купить или сделать самостоятельно, смешав серную кислоту с дистиллированной водой. Единственное, работайте с кислотой очень осторожно, соблюдая все правила техники безопасности. Причем заниматься этим лучше на улице, но не в домашних условиях. Учтите, что в процессе смешивания кислоты с дистиллированной водой выделяется тепло.
Ни в коем случае не заливайте серную кислоту прямо в аккумулятор, так как жидкость может закипеть и АКБ выйдет из строя.
Если оказалось, что плотность электролита выше положенного значения, слейте с банок небольшое количество раствора в специальную емкость и добавьте дистиллированную воду. Так как концентрация серной кислоты в электролите достаточно высокая, работать с жидкостью необходимо тоже очень осторожно.
5 Восстанавливаем старый аккумулятор новым электролитом
Если вы заметили, что АКБ стал быстро разряжаться, при этом электрика в автомобиле в полном порядке, скорее всего батарея выходит из строя. Но не спешите отправляться в автомагазин за покупкой нового аккумулятора. Как правило, замена раствора позволяет исправить ситуацию.
Надо сказать, что заменить электролит имеет смысл и в других некоторых случаях:
- АКБ длительное время не использовался;
- жидкость стала мутной. Имейте в виду, что серый оттенок раствора может свидетельствовать о том, что АКБ нужно зарядить. После полноценной зарядки первоначальная прозрачность жидкости возвращается.
Прежде чем поменять жидкость, подкорректируйте плотность нового электролита, чтобы она составляла 1,28 г/см³. Старый кислотный раствор полностью слейте и залейте дистиллированную воду. Затем аккумулятор нужно интенсивно потрясти и слить с него воду. Повторяйте процедуру до тех пор, пока вместе с водой не выйдет вся угольная крошка.
Перед заливкой в электролит желательно добавить специальную присадку, удаляющую сульфат с электродов. Затем залейте жидкость в горловины банок. Делайте это потихоньку, при помощи воронки с узким горлышком. Чтобы присадка полностью растворилась, аккумулятор нужно оставить на 48 часов. После этого необходимо поставить его на зарядку под током 0,1 А. Зарядка должна осуществляться циклично, т.е. по схеме зарядка/разрядка, пока не восстановится плотность электролита. В итоге напряжение на клеммах должно составлять 14-15 В.
Делайте это потихоньку, при помощи воронки с узким горлышком. Чтобы присадка полностью растворилась, аккумулятор нужно оставить на 48 часов. После этого необходимо поставить его на зарядку под током 0,1 А. Зарядка должна осуществляться циклично, т.е. по схеме зарядка/разрядка, пока не восстановится плотность электролита. В итоге напряжение на клеммах должно составлять 14-15 В.
По достижении этого напряжения зарядный ток следует уменьшить в два раза и заряжать батарею еще на протяжении двух часов. Если плотность не меняется, зарядку надо прекратить и разрядить АКБ до напряжения 10 В с применением тока 0,5 А.
- T – время разрядки;
- I – разрядный ток;
- С – емкость АКБ.
Если оказалось, что емкость составляет менее 4 ампер/часов, цикл заряда необходимо повторить, чтобы повысить показатель емкости. Если вы произведете вышеописанную процедуру правильно, о покупке нового аккумулятора на некоторое время можно будет забыть.
Очень важно не только уметь хорошо управлять автомобилем, но и знать, из чего состоит машина, как за ней следить и правильно ее обслуживать. В этой статье рассмотрим актуальный вопрос для АКБ: каким должен быть уровень электролита в автомобильном аккумуляторе, и на что он влияет?
Электролит и его роль в аккумуляторе
Итак, начнем с определения, что же все-таки называется электролитом. Это попросту раствор серной кислоты и дистиллированной воды. Причем наличие каких-то посторонних примесей недопустимо, ведь тогда изменится его плотность, что самым негативным образом отразится на работе аккумуляторной батареи. Также очень важную роль играет и его уровень. Так, например, если он будет ниже нормы, произойдет высыхание внутренних пластинок и мощность снизится.
Не стоит думать, что выходом будет доливание жидкости сверх нормы, ведь в этом случае кислота разъест внешнюю часть агрегата. Кроме того, можно столкнуться и с такими проблемами, как быстрая саморазрядка батареи или выход из строя регулятора напряжения. В общем, залогом нормального функционирования вашего автомобиля служит надлежащий уровень электролита, поэтому периодически следует осматривать АКБ.
В общем, залогом нормального функционирования вашего автомобиля служит надлежащий уровень электролита, поэтому периодически следует осматривать АКБ.
Как проверить уровень электролита в аккумуляторе?
Бытует мнение, что аккумуляторные батареи не нуждаются в техническом обслуживании, и, в принципе, так оно и есть, но учтите — речь идет о нормальных условиях эксплуатации. Любителям же путешествовать на своем «железном коне» или же жителям регионов, в которых царит очень жаркое лето, все-таки стоит контролировать вышеуказанный параметр. Ведь в состав электролита входит вода, а она, как известно, имеет свойство испаряться.
Кроме того, интенсивному выкипанию способствуют и неисправности реле-регулятора. О том, что пора проверить состояние аккумулятора, свидетельствуют следующие признаки:
- из заливных отверстий сильно парит;
- на корпусе АКБ можно увидеть капли электролита;
- сам аккумулятор очень интенсивно нагревается.
Проверка уровня электролита в аккумуляторе осуществляется разными способами. Наиболее простой – визуальный контроль. Обычно корпус батареи, в котором находится жидкость, делают прозрачным, и на него наносятся отметки, указывающие максимальный и минимальный уровень. И, соответственно, количество электролита должно находиться в этих пределах.
Снижается уровень электролита за счет испарения воды или вытекания состава из-за повреждения корпуса. В первом случае можно самостоятельно поправить состояние АКБ.
Но иногда такая возможность отсутствует, тогда необходимо действовать примерно так. Берем прозрачную трубочку диаметром в 5 миллиметров и опускаем ее в резервуар до упора. Затем плотно зажимаем пальцем наружное отверстие трубки и вытаскиваем ее. В ней будет находиться измеряемая жидкость. Уровень электролита будет соответствовать высоте его столба в данной трубочке.
В АКБ низкий уровень электролита – что делать автовладельцу?
Итак, высота жидкости в трубке должна быть в пределах 10–15 миллиметров. Если ее больше нормы, тогда следует убрать лишнюю. Сделать это довольно просто, нужна всего лишь резиновая груша или шприц, которыми за считаные секунды можно выкачать излишки. Естественно, после этой операции еще раз осуществляем проверку. А вот если анализ показал низкий уровень электролита, что делать тогда?
Если ее больше нормы, тогда следует убрать лишнюю. Сделать это довольно просто, нужна всего лишь резиновая груша или шприц, которыми за считаные секунды можно выкачать излишки. Естественно, после этой операции еще раз осуществляем проверку. А вот если анализ показал низкий уровень электролита, что делать тогда?
В таком случае заливать новый раствор не рекомендуется, так как это повлияет на плотность и также негативно отразится на состоянии батареи . Ведь испаряется только вода, а концентрация серной кислоты остается прежней. Поэтому следует добавлять дистиллированную воду комнатной температуры. Причем использование простой жидкости из крана категорически запрещено, так как батарея может разрядиться. Заливать сам электролит можно только в одном случае: если его уровень снизился из-за разбрызгивания либо вытекания.
Уровень электролита в аккумуляторе – это то, на что должен обращать внимание каждый автомобилист. Ведь от данного параметра зависит работоспособность автотранспорта, срок эксплуатации и частота обслуживания акб. Допустимо выполнение таких действий в домашних условиях.
Автомобили комплектуются такими аккумуляторами:
- WET (свинцово-кислотные акб). Электролит представлен в виде водного раствора, включающего серную кислоту.
- AGM. Отличаются тем, что входящее в состав стекловолокно пропитано электролитическим составом.
- GEL (гелиевый акб). Электролит представлен в виде геля. Для этого в серно-водный раствор введена окись кремния.
Определять, сколько электролита в аккумуляторе, необходимо, если речь идет о свинцово-кислотных источниках питания.
Особенности проверки уровня электролита в автомобильном аккумуляторе
Регулярно проверяя уровень электролита в аккумуляторе, контролируя плотность, можно поддерживать автотранспорт, отдельные узлы в работоспособном состоянии. При необходимости проводят корректировку плотности, увеличивают или уменьшают уровень электролитического состава. Ведь использование источника питания, в котором электролитической жидкости меньше нормы, приводит к пагубным последствиям.
Просмотрите интересное видео про уровень электролита.
Проверка уровня электролита
Информация о том, какой уровень электролита должен быть, присутствует в технической документации, которая прилагается к автотранспортному средству. Для проверки и контроля используется два метода, каждый из которых имеет свои особенности:
- На корпусе АКБ сосредоточены отметки max и min. Если корпус подготовлен из прозрачного материала, то легко определить количество электролитического состава. На основании полученной информации нужно принимать решение об уменьшении, увеличении дистиллированной воды. Такой способ малоэффективен, если корпус окрашен в черный цвет.
- Уровень электролита в акб проверяют с помощью стеклянной, пластиковой трубочки. Диаметр трубки – 3–5 мм. Перед тем как ввести трубку, изымается пробка. Опускается трубка до момента соприкосновения с пластинами. Норма – 12 мм. Такая процедура проводится для каждой банки, входящей в состав аккумуляторной батареи.
Избыток электролитического состава изымается с помощью шприца. Этот же инструмент используется для введения подготовленного электролита или дистиллированной воды.
Для того чтобы определить уровень жидкости в необслуживаемых источниках питания, используются отметки на поверхности акб. Дополнительно применяется индикатор заряда.
Причины снижения уровня электролита
- Чрезмерное увеличение выдаваемого генератором напряжения.
- Деформация корпуса аккумуляторной батареи, появление микротрещин или других дефектов.
- КЗ внутри источника питания.
- Наличие свинцового осадка и мусора.
В кислотно-свинцовых источниках питания уровень дистиллята постепенно снижается. При этом неопытные автомобилисты пытаются исправить ситуацию, добавив водный раствор с введенной серной кислотой. В результате, увеличивается уровень и плотность. Это приводит к тому, что аккумуляторная батарея быстро выходит из строя, внутренняя часть стремительно разрушается.
Неправильно определенный уровень приводит к таким последствиям:
- Разрушение свинцовых пластин, формирование остатков и шлама.
- Со временем образуются мостики между включенными в состав пластинами. Такие мостики способствуют возникновению КЗ, снижению мощности.
- Появление подтеков, затрудняющих эксплуатацию аккумуляторной батареи.
- Окисление основных контактов.
- Выход из строя аккумуляторной батареи.
Определение плотности электролитического состава
К проверке плотности приступают после тщательной зарядки аккумуляторной батареи. Предварительно подготавливается прибор, при помощи которого устанавливается степень плотности. Чаще всего используется ареометр.
С банок, сосредоточенных в корпусе источника питания, изымаются пробки. В отверстие помещается ареометр, набирается немного электролитического состава. Поплавок, включенный в состав, содержит шкалу с соответствующими отметками, которая используется для определения степени плотности. Оптимальный показатель – 1,29-1,3 г/см3.
Для понижения степени плотности электролитического состава допускается применение дистиллята, который реализуется в специальных магазинах, аптеках. Процедура введения дистиллированной воды осуществляется поэтапно. При этом в каждой банке периодически измеряется этот показатель.
Повысить плотность сложнее, чем увеличить уровень электролита в акб. Ведь изначально изымается часть состава при помощи ареометра, другого инструмента. После этого вводится смесь с соответствующей плотностью. Иногда возникает потребность в полной замене жидкости. Выявить это можно, если знать, как проверить уровень, степень плотности.
Процедура замены электролита
Полную замену проводят при условии, что уровень плотности значительно снизился. Процедура имеет особенности, правила. Перед выполнением нужно подготовить:
- Смесь с соответствующей плотностью (около 1,29 г/см3).
- Тара, подходящая для размещения старого раствора.

- Ареометр или другой инструмент.
Запрещено переворачивать источник питания для последующего удаления водно-серного раствора. Ведь это приводит к разрушению свинцовых пластин, образованию мостиков и подтеков, замыканию.
Перед работой должно быть подготовлено все необходимое для защиты: перчатки из плотной резины, прочная одежда, защитные очки. Ведь попадание смеси на кожу провоцирует образование химических ожогов.
Для откачки старой смеси применяют «грушу» или другой инструмент. Откачиваемую жидкость помещают в специальную тару, отличающуюся стойкостью, прочностью.
Заливку новой смеси выполняют поэтапно, соблюдая правила, нормы.
Меры безопасности
При работе с растворами, в состав которых входит серная кислота, требуется выполнение таких правил:
- Все предметы одежды, элементы должны быть подготовлены из прочности и стойкого материала.
- Для хранения использованной электролитической смеси применяется стеклянная либо полиэтиленовая тара, оснащенная плотными крышками и оплеткой.
- Для заливки используется только качественный состав, реализуемый в специальных магазинах. Самостоятельная подготовка приемлема при условии, что человек обладает требуемым опытом и знаниями, инструментами.
- Замена электролитической смеси проводится только после отключения аккумуляторной батареи, ее демонтажа.
- Перед подключением источника питания проверяется состояние выводов, ликвидируются окислы.
Точно определить уровень, плотность электролитического состава несложно. Достаточно соблюдать правила и рекомендации, подготовленные специалистами. С особой тщательностью нужно выбирать помещение, в котором будут проводиться все работы. В помещении должна быть вентиляционная система. Ведь в смеси присутствует кислота, другие вещества.
Своевременная проверка основных показателей – залог эффективной работы аккумуляторной батареи.
Видео про проверку электролита в аккумуляторе
От состояния аккумулятора зависит, сможете вы завести мотор своего автомобиля, или нет. Прочитав статью, вы узнаете, что влияет на уровень электролита и научитесь определять и регулировать его. Вы узнаете, как уровень электролита влияет на состояние аккумулятора и почему падение уровня снижает не только емкость, но и ресурс аккумуляторной батареи.
Прочитав статью, вы узнаете, что влияет на уровень электролита и научитесь определять и регулировать его. Вы узнаете, как уровень электролита влияет на состояние аккумулятора и почему падение уровня снижает не только емкость, но и ресурс аккумуляторной батареи.
Что влияет на уровень электролита
Для ответа на этот вопрос, необходимо понимать, что происходит внутри аккумулятора во время заряда и разряда. При подаче зарядного тока диоксид свинца на катоде (отрицательном контакте) отдает не только свободные электроны, но и молекулы кислорода, превращаясь в свинец. На аноде (положительном электроде) наоборот, свинец впитывает из электролита электроны и молекулы кислорода, превращаясь в диоксид свинца. В обоих процессах из электролита выделяется свободный водород и незначительное количество кислорода, которые уходят в атмосферу. Чем сильней зарядный или разрядный ток, тем больше водорода и кислорода уходит в атмосферу. Помимо этого сильный зарядный или разрядный ток приводит к закипанию электролита, в результате чего в атмосферу уходит не только чистый водород и кислород, но и водяной пар. Все это со временем приводит к падению уровня электролита. Этот процесс происходит в любом аккумуляторе.
Почему снижается уровень
Если уровень электролита падает настолько, что открывает свинцовые пластины, то ресурс аккумулятора резко снижается. Это вызвано тем, что в реакции окисления и восстановления вмешивается газообразный кислород из атмосферы. В результате баланс чистого свинца и его диоксида меняется, а вместе с ним падает емкость и рабочее напряжение аккумулятора. Добавление дистиллированной воды позволяет , но не может восстановить их состояние. Еще одна причина, по которой может падать уровень электролита — механическое повреждение корпуса. Даже небольшая трещина, которую очень сложно заметить невооруженным взглядом, может стать причиной потери электролита. При утечке в размере 1 капли в час, за месяц аккумулятор потеряет 30-50 миллилитров электролита. Примерно 0,5 литра в течение года, то есть почти весь электролит одной банки аккумулятора.
Примерно 0,5 литра в течение года, то есть почти весь электролит одной банки аккумулятора.
Как проверить и восстановить уровень электролита
Для проверки электролита вам понадобятся:
- чистая тряпка, чтобы очистить его поверхность от грязи;
- широкая (не менее 1 см) плоская отвертка, с помощью которой вы будете откручивать заливные пробки;
- фонарик.
Откройте капот и осмотрите аккумулятор. На некоторых автомобилях для проверки и доливки электролита приходится снимать аккумулятор. Если ничто не мешает выкручивать пробки и пользоваться фонариком, то тряпкой очистите аккумулятор от пыли, грязи и капелек жидкости. Его поверхность должна быть сухой и чистой. Если заливные пробки закрыты пластиковой накладкой, то снимите ее. Затем выкрутите все пробки и уберите их в сторону. Уровень электролита должен быть на 1,5-2 см ниже поверхности аккумулятора. Для более точной проверки уровня необходима стеклянная или пластиковая палочка. Вставьте ее в заливное отверстие и доведите до верхнего края пластин. Уровень электролита должен превышать пластины на 1,5-2 см. Если уровень ниже и, вы не видите электролит, посветите в заливное отверстие фонариком. Если видны пластины, значит, ресурс аккумулятора уже пострадал. Если восстановить уровень и плотность электролита, то он будет давать нормальный ток, но емкость снизится.
Если уровень электролита меньше, чем должен быть, проверьте его с помощью ареометра, который можно купить в любом автомагазине. Если плотность электролита разряженного аккумулятора ниже 1,2 г/см³, а полностью заряженного ниже 1,29 г/см³, проблема в корпусе аккумулятора. Испарение кислорода и водорода уменьшает объем, но повышает плотность электролита выше стандартной. Утечка не только снижает объем, но и . Аккумулятор, который теряет электролит чинить бесполезно, в большинстве случаев трещина незаметна. Иначе вокруг аккумулятора было бы мокрое пятно.
Убедившись, что проблема не в утечке электролита, приступайте в восстановлению его уровня. Для этого используйте только дистиллированную воду. Желательно наливать ее с помощью лейки. Это позволит избежать разлива воды по поверхности аккумулятора и попадания в банки различных загрязняющих веществ, которые станут участниками химических реакций. Заливайте воду тонкой струйкой, это позволит избежать превышения уровня. Подняв уровень электролита, прочистите отверстие (сапун) пробки и вкрутите ее в аккумулятор. Так поступите с каждой банкой аккумулятора.
Иногда владельцы автомобилей спрашивают о том, как проверить . Если выражаться корректнее и точнее, речь идет о том, как проверить плотность электролита в аккумуляторе. Как известно, уровень электролита в батарее измеряется в том случае, если АКБ относится к категории обслуживаемых. Для того чтобы научиться делать это самостоятельно, как в гараже, так и в домашних условиях, нужно знать о том, что представляет из себя жидкий электролит и как устроена внутри обслуживаемая автомобильная батарея.
Что находится внутри АКБ
Внутри аккумуляторной батареи автомобиля в определенной последовательности расположены шесть отсеков, или «банок». Каждый отсек имеет свинцовые пластины с положительными и отрицательными зарядами. «Банка» устроена герметично, и ее контакт с другими элементами происходит через общее полярное соединение.
Уровень напряжения в каждом отсеке АКБ составляет 2, максимум — 2,1 вольт. Все элементы соединяются друг с другом в последовательную электрохимическую цепь, имея на выходе общее напряжение 12 вольт.
Благодаря тому, что каждая «банка» заполнена особым химическим соединением, имеющим жидкую консистенцию, автомобильный аккумулятор обладает способностью накопления и отдачи электрического заряда. Эта жидкость получила название «электролит», а такие простые теоретические знания из области физики и химии помогут разобраться в том, как проверить плотность аккумулятора (точнее, электролита) правильно.
Для чего необходимо проверять плотность электролитической жидкости
Любой электролит представляет собой не что иное, как химическую смесь, состоящую из дистиллированной воды и серной в определенной пропорции: вода 65%, 35% — кислота. Именно такое процентное соотношение и позволяет электролиту осуществлять накопление электрического заряда без нанесения урона чувствительным свинцовым пластинам АКБ.
В процессе постоянной эксплуатации батареи происходят постоянные изменения плотности электролита, что определенным образом может сказаться на ее рабочих функциях. Само понятие плотности, кстати, означает не что иное, как процентное соотношение серной кислоты к дистилляту.
Если уровень серной кислоты внутри аккумулятора становится слишком высоким, это может печально закончиться для его пластин. Бывают ситуации, когда кислота попросту разъедает свинец, и пластины разрушаются.
Если же кислоты слишком мало, это означает, что АКБ разряжена или близка к тому, чтобы разрядиться полностью. Аккумулятор не может работать в режиме той емкости, которая указана в его технических характеристиках. Например, энергии может просто не хватить в условиях холодного запуска двигателя внутреннего сгорания.
Также, если водитель долго пытается ездить на разряженном аккумуляторе, процесс оседания сульфатов на пластинах неизбежен. На них образуется плотный белый налет, убрать который порой бывает весьма проблематично. При критичном уровне сульфатов произойдет либо разрушение пластин, либо короткое замыкание. Потребуется .
Принцип работы аккумуляторной батареи
Чтобы знать, как правильно измерять уровень электролита, важно помнить — любая АКБ работает по цикличному принципу. Вначале она осуществляет накопление заряда внутри, а затем, при запуске двигателя, начинает его постепенно отдавать автомобилю, приводя его в движение. При отдаче заряда аккумулятором кислота выделяет те самые сульфаты (соли), оседающие на пластины «банок». А в «банках» происходит образование воды. Это приводит к тому, что уровень электролита значительно снижается.
Что потребуется сделать в данном случае:
- когда уровень плотности выше требуемого, нужно разбавить электролит дистиллированной водой;
- когда плотность снижается, батарея срочно нуждается в полноценной зарядке в течение, как минимум, 10-12 часов.
Как проверить электролит и измерить его плотность
Перед тем как проверить электролит в аккумуляторе, очистите его поверхность от грязи и пыли, чтобы при снятии крышек с батарейных отсеков они не попали внутрь . Возьмите тонкую трубку из стекла, ее диаметр может составлять от 4 до 5 миллиметров. Теперь нужно опустить трубку в отсек до конца, так, чтобы она коснулась его дна. Отверстие можно закрыть с помощью пальца (предварительно не забудьте обезопасить себя, надев технические перчатки!).
Достаньте из банки трубку: в нее должно попасть небольшое количество электролитической жидкости. Ориентируйтесь на ее высоту — сколько места она занимает в трубке. Если высота жидкости 10-15 миллиметров — плотность в пределах нормы, а когда уровень больше, либо меньше — плотность необходимо откорректировать.
Перед тем как приступить к корректировке плотности, нужно произвести ее точные замеры — в каждом аккумуляторном отсеке по отдельности, так как они между собой не сообщаются. Обязательно зарядите АКБ перед измерением, иначе результаты могут оказаться неверными. Кроме этого, незадолго до процесса батарею нужно на 3-4 часа оставить в помещении с комнатной температурой (от 20°С, можно чуть выше). Ведь химическая жидкость имеет прямую зависимость от температурного фактора.
Для измерения уровня плотности электролита применяется такой простой инструмент, как . Его еще иногда называют более сложным словом — денсиметр. Но по сути это одно и то же. Ареометр состоит из наконечника, поочередно опускаемого в аккумуляторные отсеки, колбы, резиновой груши для отсасывания жидкости и шкалы измерений, которая расположена внутри колбы.
Алгоритм действий проверки будет таким:
- вытрите наконечник насухо чистой тряпочкой;
- опустите его в аккумуляторный отсек;
- резиновой грушей наберите небольшое количество жидкости;
- следите за «поведением» электролита: когда он перестанет двигаться — замерьте плотность по шкале;
- слейте жидкость обратно в «банку».
Как видите, техника снятия показаний очень проста. Главное — не забывать защитить руки с помощью перчаток.
Цифровые показатели, на которые нужно ориентироваться
Поскольку химическая составляющее АКБ напрямую зависит от температурных факторов, существуют общепринятые цифровые показатели, обозначающие уровень оптимальной концентрации электролита. На юге РФ это 1,25 , в районах средней полосы — 1,27 , а в северных регионах — 1,29 гр/см 3 .
Итак, как проверить уровень электролита в аккумуляторе и его плотность? Отнесите батарею в помещение с комнатной температурой, удалите с нее загрязнения, откройте банки и воспользуйтесь стеклянной трубочкой и ареометром. Не забудьте надеть перчатки. нужно осуществлять регулярно для обеспечения наилучшего уровня его работы.
«Как определить уровень электролита в аккумуляторе?» – Яндекс.Кью
Посмотрите на уровень электролита. Заглянув в каждое заливное отверстие, можно определить уровень этого вещества в каждом из отсеков. Должно быть одинаковое количество электролита во всех отсеках
Если уровни слегка отличаются, то причина может быть в том, что в прошлый раз вы налили слишком много жидкости. В этом случае, когда этот излишек испариться, просто наливайте необходимое количество.
Если уровни явно разные, то дело может быть в треснувшем корпусе и небольшой утечке электролита. В таком случае требуется замена аккумулятора. Если мест очевидной утечки не видно, то долейте в аккумулятор дистиллированную воду (ничего другого) до максимально безопасного уровня и спустя несколько недель проверьте, насколько изменился ее уровень.
Определите низкий уровень электролита. Если электролит не покрывает пластины полностью, значит его недостаточно. В таком случае аккумулятор не сможет функционировать с максимальной производительностью.
Части пластины, подверженные воздействию воздуха, разрушаются за считанные дни.
Если уровень электролита опустился только на 1 см ниже верхней кромки пластины, то, налив необходимое количество воды, аккумулятор снова заработает, однако его производительность немного снизится. (Советы как добавлять воду, будут рассмотрены в 3-ей части этой статьи) Если же уровень опустился намного ниже, возможно, вам придется менять аккумулятор.
Низкий уровень электролита может свидетельствовать о перезарядке аккумулятора. В этом случае нужно проверить генератор переменного тока.
Определите нормальный уровень электролита. Нормальным уровнем считается уровень электролита, который либо выше пластин примерно на 1 см, либо ниже горловины заливного отверстия на 3 мм.
Если все в норме, то доливать воду пока нет необходимости. Можете просто закрутить обратно пробки заливных отверстий. Следующую проверку нужно будет провести через три месяца.
Определите предельный уровень электролита. Уровень жидкости находится на безопасном максимуме, когда электролит касается горловины заливного отверстия.
Где-то в нижней части большинства горловин есть пара выемок. Благодаря этим выемкам образуется мениск (жидкость выгибается возле края горловины, по форме напоминающая глаз). Если жидкость касается горловины, мениск появляется. Если ниже горловины, мениска не видно.
Мениск в форме глаза нужен для того, чтобы избежать переливов. Вам стоит воспользоваться фонариком, чтобы иметь возможность определить уровень жидкости и увидеть, есть ли мениск.
Источник: https://ru.wikihow.com/проверить-уровень-жидкости-в-автомобильном-аккумуляторе
Необслуживаемые аккумуляторы: Жидкостные, Гелевые и AGM
Такие аккумуляторы бывают различных типов: Жидкостные, Гелевые и AGM. Начнем с того, что это все кислотные аккумуляторы и принцип их работы не отличается от друг от друга.
12-ти вольтовый Аккумулятор состоит из шести ячеек, в которых находятся электродные блоки, состоящие из пластин (решеток) положительных и отрицательных с нанесенной на них активной массой и разделенных между собой сепаратором, все это залито электролитом. Процесс образования (выработка) электричества происходит при химическом взаимодействии между активной массой, нанесенной на решетки и электролитом.
Основное принципиальное отличие Обычных жидкостных, Гелевых (GEL) и VRLA или SLA созданных по AGM технологии батарей заключается в физическом состоянии электролита:
- Обычные аккумуляторы имеют — жидкий электролит.
- Гелевые (GEL) — загущенный электролит до нетекучего состояния с помощью специальных присадок.
- VRLA или SLA, произведенные по AGM технологии — электролит абсорбирован (впитан) в сепаратор.
Решетки электродов, удерживающие активную массу, легируют сурьмой и мышьяком. Добавки улучшают технологичность литья, повышают твердость и коррозионную стойкость электродов. В то же время сурьма способствует повышенному расходу воды и снижению ЭДС батареи в процессе эксплуатации.
Дальнейшее развитие привело к снижению доли сурьмы в составе сплава, из которого льют решетки. Это привело к появлению малообслуживаемых аккумуляторов (малосурьмянистые технологии), так же увеличился срок службы батареи. Затем из отрицательных пластин сурьму вытеснил кальций. Появились «Гибридные» аккумуляторы стали требовать долива еще реже.
Применение кальция в положительных и отрицательных пластинах (кальциевые технологии) привело к появлению батарей, теоретически не требующих долива на протяжении всего срока эксплуатации. Однако такие батареи выходят из строя от глубоких разрядов. Чтобы повысить стойкость, в свинцово-кальциевый сплав положительных пластин стали добавлять серебро. Применение лабиринтных крышек и пробок, конденсирующих остатки испарения воды и возвращающих ее обратно в аккумулятор, привело к появлению полностью необслуживаемых батарей в течение всего срока их жизни.
Гелевые аккумуляторы появились с началом освоения космоса. Гель, получающийся в результате добавления в серную кислоту двуокиси кремния, позволяет добиться полной герметичности батареи, так как все газовыделение происходит внутри пор в массе геля. Таким батареям нет равных по стойкости к глубоким разрядам, они намного долговечнее традиционных. Но распространения у автомобилистов гелевые аккумуляторы не получили по причине очень высоких требований к бортовому электрооборудованию и из-за резкого падения пускового тока на холоде.
Наиболее современная технология (AGM) вновь вернулась к жидкой кислоте, но теперь электролит удерживается в порах сепаратора из ультратонких стеклянных волокон. Такая конструкция позволяет не только герметизировать корпус, но и сохранить работоспособность батареи даже в случае повреждений наружной оболочки. AGM-батареи нечувствительны к колебаниям температуры, очень стойки к глубоким разрядам, долговечны, виброустойчивы и могут работать хоть лежа на боку, но боятся перезаряда.
ОСОБЕННОСТИ ГЕЛЕВЫХ АККУМУЛЯТОРОВ
Гелевый электролит заполняет пространство между пластинами аккумулятора, но сепаратор не исключается. Рекомбинация газов в гелевых аккумуляторах имеет эффективность до 97%. Гель эффективнее фиксирует материал пластин, снижая их износ в режимах глубоких разрядов, поэтому циклический ресурс гелевых аккумуляторов в 2-3 раза выше, чем у обычных, поэтому их целесообразно применять в тех случаях, где такое применение (циклический режим с глубоким разрядом) востребовано. Гелевые аккумуляторы также могут эксплуатироваться в любом положении (кроме перевернутого), имеют несколько меньший саморазряд, поэтому гелевые аккумуляторы предпочтительно использовать в тех режимах, где разряд производится малым током на протяжении длительного времени.
В гелевом электролите ионы имеют худшие показатели подвижности (в силу большей плотности среды), что отрицательно сказывается на динамических разрядных и зарядных характеристиках гелевых аккумуляторов. Более того, может наблюдаться временный провал в напряжении при резком увеличение нагрузки, что может приводить к неадекватному поведению оборудования; поэтому следует с осторожностью применять гелевые аккумуляторы в системах управления током и т.п. устройствах с коммутацией быстроизменяющихся токов. Гелевые батареи очень чувствительны к качеству зарядки аккумуляторы с гелем внутри можно применять лишь там, где бортовая электрика позволяет очень точно поддерживать режим заряда. Куда там, на отечественных автомобилях даже с исправным реле-регулятором напряжение «гуляет» с 13 до 16 вольт! Да и на большинстве иномарок немногим лучше. А уж если реле-регулятор из строя выйдет, то гелевый аккумулятор можно сразу выбрасывать. Не зря же на нем написано: напряжение заряда не более 14,4 В. Если больше, то гель тает как холодец в тепле и обратно уже не восстанавливается. И вот еще что: у настоящих гелевых батарей, конечно, может быть огромный ток, но только летом. Гель и так вязкий, а на морозе он совсем застывает. В результате характеристики падают наполовину и больше.
Зарядка гелевых аккумуляторов ограничивается очень малыми токами, в противном случае возникает опасность «вспучивания» геля избыточными газами из-за меньшей эффективности рекомбинации и ограниченной теплопроводности. Гелевые аккумуляторы предпочтительней питать от зарядных устройств с высоким качеством напряжения (стабильность, минимум пульсаций) во избежание перезаряда и перегрева, они не переносят даже кратковременных коротких замыканий — любое КЗ (например, при установке аккумулятора Вы случайно замкнули на долю секунды два полюса металлическим гаечным ключом) моментально выводит аккумулятор из строя.
Высокие вибрации приводят к разжижению геля и стеканию его с пластин. Как видим, гелевые аккумуляторы «лушче» (если так можно сказать), только в плане повышенного циклического ресурса и меньшего % саморазряда. К тому же такой тип батарей самый дорогой.
СВИНЦОВО—КИСЛОТНЫЕ, ГЕРМЕТИЗИРОВАННЫЕ, КЛАПАННО-РЕКОМБИНАЦИОННЫЕ АККУМУЛЯТОРЫ (VRLA или SLA)
- VRLA (Valve Regulated Lead Acid) в переводе с английского — Клапанно-Регулируемые Свинцово-Кислотные;
- SLA (Sealed Lead Acid) — Герметизированные Свинцово-Кислотные;
- AGM (Absorbent Glass Mat) — это технология изготовления свинцово-кислотных аккумуляторов, созданная инженерами Gates Rubber Company в начале 1970-х годов. Пористый сорбент из стекловолокна (AGM) — впитывающий сепаратор, использующийся между пластинами в VRLA-батарее.
Особенность аккумуляторов типа VRLA — отсутствие необходимости долива воды в течение всего срока службы и практически полное отсутствие выделения газов (водорода и кислорода) — продуктов электролиза воды, входящей в состав электролита. Поэтому их нередко называют герметизированными необслуживаемыми. Незначительное обслуживание, тем не менее, необходимо: прежде всего, визуальный осмотр, протирание от пыли, подтяжка соединений и контроль напряжений.
Благодаря особенностям конструкции и составу материалов пластин, сепараторов и электролита продукты электролиза воды — молекулы водорода и кислорода — в аккумуляторах данного типа рекомбинируют, превращаясь в молекулы воды и возвращаясь в состав электролита.
Коэффициент рекомбинации при нормальных условиях эксплуатации достаточно высок и может достигать >99 %. Поэтому лишь очень незначительная часть непрорекомбинировавших газов накапливается внутри корпуса аккумулятора и затем при превышении заданного уровня давления стравливается в атмосферу через специальные клапаны.
Преимущества:
- Устойчивость к вибрации, возможность установки в любом положении и в отсутствии необходимости обслуживать, высокий пусковой ток.
- Конструкция не требующая обслуживания.
- Конструкция герметична и имеет клапанную регулировку, предотвращает утечку кислоты и коррозию клемм.
- Более безопасная работа: при правильной зарядке батарей исключается возможность выделения газов и опасность взрыва.
- Герметичная конструкция позволяет устанавливать батарею почти в любом положении (однако установка вверх дном не рекомендуется).
- Уверенная работа при низких температурах (ниже − 40*С), низкий саморазряд (всего на 15 — 20% за год простоя), полная необслуживаемость и долгий, до 12 — 15 лет, срок службы.
- Повышенная виброустойчивость увеличивает срок службы.
- Они обеспечивают число полных (70%) циклов разряда около 500 раз.
Недостатки:
- Не должны храниться в разряженном состоянии, напряжение не должно упасть ниже 10,8 В.
Крайне чувствительны к превышению напряжения заряда.
Для заряда батарей изготовленных по технологии AGM, желательно использовать специальное зарядное устройство с соответствующими параметрами заряда, отличными от заряда классических аккумуляторов с жидким электролитом. AGM-батареи не такие «капризные» как гелевые, но тоже требуют внимания к состоянию генератора и реле-регулятора. Дело в том, что в аккумуляторах этого типа конструктивно очень мало электролита, и если он выкипит, то долить невозможно. - Высокая цена.
Аккумуляторы, производимые с использованием технологии AGM, изготавливаются в спиральной или плоской конфигурации. Спиральные элементы обладают большей площадью поверхностного контакта, что даёт возможность кратковременно выдавать большие токи и быстрее заряжаться. Однако обратной стороной является уменьшение удельной ёмкости аккумулятора (соотношение электрической ёмкости и размеров) по сравнению с плоской конфигурацией. Обе технологии являются перспективными. В настоящий момент наиболее распространены автомобильные аккумуляторы AGM с плоской конфигурацией блоков. Спиральные блоки SpiraCell запатентованы компанией Johnson Controls для серии Optima и не могут использоваться без её разрешения, в отличие от плоских блоков. У спиральных батарей выше характеристики токоотдачи и меньшее внутреннее сопротивление из-за большей рабочей поверхности пластин при тех же внешних габаритах батареи. Простым языком говоря, они мощнее.
Свинцовые аккумуляторы со связанным электролитом, изготовленные по технологии AGM, появились около 40 лет назад — их изобрели для работы в буферном режиме в стационарных системах бесперебойного электроснабжения. Такие батареи хороши с точки зрения безопасности, поскольку практически не выделяют в атмосферу образующиеся при зарядке газы. В 90-х годах прошлого века технология AGM прижилась в автоспорте. Во-первых, вновь из-за безопасности — теперь уже благодаря полностью герметичному корпусу аккумулятора, исключающему вытекание электролита при аварии. А во-вторых, из-за компактности — благодаря малому сопротивлению не изолирующих, а пропитанных электролитом сепараторов большой пусковой ток они выдают при меньшей емкости, то есть с меньшим количеством пластин в пакете. На обычных автомобилях AGM-аккумуляторы появились больше десяти лет назад. В настоящий момент автомобильные стартерные батареи AGM используются в качестве источника питания системы «Старт-Стоп», которой оснащается ряд моделей автомобилей ведущих производителей из-за возможности быстро и отдавать, и принимать большое количество энергии, способности безболезненно выдерживать глубокие разряды (при периодических разрядах больше 50% АGМ — батарея прослужит вчетверо дольше обычной) и не деградировать при частых циклах разрядов-зарядов. Ведь стекловолоконные маты вдобавок ко всему механически удерживают активную массу на пластинах, не давая ей осыпаться. Именно поэтому на машинах с системой «Старт-Стоп» подобный аккумулятор способен проработать четыре-пять лет, а не два-три года, как обычный «жидкий».
Ещё почитать:
Гель или AGM?Аккумуляторы GEL, AGM и особенности их обслуживания
Вопрос-ответ
Сергей, 08.03.2017
Доброго времени.хотел узнать. Аккумулятор са/са если заряжать меньше чем 16,2 вольта,что случится? У меня зарядник выдаёт 14.8. СПС
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Сергей, благодарим Вас за обращение.
Критерием окончания заряда является достижение плотности электролита 1.27 г/см3 во всех банках, при невозможности контроля плотности, окончанием заряда можно считать падение зарядного тока до 0,5-1А и (либо) его стабилизация в течении 2-х часов.
Рекомендуем
производить заряд в соответствии с инструкцией по эксплуатации, с
выставлением зарядного тока в ручную с величиной 5% от ёмкости АКБ (в
Вашем случае 3А). При таком методе заряда ЗУ автоматически будет
повышать зарядное напряжение при падении тока (приём заряда), достигая
порога в 16В по окончанию заряда. В случае невозможности ЗУ повысить
значение напряжения до 16В, плотность не достигнет значения в 1.27
г/см3, соответственно степень заряженности не будет полной
Александр, 27.01.2017
Доброго времени суток! Приобрел АКБ АКОМ «ULTIMATUM» 60 Ач. А/м Лада Приора, эксплуатируется редко, выезжаю на небольшие расстояния 1-2 раза в неделю. Интересует следующий вопрос: Нужно ли заряжать новый АКБ, если да то, каким током в амперах и как долго по времени. Заранее спасибо за ответ.
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Александр, благодарим Вас за обращение.
Необходимость в заряде батареи заключается в её текущем состоянии, а именно в степени заряженности, которую можно определить несколькими способами. Самый простой способ это показания индикатора степени заряженности, который встроен в крышку аккумуляторной батареи, если цвет индикатора зелёный, значит степень заряженности достаточная для полноценной работы, если чёрный — батарею необходимо дозарядить.
Следующий способ требует наличия оборудования, такого как вольтметр и ареометр. При помощи вольтметра необходимо замерить НРЦ (напряжение разомкнутой цепи) на полюсных выводах АКБ без подключенной нагрузки.
Напряжение в 12,8-12,9В означает, что батарея заряжена на 100%, для Вашего удобства таблица степени заряженности находится во вложении к данному письму. Также степень заряженности можно определить по плотности электролита при помощи ареометра.
Рекомендации по заряду аккумуляторной батареи Вы можете найти в инструкции по эксплуатации или на официальном сайте нашей компании по адресу: http://www.akom.su/support/articles/calcium_battery/
Обратите
внимание на то, что зарядное устройство должно быть способно выдавать
напряжение в 16,2В.
Михаил, 23.12.2016
АКБ Аком EFB 60ач, плотность 12,3. ранее было ЗУ, которое не давало больше 14,2. Приобрел Вымпел-55, использую 1 алгоритм, ток 6а,
напряжение выставил 15,9, не смотря на то, что на сайте у Вас рекомендуется 16+. Со старта Напряжение уже практически на выставленном уровне, а снижаются амперы. Но вот только всё это дело немного побулькивает, и спустя несколько часов в таком режиме, электролит стал мутнее, цвет не поменял, просто мутнее, пластины плохо видно. Это нормально? И нормально ли то, что уже со старта ЗУ выдает заданное напряжение, и уменьшаются только амперы, показателем завершения будут упавшие амперы?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Мы не готовы комментировать работу зарядных устройств сторонних производителей без проведения предварительных испытаний. Рекомендуем к применению фирменное зарядное устройство «АКОМ»
Аккумуляторные батареи, изготовленные по технологии EFB (Enhanced Flooded Battery) — это улучшенные аккумуляторные батареи с жидким электролитом, специально разработанные для эксплуатации в условиях нагрузок, связанных с постоянно повторяющимися циклами заряда и разряда. За счёт применения целого ряда конструктивных изменений увеличивается срок службы АКБ и расширяется применяемость.
Исходя из того, что данная батарея конструктивно схожа с батареями изготовленными по технологии Ca/Ca (кальций-кальций), методики заряда данных батарей идентичны. Описание процесса заряда указано в п.2.2. инструкции по эксплуатации АКБ (для Вашего удобства инструкция во вложении).
Обращаем особое внимание на то, что для эффективной и полной зарядки АКБ, изготовленных по технологии Ca/Cа, зарядное устройство должно обеспечивать зарядное напряжение 16,2В.
«Кипение» электролита (выделение пузырьков газа) — естественный процесс, возникающий в момент приближения напряжения к значению в 16В на клеммах батареи при заряде. Является признаком того, что степень заряженности АКБ приближается к максимальному значению. Критерием окончания заряда является достижение плотности электролита 1.27 г/см3 во всех банках, при невозможности контроля плотности, окончанием заряда можно считать падение зарядного тока до 0,5-1А и (либо) его стабилизация в течении 2-х часов.
Рекомендуем производить заряд
в соответствии с инструкцией по эксплуатации, с выставлением зарядного
тока в ручную. При таком методе заряда ЗУ автоматически будет повышать
зарядное напряжение при падении тока (приём заряда), достигая порога в
16В по окончанию заряда.
Максим, 20.12.2016
Планирую приобретение аккумулятора для легкового а/м иностранного производства. На подсознательном уровне имею желание поддержать
отечественного производителя и соответственно приобрести ваш аккумулятор. Но непонятно одно, чем ваш аккумулятор лучше аккумуляторов иностранного производства, при том, что максимальная разница в цене на аналогичные модели всего 500 р., а на некоторые марки и вообще разницы в цене нет. Почему люди должны брать ваш аккумулятор по той же цене, что и импортный, если иностранные производители уже давно зарекомендовали себя хорошим качеством.
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Интеграция в мировую автомобильную индустрию требует поддержания высокого уровня качества и конкурентоспособности продукции. На аккумуляторном производстве «АКОМ» эта задача решается путем постоянного развития производства, совершенствования конструкции и технологий, внедрения международных стандартов качества, системы LEAN Production.
Система менеджмента качества АО «АКОМ» сертифицирована на соответствие стандартам ISO 9001-2008, ISO TS 16949-2009. Отклонение по качеству невозможно, т.к. в технологический процесс изготовления аккумуляторных батарей включены посты контроля ключевых параметров, определяющих электрические характеристики батареи. Их уникальность — автоматическая отбраковка продукции, не соответствующей установленным техническим требованиям.
АКОМ — высокотехнологичное предприятие с уникальной многоступенчатой системой контроля качества выпускаемой продукции. Высокое качество продукции является фундаментальной основой нашего бизнеса. Каждый покупатель, приобретая аккумуляторную батарею нашего производства, получает гарантию от производителя и может рассчитывать на квалифицированное гарантийное и послегарантийное обслуживание, получая при этом уверенность в надёжной работе всех потребителей в автономном режиме, а также в гарантированном запуске двигателя автомобиля.
Исходя из того, что вся продукция АО «АКОМ» полностью соответствует заявленным характеристикам, обладает высоким качеством и уровнем сервиса, она априори не может быть дешевой.
Рекомендуем ознакомиться с презентационным фильмом о Группе Компаний АКОМ.
Ильназ, 18.11.2016
Подскажите, пожалуйста, по какой технологии (Ca/Ca и т.д.) изготовлен аккумулятор, устанавливаемый на автомобили LADA Vesta 2016 года? На моей есть лишь обозначения «6CT-62VL Евро», изготовлен 4 апреля 2016 года сменой «С».
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Согласно
нормативной документации, батарея 6СТ-62VL Евро по
конструкторско-технологическому исполнению относится к классу батарей
очень малым (VL) расходом воды, изготавливается по технологии Ca\Ca
(Кальций-Кальций), одним из преимуществ которой является сокращение
потери воды из электролита во время эксплуатации, что в свою очередь
значительно снижает объём обслуживания и повышает уровень безопасности.
Для удобства обслуживания (контроль уровня и плотности электролита),
батарея оснащена заливными отверстиями с пробками.
Алексей, 16.11.2016
Здравствуйте замечательная компания АКОМ! Скажите пожалуйста какие модели аккумуляторов являются обслуживаемыми а какие не обслуживаемые? Для меня это важно знать т.к. я их продаю. Не могу данной корректной информации найти в источнике. Заранее спасибо.
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Согласно нормативной документации, батареи легковой группы с ёмкостью от 40Ач до 100Ач, произведённые на аккумуляторном производстве АО «АКОМ», по конструкторско-технологическому исполнению относятся к классу батарей очень малым (VL) расходом воды, изготавливаются по технологии Ca\Ca (Кальций-Кальций), оснащаются крышкой особой конструкции с лабиринтной системой газоотвода для сокращения потери воды из электролита во время эксплуатации, что в свою очередь значительно снижает объём обслуживания и повышает уровень безопасности. Для удобства обслуживания (контроль уровня и плотности электролита), все производственные линейки АКБ оснащены заливными отверстиями с пробками. Тяжелая группа батарей с ёмкостью от 140Ач до 225Ач по конструкторско-технологическому исполнению относятся к классу батарей малым (L) расходом воды и так же являются обслуживаемыми. Вышеперечисленные батареи относятся к свинцово-кислотным аккумуляторам с жидким электролитом, понятие обслуживания заключается в контроле расхода воды из электролита и при необходимости добавлении дистиллированной воды. Величина расхода воды зависит от применяемой технологии и особенностей конструкции. Любая батарея с жидким электролитом является обслуживаемой.
Так называемые
необслуживаемые батареи — это батареи не имеющие свободного электролита.
Электролит в таких батареях находится во связанном состоянии. Одной из
технологий производства таких батарей является технология GEL (Gelled
Electrolite) с гелеобразным электролитом. Так же на рынке представлены
батареи AGM (Absorptive Glass Mat ), в которых такой элемент
конструкции, как сепаратор изготовлен из стекловолокна. При
использовании такого материала нет нужды превращать электролит в гель,
весь электролит впитывается стекловолоконным сепаратором, и надежно в
нем удерживается. Обе технологии подразумевают наличие герметизированной
конструкции моноблока без доступа во внутрь. Необслуживаемые —
означает, что в АКБ этого вида не требуется следить за уровнем
электролита и доливать воду.
Евгений, 15.10.2016
Здравствуйте, у вас на сайте есть статья про зарядку кальциевого АКБ. там сказано что нужно 16В. У меня Лада Приора и стоит ваша батарея. Напряжение заряда в Приоре менее 16В. Получается она всегда недозаряжается?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Евгений, благодарим Вас за обращение.
Рекомендуем Вам заряжать аккумуляторную батарею на стационарном зарядном устройстве постоянным током 0,1 от её емкости до напряжения 14,4В, а когда значение тока упадет до 1-1,5 ампера продолжить зарядку таким током до достижения значений напряжения в 16,5В. Именно поэтому мы рекомендуем зарядное устройство, способное выдать напряжение 16,25-16,5В.
Маленький совет. Заряжать током 0,1С20 можно только при комнатной температуре и никогда не стремиться заряжать аккумулятор до 100%, т.к. такие заряды значительно изнашивают активные массы аккумуляторных пластин. После установки батареи на автомобиль степень заряженности фактически за один день упадет до 80%, это абсолютная норма.
Напряжение АКБ, установленной на автомобиль должно находиться в пределах 12,4-12,8В. Замерять не раньше 3-х часов после того, как двигатель будет заглушен.
Для того чтобы обеспечить нормальный заряд аккумуляторной батареи, изготовленной по технологии Са/Са, каковыми и являются наши АКБ, напряжение в бортовой цепи автомобиля зимой должно быть 14,5В, летом 14,2В. Если данное условие будет соблюдено, Вы не должны иметь проблем с исправной аккумуляторной батареей.
Очень важно в зимнее время ежедневно эксплуатировать автомобиль при времени одной поездки не менее 30 минут, этого достаточно для подогрева подкапотного пространства автомобиля и возвращения в АКБ израсходованного заряда на запуск двигателя и при стоянке. Разряд происходит за счет естественных токов утечки в бортовых системах автомобиля не отключаемых при вынутом ключе зажигания.
Надеемся на Ваше понимание вышеизложенного.
Желаем
удачи на дорогах!
Алексей, 24.09.2016
Доброго времени суток! У меня стоит АКБ 90 А/ч машина работает на ДТ специалисты замеряли пусковой ток и говорят, что он низкий, пробывал заряжал АКБ, плотность во всех банках 1,25 в связи с этим вопрос есть ли возможность поднять пусковой ток? За ранее спасибо с Уважением Алексей
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Алексей, благодарим Вас за обращение.
В соответствии с ГОСТ Р 53165-2008 «БАТАРЕИ АККУМУЛЯТОРНЫЕ СВИНЦОВЫЕ СТАРТЕРНЫЕ ДЛЯ АВТОТРАКТОРНОЙ ТЕХНИКИ»‘ и ТУ АКОМ 3481-001-57586209-2010 ток холодной прокрутки (Ix.n.) это ток разряда, указанный изготовителем, который может обеспечить батарея для пуска двигателя в заданных условиях. В соответствии с данными нормативными документами аккумуляторные батареи подвергаются испытанию на ток холодной прокрутки по строго определенной методике, обязательными условиями которой являются:
1) Проведение испытаний на батареях, с момента изготовления которых прошло не более 30 дней;
2) Предварительное испытание на номинальную или резервную емкость перед испытанием на ток холодной прокрутки;
3) Полный заряд аккумуляторной батареи после испытания на номинальную или резервную емкость в соответствии с методикой, определенной в этих же документах;
4) Проведение испытания на ток холодной прокрутки при температуре минус (18±1) °С;
5) Разряд аккумуляторной батареи при проведении данного испытания в две ступени: током Ix.n. на первой, и током 0.6 Iх.п. на второй ступени.
Также предусмотрено проведение трех циклов испытаний на номинальную или резервную емкость и ток холодной прокрутки. Результаты испытаний считаются положительными, если они достигнуты хотя бы на одном из трех циклов.
Любые иные методы
испытаний и проверок на ток холодной прокрутки аккумуляторных батарей
(в том числе на аккумуляторных батареях без предварительного заряда и с
помощью портативных тестеров, использующих расчетный метод для
определения величины тока холодной прокрутки) не соответствуют ГОСТ Р
53165-2008 и ТУ АКОМ 3481-001-57586209- 2010 и не могут являться
основанием для предъявления претензий заводу-изготовителю.
Алексей, 27.08.2016
Добрый день. Может ли «высохнуть» аккумулятор в летний период (до +35) с учетом эксплуатации в выходные (будни авто стоит на стоянке)?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Алексей, благодарим Вас за обращение.
Выкипание воды из электролита и, как следствие, снижение его уровня происходит под влиянием нескольких факторов, главными из которых являются применяемая технология изготовления АКБ, условия эксплуатации и температура.
В любом
случае, батарея, не находящаяся в эксплуатации, «выкипеть» не может.
Виктор, 23.07.2016
Добрый день, в марте 2016 купил Ниву Шевроле, стоит ваш штатный аккумулятор. При проверке: напряжение-12.50, плотность-1.21. Что делать?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Виктор, благодарим Вас за обращение.
В виду того, что аккумуляторная батарея была приобретена Вами в составе автомобиля, все гарантийные обязательства перед Вами несет производитель авто (ЗАО «Джи Эм-АВТОВАЗ») в лице своего дилера, у которого был приобретен автомобиль.
Рекомендуем Вам ознакомиться с условиями предоставления гарантии на АКБ в сервисной книге. Если Ваш автомобиль находится в гарантийном периоде — обратитесь к дилеру для проведения диагностики АКБ и автомобиля.
Претензии к АКБ не удовлетворяются в случае если плотность электролита ниже 1,2г/см3 во всех банках одновременно (не гарантийный случай).
Причина низкой
плотности — низкая степень заряженности, батарею необходимо зарядить.
Евгений Павлович, 30.06.2016
Здравствуйте. Аккумулятор «кальций-кальций» означает, что свинцовые пластины покрыты слоем кальция, или состоят из сплава вышеназванных металлов? А аргентум-кальций — это что, положительные пластины посеребрённые или….?? Что-то не понятно; ответе, пожалуйста, если знаете.
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Евгений Павлович, благодарим Вас за обращение.
Технология Ca/Ca предусматривает изготовление электродов (положительных и отрицательных) из свинцового сплава, легированного кальцием для достижения определённых задач, а именно: снижение расхода воды, снижение времени саморазряда, увеличения электрических характеристик и пр.
Основная цель легирования электродов серебром это снижение влияния коррозии.
Сергей, 13.03.2016
Здравствуйте! Допускается ли использование аккумулятора Аком Reactor Са-Са 62 Ач в дежурном режиме, т.е. аккумулятор постоянно находится под напряжением 13.6В. Я использую такой режим в случае длительного простоя автомобиля а гараже, скажем 3..4 недели или вообще всю зиму. Какие есть рекомендации по этому поводу? Возможно ли использование Са-Са аккумулятора в источниках бесперебойного питания?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Сергей, благодарим Вас за обращение.
Хранить батарею под постоянным напряжением в 13,6В не имеет никакого смысла. Достаточно зарядить её до 100% степени заряженности и оставить на хранение, периодически (раз в 2 месяца) проверяя степень заряженности и заряжать при необходимости.
Для работы в ИБП стартерные аккумуляторные батареи не подходят,
т.к. их основная задача — кратковременная отдача высокой мощности, для
ИБП необходимы тяговые батареи, работа которых заключается в длительном
режиме разряда.
Михаил, 11.01.2016
Лада Калина Хэтчбек 1,6 8кл 2012г. штатный аккумулятор на 55а/ч. возможна ли замена на Akom Reactor 55а/ч 550а/ч. Какие еще возможны замены, без ущерба генератора.
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Михаил, благодарим Вас за обращение.
Замена штатной АКБ 6СТ-55VL АКОМ Стандарт на батарею 6СТ-55VL REACTOR возможна без негативного влияния на штатное оборудование автомобиля. В случае, если Вы оснащали автомобиль дополнительным электрооборудованием, рекомендуем батарею 6СТ-65VL АКОМ, либо 6СТ-62VL REACTOR.
Нагрузка на генератор не зависит от повышения ёмкости АКБ, следите за
напряжением заряда, которое должно быть в диапазоне от 13,8В до 14,5В.
Антон, 28.12.2015
Добрый день у меня аккумулятор АКОМ REACTOR 750, морозы у нас бывают лютые. Сегодня аккумулятору исполнилось 2 года. За его состоянием следил диллер которому я доверя — и как оказалось зря. Так как они совсем не смотрели и не обслуживали его. Недавно при маленьком морозе у меня не завелся автомобиль. Замеры показали плотность 1.170-1.190 во всехбанках. После длительной зарядке (2 суток) напряжение дошло до 14.7 и сила тока опустилась до 0 ампер (изначально было 3 ампера) вобщем плотность поднялась до 1.220-1.240. Что мало для крайнего севера/ .
Вопроса два:
1) при каком напряжении заряжать аккумулятор (гдето читал что кальциевые нужно заряжать при 15-16)? или я заряжал правильно?
2) как поднять плотность аккумулятора правильно до 1.27 -1.28
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Антон, благодарим Вас за обращение.
Вы совершенно правы, для полного заряда аккумуляторной батареи, изготовленной по технологии кальций-кальций, необходимо напряжение в 16,2В.
Заряд АКБ необходимо проводить при температуре электролита более 0ºС.
Перед началом зарядки необходимо выкрутить заливные пробки и оставить их в посадочных гнездах крышки. По окончанию заряда, прежде чем завернуть пробки, необходимо извлечь их из заливных отверстий для выхода скопившихся газов и выдержать в таком состоянии батарею не менее 20 минут. Во время заряда периодически проверяйте температуру электролита и следите за тем, чтобы она не поднималась выше 45ºС. Начинать заряд рекомендуется током не более 5% от номинальной емкости в течении двух часов, с последующим повышением тока зарядки до 10% от номинальной емкости. Для эффективной и полной зарядки АКБ зарядное устройство должно обеспечивать зарядное напряжение 16,0 В. Критерием окончания заряда является достижение плотности 1.27 г/см3, при невозможности контроля плотности, окончанием заряда можно считать падение зарядного тока до 0,5-1А и его стабилизация в течении 2-х часов.
При заряде выделяется взрывоопасный газ! Помещение, где ведется зарядка должно быть оборудовано приточно-вытяжной вентиляцией или проветриваться, в нем запрещается курить и пользоваться открытым пламенем!
Для проверки напряжения разомкнутой цепи АКБ после заряда
необходимо выключить зарядное устройство, отсоединить наконечники
проводов зарядного устройства от полюсных выводов АКБ, выдержать АКБ не
менее 8 часов при комнатной температуре и затем провести замер.
Булат, 19.12.2015
Добрый день.
На Ладе Приоре стоит штатный акк. АКОМ 55 VL, однако он стал плохо держать заряд (4 года эксплуатации), поэтому планирую поменять на новый и хочу приобрести АКОМ Браво 60 VL. Допускается ли подобная замена? Не будет ли новый аккумулятор ездить недозаряженным?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Булат, благодарим Вас за обращение.
В качестве замены штатной аккумуляторной батареи, рекомендуем Вам АКБ АКОМ 55Ач, либо 60Ач.
Но в случае, даже если Вы приобретёте АКБ BRAVO 60Ач, такого явления как недозаряд возникать не будет, при условии исправности системы заряда АКБ и отсутствии высоких токов утечки (свыше 30-50мА).
Константин, 25.11.2015
Добрый день,аккумулятор аком 65ач ca/ca.В первой и в посл. банке плотность электролита 1.25 и выше не поднимается!В остальных банках во 2,3,4,5 плотность 1.27!Заряжал током 1а и напряж 15в. 24часа. плотность в крайних банках не поднялась выше 1.25!Подскажите как выравнять плотность и поможет ли зарядка 16вольтовым оборудованием?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Константин, благодарим Вас за обращение.
Если батарея не подвергалась глубокому разряду, не перезаряжалась
или долго не эксплуатировалась в недозаряженном состоянии (о чем можно
судить по оплыванию активной массы и цвете электролита) и все банки
кипят при заряде, то все должно быть нормально. Если есть отличие в
уровне электролита, то в показаниях плотности может быть разница. Если
есть возможность, конечно необходимо применить ЗУ, которое способно
выдавать 16В. Для батарей, изготовленных по кальциевой технологии это
идеальный вариант. Продолжайте заряд с напряжением в 16В, плотность
должна выровняться.
Рамиль, 14.10.2015
Разрешается ли путем смешивания электролита в разных банках, выравнивать плотность в банках?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Рамиль, необходимо уточнить какой именно электролит Вы используете и в каких целях, нельзя заливать электролит при потере уровня из-за выкипания воды, в этом случае доливается только дистиллированная вода.
Также не рекомендуем использовать электролит сторонних производителей, т.к. его компоненты (присадки) отличаются.
Игорь, 20.08.2015
Что за аккумулятор Аком ставят на конвейере на Ладу Ларгус?
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Игорь, благодарим Вас за обращение.
Автомобили Ларгус оснащались АКБ 6СТ-70VL (70Ач, 720А, формат L3,
обратная полярность) в период с мая 2014г по январь 2015г. С января
2015г по сегодняшний день данный автомобиль оснащается батареей 6СТ-64VL
(64Ач, 620А, формат L2, обратная полярность). Продукция произведена на
аккумуляторном производстве ЗАО «АКОМ» (г.Жигулёвск).
Сергей, 14.06.2015
Какой завод выпускает аккумуляторы марки Аком?
Евгений Смолькин, менеджер по интернет-маркетингу
Здравствуйте, Сергей. Производством АКБ «Аком» занимается ЗАО «АКОМ» г. Жигулевск
Петр, 12.05.2015
Добрый день!
Купил авто вместе с Вашим АКБ в 2008 г.
и…. вот спустя сколько времени он только начал плохо держать заряд.
Желаю Вам процветания и так же держать МАРКУ.
Геннадий Кольчугин, менеджер по гарантийному обслуживанию
Добрый день!
Пётр, благодарим Вас за тёплые слова в наш адрес.
Залогом безотказной работы аккумуляторной батареи является грамотная эксплуатация.
Надеемся, что и в будущем Вы отдадите предпочтение продукции ЗАО «АКОМ».
(PDF) Обнаружение низкого уровня электролита в свинцово-кислотных аккумуляторах с вентиляцией на основе электрических измерений
Энергия 2019,12, 4435 13 из 14
2.
Rand, D.A.J .; Moseley, P.T .; Garche, J .; Паркер, К. Свинцово-кислотные батареи с регулируемым клапаном; Elsevier Inc: San
Diego, CA, USA, 2004.
3. Справочник по батареям; McGraw Hill: New York, NY, USA, 2002.
4.
Karimi, M.A .; Karami, H .; Махдипур, М. Моделирование потребления воды в свинцово-кислотных аккумуляторах с помощью ИНС.
J. Источники энергии 2007, 172, 946–956. DOI: 10.1016 / j.jpowsour.2007.06.027.
5.
Руетски П. Механизмы старения и срок службы свинцово-кислотных аккумуляторов. J. Источники энергии
2004
, 127, 33–44.
DOI: 10.1016 / j.jpowsour.2003.09.052.
6.
Schulte, D .; Sauer, D.U .; Ebner, E .; Börger, A .; Gose, S .; Венцль, Х. «Индекс стратификации» — количественная оценка
кислотной стратификации в затопленных свинцово-кислотных батареях.J. Источники энергии
2014
, 269, 704–715.
DOI: 10.1016 / j.jpowsour.2014.06.155.
7.
Franke, M .; Коваль, Дж. Эмпирическая модель сульфатирования для свинцово-кислотных батарей с регулируемым клапаном при циклической работе
. J. Источники энергии 2018, 380, 76–82. DOI: 10.1016 / j.jpowsour.2018.01.053.
8.
Ouyang, M .; Чжан, М .; Feng, X .; Lu, L .; Li, J .; Он, X .; Чжэн, Ю. Обнаружение внутреннего короткого замыкания для аккумуляторной батареи
с использованием эквивалентных параметров и метода согласованности.J. Источники энергии
2015
, 294, 272–283.
DOI: 10.1016 / j.jpowsour.2015.06.087.
9.
Павлов, Д .; Петкова, Г .; Рогачев, Т. Влияние концентрации кислоты на характеристики отрицательных пластин свинцово-кислотных аккумуляторов
. J. Источники энергии 2008, 175, 586–594. DOI: 10.1016 / j.jpowsour.2007.09.015.
10.
Deveau, J .; Белый, C .; Свон, Л. Реакция свинцово-кислотной батареи на различные уровни пласта — Часть B: Внутреннее сопротивление
.Поддерживать. Energy Technol. Оценивать. 2015, 11, 126–133. DOI: 10.1016 / j.seta.2015.08.005.
11.
Brik, K .; Бен Аммар, Ф. Анализ трех неисправностей деградации свинцово-кислотных аккумуляторов. J. Electr. Syst.
2008
,
4, 504–511.
12. Bro, P .; Леви, S.C. Опасности, связанные с аккумулятором, и предотвращение несчастных случаев; Plenum Press: New York, NY, USA, 1994.
13.
Yahamadi, R .; Брик, К .; Бен Аммар, Ф. Эффекты режима отказа и анализ критичности процесса производства
свинцово-кислотных аккумуляторов.Int. J. Sci. Res. Англ. Technol. 2015,3, 6–11.
14.
IEEE-450. Рекомендуемая практика IEEE для обслуживания, тестирования и замены вентилируемых свинцово-кислотных батарей для стационарных приложений
; IEEE: Нью-Йорк, Нью-Йорк, США, 2011.
15.
IEEE-1188. Рекомендуемая практика IEEE для обслуживания, тестирования и замены свинцово-кислотных аккумуляторов с клапаном регулирования
(VRLA) для стационарных применений; IEEE: Нью-Йорк, Нью-Йорк, США, 2014.
16.
IEEE-1106. Рекомендуемая практика IEEE для установки, обслуживания, тестирования и замены вентилируемых никель-кадмиевых батарей
для стационарных применений; IEEE: Нью-Йорк, Нью-Йорк, США, 2015.
17.
UL-4128. Схема UL исследования межэлементных и межэлементных соединителей для использования в электрохимических аккумуляторных системах
Приложения; UL: Чикаго, Иллинойс, США, 2019.
18.
Standard PRC-005-2. Обслуживание системы защиты; North American Electric Reliability Corporation (NERC):
Атланта, Джорджия, США, 2014.
19.
Jones, D .; Уортингтон Дж. Система и метод контроля уровня электролита в батарее. Патент США
8928326, 5 января 2015 г. Доступно на сайте: http://scholar.google.com (по состоянию на 10 января 2019 г.).
20.
Herrema, M .; Earl, R.D .; Kloote, S .; Fox, J.L .; Shinew, M.T .; Мёлкер, Д.А. Датчик уровня жидкости для аккумуляторной батареи
Системы мониторинга. Патент США 20170279167, 28 сентября 2017 г. Доступно на сайте: http://patents.com
(по состоянию на 10 января 2019 г.).
21.
Jones, W.E.M .; Weidner, E.C. Монитор уровня электролита в аккумуляторной батарее. Патент США 005936382, 10 августа 1999 г.
Доступно на сайте: http://scholar.google.com (по состоянию на 10 января 2019 г.).
22.
Deveau, E.W .; Стюарт, Д .; Popken, D .; Мартинес Дж. Ультразвуковой датчик электролита. Патент США 9548520,
17 января 2017 г. Доступно на сайте: http://scholar.google.com (по состоянию на 10 января 2019 г.).
23.
Herrema, M .; Эрл, Р.D .; Kloote, D .; Фокс, Дж. Л. Интеллектуальные системы мониторинга для батарей с жидким электролитом.
Патент США 2019260090, 22 августа 2019 г. Доступно на сайте: https://worldwide.espacenet.com (доступ 1
сентября 2019 г.).
24.
Система CELLGUARD — решение для мониторинга батарей; Midtronics Inc: Уиллоубрук, Иллинойс, США, 2019; Доступно
онлайн: http://www.stationary-power.com/siteassets/products/cellguard (по состоянию на 10 января 2019 г.).
25.
Zou, Y.; Ху, X .; Ma, H .; Ли, С. Совместная оценка состояния заряда и состояния здоровья на протяжении
срока службы литий-ионных аккумуляторных элементов для электромобилей. J. Источники энергии
2015
, 273, 793–803.
DOI: 10.1016 / j.jpowsour.2014.09.146.
26.
Плетт, Г.Л. Системы управления батареями, Том II: Методы эквивалентной схемы; Artech House: Норвуд, Массачусетс,
США, 2016 г.
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с вашим системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файлах cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Концентрация электролита — обзор
2.3.4 Гидратация в концентрированных растворах
По мере увеличения концентрации электролита количество молекул воды во вторичной гидратной сфере уменьшается.Следовательно, происходит усиление связи между катионом металла и гидратными водами во внутренней сфере (Choppin, Jensen, 2006). Основываясь на исследованиях ЯМР трехвалентных актиноидов и лантаноидов, Чоппин пришел к выводу, что комплексообразование внутренней сферы перхлорат-ионами не происходит ниже примерно 8–10 М (Choppin, Labonne-Wall, 1997). Множественные равновесия для системы уранилхлорида (UO 2 Cl 2 (H 2 O) 2 , UO 2 Cl 3 (H 2 O) — и UO 2 Cl 4 2–) использовались для отделения урана от его дочерних продуктов или других металлов.Поскольку Th 4 + не образует анионных хлоридных комплексов, он остается на катионообменной смоле, в то время как анионные хлоридные комплексы UO 2 2 + проходят через колонку в элюате. Альтернативно такие анионные комплексы можно удерживать на анионообменной колонке.
Число гидратации Eu (III) остается относительно постоянным в соляной кислоте примерно до 6–8 M, выше которой концентрация уменьшается. То же самое верно и для числа гидратации Cm (III) в HCl, которое начинает снижаться примерно при 5 M HCl.Эта разница между (Eu 3 + и Cm 3 + ) отражает большее комплексообразование трехвалентного иона актинида с относительно мягким анионом Cl —. Разница в комплексообразовании хлоридов использовалась для обеспечения эффективного отделения трехвалентных актинидов от трехвалентных актинидов в концентрированных растворах HCl путем пропускания через колонки с катионообменной смолой с 1950-х годов (Diamond et al., 1954).
Нитратные комплексы для четырехвалентных актинидов, например Th 4 + и Pu 4 + , чрезвычайно важны в процессах разделения и очистки актинидов.Нитрат-ионы начинают образовывать комплексы внутренней сферы при более низких концентрациях, чем хлорид-анионы; это наблюдение подтверждается уменьшением числа гидратации катиона даже при относительно более низких концентрациях (Choppin, Jensen, 2006). Однако, поскольку атомы кислорода нитрата являются твердыми донорами, нет никаких доказательств какого-либо ковалентного усиления его связывания, как это видно с анионами хлорида для трехвалентных катионов актинидов по сравнению с катионами лантанидов (Choppin, Jensen, 2006). В процессах разделения и очистки чрезвычайно важны нитратные комплексы актинидов.Раствор нитрат-азотной кислоты является наиболее распространенной водной средой в процессах разделения ядер. В случае нейтральных экстрагентов, таких как трибутилфосфат (TBP), карбамоилметилфосфиноксид (CMPO) или дипиколинамиды (DPA), он обеспечивает нитратные единицы, необходимые для компенсации заряда катионов актинидов для обеспечения экстракции. Комплексообразование нитрата с шестивалентными ионами актинида происходит очень слабо, и определение констант образования для разновидностей водного раствора нитрата является чрезвычайно трудным.В водных условиях с высокими концентрациями азотной кислоты комплексы формы AnO 2 (NO 3 ) (H 2 O) x + , AnO 2 (NO 3 ) 2 (H 2 O) 2 и AnO 2 (NO 3 ) 3 — (An = U, Np, Pu). Лимитирующим веществом в ряду нитратов является гексанитрато-комплекс An (NO 3 ) 6 2– (Matonic et al., 2002). Известно комплексообразование пятивалентных ионов Pa и Np нитратом; однако доступны ограниченные термодинамические и структурные данные. Предполагаемая стехиометрия для разновидностей Np (V) — NpO 2 (NO 3 ) (H 2 O) x . Для протактиния, который легко гидролизуется, были предложены смешанные гидроксо / нитрато- или оксо / нитрато-комплексы.
Фториды и хлориды являются наиболее изученными актино-галогенидными системами, и они очень важны для процессов пирообработки и электрорафинирования.
Карбоновые кислоты прочно связаны с ионами актинидов. Первичный способ связывания простых карбоновых кислот — бидентатный, тогда как в комплексах поликарбоновых кислот карбоксилаты имеют тенденцию к монодентатной координации с ионом металла. Сродство низковалентных актиноидов к этим лигандам увеличивается с увеличением дентальности лиганда, например, этилендиаминтетраацетата (ЭДТА) >>> ацетата. Для An 4 + лиганд EDTA является гексадентатным с конформацией скручивания (спиральная конформация, охватывающая ион металла, а не инкапсулирующая ион металла в центральной полости, как триподальные или макробициклические лиганды).Диэтилентриамин-N, N, N ‘, N ″, N ″ -пентаацетат (DTPA) имеет еще более высокое сродство к ионам An 3 + и An 4 + .
Новая конструкция электролита может улучшить аккумуляторы для электромобилей
Новый электролит на основе лития, изобретенный учеными Стэнфордского университета, может проложить путь для следующего поколения электромобилей с батарейным питанием.
Обычный (прозрачный) электролит слева и новый электролит Стэнфордского стандарта справа.(Изображение предоставлено: Чжиао Юй)
В исследовании, опубликованном 22 июня в журнале Nature Energy , исследователи из Стэнфорда демонстрируют, как их новая конструкция электролита повышает производительность литий-металлических батарей — многообещающей технологии для питания электромобилей, ноутбуков и других устройств.
«Большинство электромобилей работают на литий-ионных батареях, которые быстро приближаются к своему теоретическому пределу по плотности энергии», — сказал соавтор исследования И Цуй, профессор материаловедения и инженерии, а также фотоники из Национальной ускорительной лаборатории SLAC.«Наше исследование было сосредоточено на литий-металлических батареях, которые легче литий-ионных батарей и потенциально могут обеспечивать больше энергии на единицу веса и объема».
Литий-ионный и металлический литий
Литий-ионные батареи, используемые во всем, от смартфонов до электромобилей, имеют два электрода — положительно заряженный катод, содержащий литий, и отрицательно заряженный анод, обычно сделанный из графита. Раствор электролита позволяет ионам лития перемещаться между анодом и катодом, когда батарея используется и когда она перезаряжается.
докторантов и ведущих авторов Хансен Ван (слева) и Чжиао Юй (справа) тестируют экспериментальную ячейку в своей лаборатории. (Изображение предоставлено: Hongxia Wang.)
Литий-металлический аккумулятор может содержать примерно в два раза больше электроэнергии на килограмм, чем современные литий-ионные аккумуляторы. Литий-металлические батареи делают это путем замены графитового анода металлическим литием, который может хранить значительно больше энергии.
«Литий-металлические батареи очень перспективны для электромобилей, где вес и объем имеют большое значение», — сказал соавтор исследования Женан Бао, специалист K.К. Ли Профессор инженерной школы. «Но во время работы анод из металлического лития вступает в реакцию с жидким электролитом. Это вызывает рост микроструктур лития, называемых дендритами, на поверхности анода, что может привести к возгоранию батареи и ее выходу из строя ».
Исследователи потратили десятилетия, пытаясь решить проблему дендритов.
«Электролит был ахиллесовой пятой литий-металлических батарей», — сказал соавтор исследования Чжао Юй, аспирант по химии.«В нашем исследовании мы используем органическую химию для рационального проектирования и создания новых стабильных электролитов для этих батарей».
Электролит новый
Для исследования Ю и его коллеги выяснили, могут ли они решить проблемы стабильности с помощью обычного, коммерчески доступного жидкого электролита.
«Мы предположили, что добавление атомов фтора к молекуле электролита сделает жидкость более стабильной», — сказал Ю. «Фтор — широко используемый элемент в электролитах литиевых батарей.Мы использовали его способность притягивать электроны, чтобы создать новую молекулу, которая позволяет аноду из металлического лития хорошо функционировать в электролите ».
В результате получилось новое синтетическое соединение, сокращенно FDMB, которое можно легко производить в больших объемах.
«Конструкции электролитов становятся очень экзотичными, — сказал Бао. «Некоторые из них оказались многообещающими, но их производство очень дорогое. Молекула FDMB, которую придумал Чжиао, легко производить в больших количествах и довольно дешево ».
«Невероятная производительность»
Команда Стэнфорда провела испытания нового электролита в литий-металлической батарее.
Результаты были впечатляющими. Экспериментальная батарея сохранила 90 процентов своего первоначального заряда после 420 циклов зарядки и разрядки. В лабораториях типичные литий-металлические батареи перестают работать примерно через 30 циклов.
Исследователи также измерили, насколько эффективно ионы лития переносятся между анодом и катодом во время зарядки и разрядки, это свойство известно как «кулоновская эффективность».
«Если вы зарядите 1000 ионов лития, сколько вы получите обратно после разрядки?» — сказал Цуй.«В идеале вы хотите 1000 из 1000 для 100-процентного кулоновского КПД. Чтобы быть коммерчески жизнеспособным, элемент батареи должен иметь кулоновскую эффективность не менее 99,9 процента. В нашем исследовании мы получили 99,52 процента в половинных ячейках и 99,98 процентов в полных ячейках; невероятная производительность ».
Батарея безанодная
Для потенциального использования в бытовой электронике команда Стэнфорда также провела испытания электролита FDMB в безанодных литий-металлических ячейках — коммерчески доступных батареях с катодами, которые подают литий на анод.
«Идея состоит в том, чтобы использовать литий только на катодной стороне, чтобы уменьшить вес», — сказал соавтор исследования Хансен Ван, аспирант в области материаловедения и инженерии. «Безанодная батарея проработала 100 циклов, прежде чем ее емкость упала до 80 процентов — не так хорошо, как эквивалентная литий-ионная батарея, которая может выдерживать от 500 до 1000 циклов, но все же одна из самых эффективных безанодных ячеек».
«Эти результаты показывают многообещающие результаты для широкого диапазона устройств», — добавил Бао. «Легкие безанодные батареи станут привлекательным элементом для дронов и многих других видов бытовой электроники.”
Аккумулятор 500
Министерство энергетики США (DOE) финансирует большой исследовательский консорциум под названием Battery500, чтобы сделать литий-металлические батареи жизнеспособными, что позволит производителям автомобилей создавать более легкие электромобили, способные преодолевать гораздо большие расстояния между зарядками. Это исследование было частично поддержано грантом консорциума, в который входят Стэнфорд и SLAC.
За счет улучшения анодов, электролитов и других компонентов Battery500 стремится почти в три раза увеличить количество электроэнергии, которое может выдать литий-металлическая батарея, с примерно 180 ватт-часов на килограмм, когда программа стартовала в 2016 году, до 500 ватт-часов на килограмм.Более высокое отношение энергии к весу, или «удельная энергия», является ключом к решению проблемы запаса хода, которую часто испытывают потенциальные покупатели электромобилей.
Перейдите на веб-сайт для просмотра видео.
Чжиао Юй
Испытание на воспламеняемость обычного карбонатного электролита (слева) и нового электролита FDMB (справа), разработанных в Стэнфорде. Обычный карбонатный электролит воспламеняется сразу после прикосновения к пламени, но электролит FDMB может выдерживать прямое пламя в течение как минимум трех секунд.
«Безанодная батарея в нашей лаборатории достигла уровня около 325 ватт-часов на килограмм удельной энергии, что является приличным числом», — сказал Цуй. «Нашим следующим шагом могла бы стать совместная работа с другими исследователями Battery500 над созданием ячеек, которые приблизятся к цели консорциума — 500 ватт-часов на килограмм».
Помимо более длительного срока службы и лучшей стабильности, электролит FDMB также гораздо менее воспламеняем, чем обычные электролиты, как исследователи продемонстрировали в этом встроенном видео.
«Наше исследование в основном обеспечивает принцип конструкции, который люди могут применять для создания более качественных электролитов», — добавил Бао. «Мы только что показали один пример, но есть много других возможностей».
Среди других соавторов Стэнфордского университета Цзянь Цинь, доцент кафедры химического машиностроения; докторанты Сянь Конг, Кеченг Ван, Вэньсяо Хуанг, Снехашис Чоудхури и Чибуезе Аманчукву; аспиранты Уильям Хуанг, Ючи Цао, Дэвид Маканич, Ю Чжэн и Саманта Хунг; и студенты Ютинг Ма и Эдер Ломели.Синьчан Ван из Университета Сямэнь также является соавтором. Чжэнань Бао и И Цуй — старшие научные сотрудники Стэнфордского института энергетики «Прекурт». Цуй также является ведущим исследователем Стэнфордского института материаловедения и энергетики, совместной исследовательской программы SLAC / Стэнфордского университета.
Эта работа также была поддержана Программой исследования материалов для аккумуляторов в Департаменте автомобильных технологий Министерства энергетики США. Средство, используемое в Стэнфорде, поддерживается Национальным научным фондом.
Чтобы читать все статьи о Стэнфордской науке, подпишитесь на еженедельный выпуск Stanford Science Digest .
Монитор и датчик уровня электролита в батарее
Технические характеристики
| Типы батарей | Совместимы со всеми типами прозрачных заливных батарей |
|---|---|
| Активация сигнала тревоги температуры | 35 ° C (95 ° F), ± 2 ° C (3,5 ° F) 49 ° C (120 ° F), ± 2 ° C (3,5 ° F) 63 ° C (145 ° F), ± 2 ° C (3,5 ° F) Дополнительно: нет сигнала тревоги по температуре |
| Точность уровня | ± 2 мм (± 0.08 ”) над или под меткой линии |
| Входное напряжение | 12 В пост. Обнаружение низкого уровня электролита 1+ Обнаружение низкого уровня электролита 4+ Обнаружение высокой температуры 1+ Обнаружение высокой температуры 4+ |
| Размеры: (Д x Ш x Г) | Монитор: 176 x 80 x 51 мм (6.9 x 1,6 x 3 дюйма) Сенсор: 54 x 35 x 15 мм (2,2 x 1,4 x 0,8 дюйма) База сенсора: 65 x 52 x 14 мм (2,6 x 2,1 x 0,6 дюйма) Кабели: 1,25 мм шаг при длине 305 мм (12 дюймов) |
| Вес | Монитор ELM: 210 г (7,41 унции) |
Часто задаваемые вопросы
Как ELM контролирует температуру?
Датчик уровня электролита использует высокочувствительную температурную ИС, установленную в корпусе.
Как ELM контролирует электролит аккумулятора?
Инфракрасный.
Какая очистка аккумуляторных элементов требуется перед установкой системы ELM?
Каждый комплект ELM включает (1) рулон чистящих полотенец и (1) банку CRC PF Precision Cleaner. Очень важно очищать ячейки с помощью прилагаемого набора для очистки, чтобы датчики не упали с ячеек. Одно чистящее полотенце следует использовать для очистки не более (4) ячеек, а один баллончик с чистящим спреем подходит для 240 ячеек.
Имеется ли звуковая сигнализация для ELM?
ELM не имеет звуковой сигнализации, но можно использовать внешний.Контакты на выходах предупреждений полностью изолированы друг от друга и цепей датчиков, поэтому вы можете управлять с ними любой цепью, световыми сигналами, звуковыми сигналами, двигателями, насосами и т. Д. Контакты рассчитаны на 15 ампер при 125 В переменного тока или 10 ампер при 277 В переменного тока. Между контактами и катушкой имеется номинальное напряжение 2 кВ (катушка подключена к цепям датчиков).
Как сбрасываются аварийные сигналы уровня электролита и температуры?
Аварийный сигнал уровня электролита срабатывает, если низкий уровень электролита обнаруживается в течение более 40 минут (для предотвращения самопроизвольного срабатывания сигнала тревоги).Когда сигнал уровня активен, он будет оставаться таковым до тех пор, пока уровень электролита не будет восстановлен и кнопка R / S не будет нажата вручную на датчике. Температурный аварийный сигнал возникает, как только будет определена пороговая температура, он автоматически сбрасывается через 4 минуты.
Каковы рекомендации по установке датчика?
Датчик уровня электролита должен быть установлен вертикально в вертикальном положении. Он должен располагаться на поверхности банки так, чтобы линия «уровня» на датчике совпадала с линией «минимума» на банке.
Каковы минимальные зазоры вокруг датчиков на аккумуляторе?
Зазоры основаны на расстоянии выше и ниже «минимальной» линии на батарейном отсеке. Рамку датчика можно снять, чтобы уменьшить необходимые зазоры. Минимальная высота без рамки: 29 мм (1 1/8 дюйма) Типичная высота с рамой: 35 мм (1 3/8 дюйма) Минимальная глубина: 32 мм (1 1/4 дюйма).
Какова максимальная длина кабеля от монитора до датчиков?
Наибольшая длина кабеля от монитора датчика не должна превышать 300 футов (91 м).Как всегда, необходимо подключить полный контур от монитора к датчикам и обратно, чтобы избежать падения напряжения в системе.
Приведет ли клейкая лента, используемая для крепления датчика, к повреждению аккумуляторной батареи?
Клейкая лента на датчиках и подставках была тщательно протестирована и не повредит аккумуляторную батарею.
Какая потребляемая мощность у ELM?
Потребляемая мощность зависит от количества подключенных датчиков и количества обнаруженных неисправностей.Монитор потребляет 0,36 Вт; один датчик без сбоев потребляет 0,024 Вт. Общая потребляемая мощность для общих конфигураций системы без сбоев будет:
- 60-элементная система: 0,36 Вт + (60 * 0,024) = 1,44 Вт
- 120-элементная система: 0,36 Вт + (120 * 0,024) = 2,88 W
- 240-элементная система: 0,36 Вт + (240 * 0,024) = 5,76 Вт
Пиковая потребляемая мощность при 4+ сбоях уровня и температуры увеличит монитор до 1,44 Вт:
- 60-элементная система: 1 .44 Вт + (60 * 0,024) = 2,88 Вт макс.
- 120-элементная система: 1,44 Вт + (120 * 0,024) = 4,32 Вт макс.
- 240-элементная система: 1,44 Вт + (240 * 0,024) = 7,2 Вт макс.
Какая потребляемая мощность на датчик?
Один монитор и один датчик потребуют не более 0,1 ампер при 12 вольт.
Обучение работе с продуктом
Если вы хотите пройти обучение по конкретному продукту, свяжитесь напрямую с Eagle Eye. Мы предлагаем бесплатное обучение по телефону. Расценки могут быть предоставлены для обучения продукту на месте.Для получения дополнительной информации позвоните по телефону 1-877-805-3377 или напишите нам по адресу [email protected]. Оказываем своевременную поддержку по всем запросам.
Учебные курсы EEU
Eagle Eye University (EEU) предлагает запланированные курсы, адаптированные к конкретным аспектам критически важной электроэнергетики. Все курсы также доступны в вашем регионе. Следующие курсы применимы к мониторингу уровня электролита.
Аккумулятор 101
2 марта 2020 г. — 3 марта 2020 г.Исчерпывающий обзор типов аккумуляторов и их использования в приложениях резервного питания
Высокопроизводительный водный натрий-ионный аккумулятор с гибридным электролитом с широким диапазоном электрохимической стабильности
Практическое применение водных натрий-ионных батарей (ASIB) ограничено электролизом воды, что приводит к низкому рабочему напряжению и плотности энергии ASIB.В данном случае гибридный электролит ацетонитрил / вода на основе NaClO 4 (NaClO 4 (H 2 O) 2 AN 2.4 s) применяется для впервые, что эффективно увеличивает окно электрохимической стабильности (ESW) до 3,0 В и снижает внутреннее сопротивление батареи. На основе этого гибридного электролита, полная ячейка ASIB с углеродным покрытием Na 2,85 K 0.15 V 2 (PO 4 ) 3 и NaTi 2 (PO 4 ) 3 902 катод 905 и соответственно материалы катода 905 и , может обеспечить разрядную емкость и плотность энергии 52 мА ч г -1 и 51 Вт ч кг -1 , соответственно, при плотности тока 1 А г -1 . Плотность энергии этой батареи превышает почти все известные традиционные ASIB.
Эта статья в открытом доступе
Подождите, пока мы загрузим ваш контент… Что-то пошло не так. Попробуйте еще раз?границ | Последние достижения в области электролитов «вода в соли» для перезаряжаемых батарей без лития
Введение
В последнее время проблемы безопасности и стоимость производства аккумуляторных батарей стали основными факторами, ограничивающими их коммерческое применение в портативных электронных устройствах (PED), электромобилях (EV) и стационарных электронных системах накопления энергии (EES) (Wang et al., 2007; Суо и др., 2015; Лукацкая и др., 2018). Таким образом, вопрос о том, как эффективно выбрать подходящие материалы для изготовления аккумуляторов, стал важной и сложной темой. Являясь важным компонентом аккумуляторов, электролиты играют жизненно важную роль в превосходных электрохимических характеристиках аккумуляторов и в последние годы привлекают к себе все большее внимание (Kandhasamy et al., 2012; Yan et al., 2012; Suo et al. , 2013). Хотя традиционные органические электролиты нашли привлекательное применение в перезаряжаемых батареях, они по своей природе содержат большое количество дорогих, но легковоспламеняющихся органических растворителей с определенным уровнем токсичности, что делает условия сборки устройства относительно жесткими (Wang et al., 2012; Сюй и Ван, 2016; Ян и др., 2019а). Следовательно, водные электролиты были признаны многообещающими альтернативными кандидатами для усовершенствованных аккумуляторных батарей с момента их первого применения в литий-ионных батареях (LIB) (Li et al., 1994). Водные батареи обладают определенными достоинствами, включая низкую стоимость, высокую безопасность, высокую электронную проводимость, мягкую среду сборки и т. Д. (Wang et al., 2007; Baskar et al., 2014; Huang et al., 2019a). Однако диапазон напряжений электрохимической стабильности водных аккумуляторов составляет всего ~ 1.23 В, что серьезно ограничивает оптимальный выбор материалов катода и анода из-за наличия реакций выделения водорода и / или кислорода. Это исключает большинство электрохимических пар, которые возникают при выходном напряжении выше 1,5 В, что ограничивает увеличение плотности энергии полных устройств (Лу и др., 2011; Ким и др., 2014; Цзян и др., 2019a; Лю и др. ., 2020).
Недавно сообщалось, что высококонцентрированные электролиты типа «вода в соли» (WIS), в которых количество растворенных солей намного превышает количество молекул воды (соотношение соль / растворитель> 1 по объему или весу), увеличивают окно стабильного напряжения в большую сторону. до ~ 3.0 V (Suo et al., 2016, 2017). В электролитах WIS все молекулы воды участвуют в сольватационных оболочках ионов, и никаких «свободных» остатков воды обнаружить не удается. В качестве типичной системы Suo et al. впервые разработал электролит с высокой концентрацией с 21 м (моль кг -1 ) бис (трифторметилсульфонил) имида лития (LiTFSI) для водных перезаряжаемых LIB (молярное отношение Li + к H 2 O составляет 2,5) ( Wang et al., 2015). Однако экономические и экологические проблемы, а также редкость и растущее потребление ресурсов лития ограничивают масштабируемые применения электрохимических устройств на основе лития.Как следствие, разработка альтернативных водных аккумуляторных батарей на основе некоторых других элементов, богатых землей, оказывается актуальной и более значимой. Поэтому в последнее время интенсивно исследуются водные вторичные батареи на основе одновалентных (Na + , K + ) и / или поливалентных (Zn 2+ , Mg 2+ и Al 3+ ) ( Wessells et al., 2011; Zhao et al., 2016; Suo et al., 2017; Wang et al., 2020).
В этом мини-обзоре мы в основном коснулись темы электролитов WIS и их последних достижений в различных нелитиевых водных перезаряжаемых металл-ионных батареях (ARMIB).В первом разделе мы дали краткое исследование задействованного механизма WIS-электролитов в расширении окна напряжения электрохимической стабильности устройств. А затем мы представили обширный обзор применения электролитов WIS в водных нелитиевых вторичных батареях, включая водные натриево-ионные батареи (ASIB), водные калий-ионные батареи (APIB), водные цинково-ионные батареи (AZIB), водные ионно-магниевые батареи (AMIB) и водные алюминиево-ионные батареи (AAIB).Наконец, мы предложили существующие проблемы и перспективы будущего развития электролитов WIS для усовершенствованных нелитиевых ARMIB.
Механизм действия электролитов «WIS» в расширении электрохимического окна приборов
Хорошо известно, что доля свободной воды является одним из ключевых факторов, влияющих на электрохимическую стабильность электролитов (McEldrew et al., 2018; Vatamanu, Borodin, 2018). В традиционных электролитах типа «соль в воде» (SIW) молекулы воды значительно превосходят количество солей и относительно свободны для образования сетей водородных связей.Таким образом, большое количество молекул воды будет разделять или растворять (или разъедать) электродный материал (Dubouis et al., 2018; Huang et al., 2019a). По мере увеличения концентрации соли может образовываться более плотная сольватационная оболочка, связанная с электролитами WIS. Между тем, молекулы «свободная» вода-растворитель обладают меньшей подвижностью. Оказывается, они предпочтительно сольватированы ионами металлов и, следовательно, менее доступны для разделения анионов солей. Соответственно, водородные связи вода-вода заменяются взаимодействиями, связывающими воду и ионы, что усиливает взаимодействия между катионами и анионами, что может еще больше расширить стабильные рабочие окна электролитов (Азов и др., 2018).
Также считается, что образование межфазного слоя твердого электролита (SEI) с высокой концентрацией соли на поверхности электрода может предотвратить восстановление воды, что положительно влияет на широкий диапазон электрохимической стабильности. Чтобы быть конкретным, OH —, образующийся во время реакции водорода с кислородом в первом цикле, будет химически реагировать с анионами (такими как TFSI), в основном, с образованием стабильной пленки SEI, которая дополнительно предотвращает восстановление воды и повышает окислительную стабильность электродные мастерства (Coustan et al., 2018; Dubouis et al., 2018). Типичная сольватационная структура для электролитов WIS схематически изображена на схеме 1.
Схема 1 . Принципиальная схема сольватационной структуры электролитов WIS. Автор: Linrui Hou и др.
Хорошо известно, что это эффективная стратегия увеличения удельной энергии батарей за счет повышения рабочего напряжения (Xia et al., 2017; Manalastas et al., 2018). Напряжение, согласно следующему уравнению Нернста, сильно зависит от потенциалов полуэлементов как положительного, так и отрицательного электродов.
V = V0-RTnFln CaredCbox (2), где V 0 — стандартный восстановительный потенциал полуячейки по отношению к стандартному водородному электроду (SHE), R — универсальная газовая постоянная, T — абсолютная температура в кельвинах, n — стехиометрическое число электронов, F — постоянная Фарадея, C красный — концентрация восстановленной формы, C ox — концентрация окисленной формы, и a и b — экспоненциальные степени, определяемые коэффициентами C красный и C ox в окислительно-восстановительной полуреакции, соответственно.
Максимальный потенциал ячейки (Δ V ) критически определяется вычитанием потенциала между положительным и отрицательным ( V 0 + — V 0 — ). Более высокая концентрация окисленной формы (C ox ) устанавливает более сильные восстановительные потенциалы, как показано в уравнениях 1, 2. Концентрация электролита и пленка SEI могут эффективно контролировать разложение электролита, что позволяет окислительно-восстановительным ионам даже с более высокой концентрацией участвуют в электрохимических реакциях в расширенном окне электрохимических напряжений.Расчеты по теории функционала плотности (DFT) считаются эффективным способом расчета потенциалов восстановления солей анионов (Suo et al., 2015; Dawut et al., 2019; Shin et al., 2019).
Электролиты WIS для не литиевых армибов
Принимая во внимание некоторые полученные обзоры об электролитах WIS в литиевых водных батареях (Wang et al., 2012; Kim et al., 2014), этот мини-обзор будет в основном сосредоточен на последних достижениях в области высококонцентрированных электролитов WIS для нелитиевых аккумуляторов. ARMIB, включая ASIB, APIB, AZIB, AMIB и AAIB.Электрохимические свойства этих батарей систематически собраны в Таблице 1.
Таблица 1 . Основные электрохимические свойства водных нелитиевых аккумуляторов на основе WIS.
Хорошо известно, что электролиты как промежуточные соединения ионного переноса, с присущей им ионной проводимостью, подвижностью, межфазными характеристиками и другими свойствами, играют решающую роль в улучшении рабочих характеристик цикла. Разработка и оптимизация функционального электролита со стабильной границей раздела электрод / электролит следует рассматривать как важный способ достижения превосходных электрохимических характеристик в водных батареях.Типичные стратегии проектирования оптимизируются путем изменения компонентов электролита, включая соли и добавки (Peng et al., 2017; Zhao et al., 2020).
Выбор солей существенно влияет на электрохимическую стабильность электролитов, а также на их ионную проводимость и термическую стабильность. Солевые анионы в водных электролитах WIS обычно можно разделить на неорганические (Cl —, SO42- и ClO4-) и органические (CF 3 SO3-, FSI —, TFSI —, BETI — и PTFSI — ) (Hong et al., 2013; Zhang et al., 2020). Неорганические соли, вероятно, будут рассматриваться из-за их низкой стоимости и высокой ионной проводимости. Например, меньшее количество побочных реакций и низкое окисление Cl — делают его пригодным для водных электролитов (Zhang et al., 2018). В случае SO42- низкая стоимость, хорошая совместимость и исключительная стабильность делают его более привлекательным; тем не менее, некоторые побочные продукты, образующиеся при чрезмерном цикле, по-прежнему ограничивают его практическое применение (Zhao et al., 2016; Huang et al., 2019b).Другой анион — это ClO4-, который обладает сильной окисляемостью, что снижает вероятность взрыва и высокую токсичность (Lee et al., 2019). Объемные органические анионы (например, CF 3 SO3-, FSI —, TFSI —, BETI — и PTFSI —) в водных электролитах могут снизить эффект сольватации, занимая большое пространство. Эти анионы обладают низкой ионной проводимостью и проблемами коррозии (Yamada et al., 2016; Jiang et al., 2019a; Pan et al., 2019).
ASIBS
Натрий, как один из щелочных металлов, находится близко к литию в периодической таблице Менделеева и имеет относительно низкий электрохимический потенциал (−2.71 В против ОНА). Как правило, SIB имеют много общих химических свойств с LIB (Kim et al., 2012; Li et al., 2013; Boyd and Augustyn, 2018; Zheng et al., 2019). Высококонцентрированные электролиты WIS производят ASIB с лучшей стабильностью при циклическом изменении. Однако легкая кристаллизация высококонцентрированных электролитов при комнатной температуре серьезно ограничит их практическое применение и даже повредит батареи (Wu et al., 2015; Reber et al., 2019; Zhang et al., 2020). В настоящее время доказано, что гидратные расплавы или бисоль, особенно использование асимметричных имидных анионов (таких как FTFSI и PTFSI), являются эффективными для снижения вязкости и плотности, а также сдерживания кристаллизации за счет разрушения структуры воды и / или изменения вероятности сольватационных структур с ионными агрегациями (Marcus, 2009; Brini et al., 2017; Suo et al., 2017), что, таким образом, приводит к высокой растворимости солевых анионов (Suo et al., 2016; Zheng et al., 2019).
Как сообщалось в предыдущих работах, обычно используемые соли в электролитах ASIB — это NaClO 4 , NaFSI, NaCF 3 SO 3 (NaOTf) и NaTFSI из-за их уникальных свойств. Suo et al. впервые сообщили о слое SEI, проводящем Na + , на поверхности анода NaTi 2 (PO 4 ) 3 в электролите 9.26 м трифторметансульфонат натрия (NaCF 3 SO 3 или NaOTf), который расширяет окно электрохимической стабильности NaTi 2 (PO 4 ) 3 до 2,5 В (по сравнению с Na + / Na) (Suo et al., 2017). Кюнель и его сотрудники получили бис (фторсульфонил) имид натрия со сверхвысокой концентрацией (до 37 M) (NaFSI) в воде путем быстрого отверждения всего перенасыщенного раствора, предлагая стабильное электрохимическое окно 2,6 В. Поразительно, но водный NaTi 2 (PO 4 ) 3 // Na 3 (VOPO 4 ) 2 F натрий-ионный аккумулятор с электролитом 35 м NaFSI демонстрирует электрохимически обратимое поведение в пределах электрохимического окна над 2.0 V (Kühnel et al., 2017). Также показано, что электролиты NaFSI с различными концентрациями эффективно расширяют окна напряжений ASIB (Zheng et al., 2019). Другим широко используемым электролитом в ASIB является раствор NaClO 4 . Когда его моляльность увеличивается до 17 м, может быть реализовано стабильное окно электрохимического потенциала ~ 2,8 В (Nakamoto et al., 2017, 2018; Lee et al., 2019). Однако потенциальный риск взрыва и высокая токсичность могут препятствовать широкому использованию NaClO 4 .Battaglia et al. исследовали NaTi 2 (PO 4 ) 3 // Na 3 (VOPO 4 ) 2 F натрий-ионный аккумулятор с использованием смешанного электролита NaFSI / NaFTFSI (25 м NaFSI и 10 м NaFTFSI). Уникальное устройство демонстрирует превосходные электрохимические характеристики с точки зрения стабильности циклов, обратимой емкости и плотности энергии в широком диапазоне рабочих температур от -10 до 30 ° C, используя положительную роль смешанного электролита (Reber et al., 2019). Новый тип смешанных электролитов WIS, содержащих инертные катионы (TEA + ), получают растворением трифторметансульфоната натрия (NaOTf) и трифторметансульфоната тетраэтиламмония (TEAOTf) в воде. Когда общая концентрация соли достигает 31 м (9 м NaOTf и 22 м TEAOTf), уникальный электролит NaOTf / TEAOTf обладает широким диапазоном напряжений ~ 3,3 В, а также подавляет растворение положительного переходного металла ( Jiang et al., 2019a).
APIBS
Калийно-ионные батареи (PIB) также считаются многообещающей системой хранения энергии из-за их обильных запасов калия (Su et al., 2016; Эфтехари и др., 2017). Как правило, калий обладает более низким стандартным окислительно-восстановительным потенциалом, чем его аналоги Na и Li, что гарантирует PIB с потенциально более высоким напряжением ячейки. Однако более высокий потенциал ионизации и больший ионный радиус самого K ограничивают выбор электродных материалов для усовершенствованных APIB (Suo et al., 2017; Hwang et al., 2018). Благодаря меньшему радиусу Стокса сольватированного K + из-за его слабой кислотности по Льюису и низкому сопротивлению межфазной реакции из-за малой энергии активации десольватации, K-содержащие электролиты всегда демонстрируют более высокую проводимость, чем его аналоги Li / Na (Komaba и другие., 2015; Ким и др., 2017; Chen et al., 2020). Между тем, слабая стойкость электролитов к окислению и недостаточная пассивация на поверхности отрицательных электродов приводят к умеренным обратимым емкостям, особенно в начальном цикле или в рабочих окнах высокого напряжения (> 4,0 В), что ограничивает огромное развитие APIB (Хосака и др., 2018). Следовательно, важно установить высокоэнергетические APIB для целенаправленного исследования подходящих электролитов.
Леонард и его сотрудники впервые сообщили о водном электролите 30 м ацетата калия (KAc) для APIB (Леонард и др., 2018). С электролитом анод KTi 2 (PO 4 ) 3 (KTP) демонстрирует хорошие обратимые характеристики в расширенном электрохимическом окне от -1,7 до 1,5 В (по сравнению с Ag / AgCl). По сравнению с электролитами на основе KAc и LiTFSI с одинаковой концентрацией электролиты на основе бис (фторсульфонил) имида (KFSI) обладают более высокой проводимостью (Chen et al., 2020). Электролит 30 м KFSI также показывает окно электрохимической стабильности от -1,55 до 2,42 В (по сравнению с Hg / Hg 2 Cl 2 ), что позволяет b -перилен-3,4,9,10- диангидрид тетракарбоновой кислоты (b, -PTCDA) и даже полные батареи на основе b на основе -PTCDA для стабильной работы в таких высококонцентрированных электролитах без выделения водорода и растворения материала (Chen et al., 2020). Jiang et al. также исследовали водный диимид 3,4,9,10-перилентетракарбоновой кислоты (анод) // K 1,85 Fe 0,33 Mn 0,67 [Fe (CN) 6 ] 0,98 · 0,77H 2 O (катодное) полное устройство с 20 м электролитом KCF 3 SO 3 (KOTf) WIS и полная батарея демонстрируют беспрецедентные характеристики с точки зрения обратимой емкости и поведения скорости (Jiang et al., 2019b).
Асимметричные гидратные расплавы с оптимизированной эвтектической системой описаны как стабильный водный электролит с хорошей текучестью и пониженной вязкостью / плотностью, в котором все молекулы воды участвуют в гидратных оболочках Li + (Yamada et al., 2016). С введенным стабильным асимметричным анионом (например, PTFSI — ), K (PTFSI) 0,12 (TFSI) 0,08 (OTf) 0,8 · 2H 2 O в качестве щелочных расплавов демонстрирует отличную растворимость в воде и расширенное рабочее окно ~ 2,5 В (~ 2,14–4,65 В по сравнению с K + / K), но не страдает от уязвимой связи SF. Кроме того, ионная проводимость K (PTFSI) 0,12 (TFSI) 0,08 (OTf) 0,8 2H 2 O поддерживается на уровне ~ 34.6 мСм см -1 , что намного выше, чем у других типичных неводных электролитов (~ 10 мСм см -1 ) (Zheng et al., 2019).
АЗИБС
В последнее время AZIB, благодаря их замечательной термической стабильности, высокой теоретической удельной емкости (~ 820 мАч г -1 ), искробезопасности и низкой стоимости металлического Zn, считаются наиболее многообещающей альтернативой LIB. Более того, металлический Zn стабилен и может непосредственно использоваться в качестве электрохимически обратимого анода в водных электролитах (Zhang, 1996; Li et al., 2019). Однако его широкое применение все еще ограничено подходящими водными электролитами с превосходными тепловыми свойствами и безопасностью. Предыдущие работы показали, что щелочные водные электролиты приводят к образованию дендрита цинка и побочного продукта ZnO, вызывая плохую циклическую емкость и низкие значения CE (Zhang et al., 2014; Wang et al., 2018a). Точно так же нейтральные или слабокислые электролиты на основе солей цинка с высокими концентрациями являются очень эффективным способом решения этих проблем.
Как правило, растворы ZnSO 4 и Zn (CF 3 SO 3 ) 2 обычно используются в качестве электролитов для AZIB из-за их превосходной стабильности и совместимости (Song et al., 2018). Zhao et al. собрал Zn // LiMn 0,8 Fe 0,2 PO 4 водную гибридно-ионную батарею с 0,5 м ZnSO 4 и 21 м LiTFSI в качестве электролита WIS. Уникальное устройство обеспечивает высокую плотность энергии ~ 183 Втч кг -1 и высокое рабочее напряжение, превышающее 1.8 V (Zhao et al., 2016). Однако электролит ZnSO 4 для AZIB всегда страдает из-за его ограниченной растворимости и более низкой эффективности удаления цинка / нанесения покрытия. Напротив, электролит Zn (CF 3 SO 3 ) 2 демонстрирует меньшую поляризацию и более высокие значения CE, что делает его пригодным для широкого применения в водных ZIB (Huang et al., 2019b; Xie et al., 2020). Группа Маи разработала новый водный гибридно-ионный аккумулятор Zn // V 2 O 5 с электролитом WIS 1 м Zn (CF 3 SO 3 ) 2 и 21 м LiTFSI.По сравнению с батареей Zn // V 2 O 5 с электролитом WIS (21 м LiTFSI и 1 м Zn (CF 3 SO 3 ) 2 ) показал более стабильную плато заряда / разряда и циклическую производительность (Hu et al., 2017). Кроме того, благодаря анионам TFSI — большого размера, Zn (TFSI) 2 , как новая органическая соль цинка, может эффективно снижать эффект сольватации. Группа Вана разработала электролит WIS из 1 м Zn (TFSI) 2 + 20 м LiTFSI, который способен удерживать воду в открытой атмосфере.Он эффективно способствует осаждению / удалению металлического Zn без дендритов с почти 100% CE и обеспечивает беспрецедентную обратимость водных ZIB с катодами LiMn 2 O 4 или O 2 (Wang et al., 2018a) . Кроме того, новый недорогой электролит WIS с содержанием 30 м ZnCl 2 может обеспечить широкое электрохимическое окно 2,3 В благодаря меньшему количеству побочных реакций и низкому окислительному Cl — (Zhang et al., 2018). В симметричной ячейке Zn || Zn с 30 мкм электролитом ZnCl 2 Zn электрод обеспечивает высокий CE 95.4% и высокий стабильный профиль гальваностатического заряда-разряда более 600 часов без каких-либо значительных колебаний перенапряжения (Zhang et al., 2018).
AMIBS
Многовалентные ионы, как хорошие переносчики, могут переносить больше электронов, чем одновалентные ионы. Помимо Zn 2+ , другой двухвалентный ион металла Mg 2+ с низким потенциалом восстановления (-2,37 В) также считается преобладающим носителем заряда для AMIB из-за высокой объемной удельной емкости Mg (~ 3833 мАч. L −1 ) и общая задержка роста дендритов (Rasul et al., 2012; Song et al., 2015; Сюй и др., 2015; Sun et al., 2016). Текущие разработки и практическое применение электролитов для AMIB ограничены коррозией электролитов (Wang et al., 2017; Zhao et al., 2020). Электрохимическое растворение Mg происходит при высоком перенапряжении, что ограничивает выбор растворителей (Hebié et al., 2017). Следовательно, обычно используемые анионы (Cl — , SO42-, ClO4-, CF 3 SO3-) в других ARMIB не могут быть напрямую применены к AMIB.Более того, высокая плотность заряда многовалентных ионов будет вызывать сильные кулоновские взаимодействия как с решеткой растворителей электролитов, так и с материалами электродов, что является неблагоприятным фактором для улучшения электрохимических характеристик (Lapidus et al., 2014; Wang et al., 2018b). Пока что AMIB все еще находятся в зачаточном состоянии; только несколько возможных материалов на основе электролитов WIS показывают обратимые характеристики по отношению к AMIB.
Более того, Mg (TFSI) 2 , как нейтральная молекула, полностью не вызывает коррозии, безопасен и экологически чист, и его можно ожидать для применения AMIB (Yoo et al., 2013). Wang et al. изготовили полипиромеллитовый диангидрид // Li 3 V 2 (PO 4 ) 3 устройство с использованием 4 м Mg (TFSI) 2 в качестве электролита. Полная ячейка демонстрирует превосходные электрохимические свойства, включая отличную производительность, высокую плотность мощности и высокую емкость в электрохимическом окне 1,9 В (Wang et al., 2017).
AAIBS
Алюминий — первый металлический элемент в земной коре, который широко исследован в качестве материала анода для AAIB (Wang et al., 2016). Более того, ионный радиус Al 3+ (0,054 нм) намного меньше, чем у Li + (0,076 нм), что обеспечивает быстрое введение / извлечение Al 3+ во время процесса заряда / разряда (Rudd и Гиббонс, 1994; Li et al., 2007; Das et al., 2017; Yang et al., 2019b). Кроме того, алюминиевый анод обладает большой гравиметрической / объемной емкостью (~ 2,980 мАч г -1 / ~ 8,046 мАч г см -3 ) благодаря своей уникальной способности переноса трех электронов. Однако низкая ионная проводимость, коррозия с низкими концентрациями электролитов и рост дендритов по-прежнему ограничивают электрохимическую стабильность электролитов, тем самым ограничивая его крупномасштабные энергетические применения (Liu et al., 2012; Накаяма и др., 2015; Чжао и др., 2018). Таким образом, ключом к разработке AAIB является использование электролитов WIS для создания высокоэффективных электродов, которые могут способствовать растворению дендритов, тем самым значительно улучшая стабильность циклирования.
AlCl 3 , благодаря сверхнизкой стоимости и безопасности, широко используется в качестве электролитов для AAIB. Pan et al. сообщили о высококонцентрированном водном растворе AlCl 3 (3,382 м) в качестве электролита для новой водной батареи Al / AlCl 3 / графит, которая может стабильно работать в диапазоне электрохимической стабильности ~ 4 В и проявлять большую емкость ~ 165 при 500 мА г -1 вместе с высоким CE 95% за 1000 циклов (Pan et al., 2019). Кроме того, Al (OTf) 3 — это другой тип электролита с некоррозионными свойствами, что делает его более предпочтительным, чем коррозионный AlCl 3 при применении в AAIB (Das et al., 2017). Группа Чена представила электролит 5 м Al (OTf) 3 для электрохимической оценки катода FeFe (CN) 6 (FF-PBA) типа аналогов берлинской синей. Примечательно, что с электролитом FF-PBA показывает чрезвычайно высокую начальную разрядную емкость ~ 116 мАч г -1 и длительный срок службы при снижении емкости до 0.39% за цикл в расширенном рабочем окне 2,65 В (Zhou et al., 2019). До сих пор сообщалось о нескольких других электролитах WIS для AAIB.
Заключение
Электролиты, как промежуточные соединения ионного переноса с присущей ионной проводимости, подвижностью, межфазными характеристиками и другими свойствами, играют решающую роль в улучшении рабочих характеристик цикла, емкости и безопасности батарей. Электролиты WIS с высококонцентрированными солевыми растворами, в частности, могут расширять окна электрохимического потенциала водных устройств примерно до 3 В и приводить к низкой активности растворителя (молекул воды) и высокой химической стабильности (сдерживание побочных реакций).Более того, формирование стабильной пленки SEI также наделяет клетки высокой плотностью энергии и превосходной стабильностью при циклическом воздействии. Этот мини-обзор в основном посвящен электролитам WIS для ARMIB и суммирует результаты недавних исследований электролитов WIS в нелитиевых батареях с одновалентными (Na, K) и поливалентными (Zn, Mg, Al) ионами.
Однако исследования, основанные на электролитах WIS, все еще находятся на начальной стадии, судя по достижениям, о которых сообщалось на данный момент; Задачи и перспективы будущего развития WIS-электролитов для нелитиевых ARMIB предлагаются следующим образом.Во-первых, научная основа для высококонцентрированных электролитов WIS создаст некоторые новые, но неизвестные концепции, которые могут противоречить текущим классическим теориям, и должны быть в дальнейшем раскрыты с помощью элегантной комбинации спектроскопических методов in / ex-situ и теоретических моделирование / расчет. Например, необходимо всесторонне изучить собственный ионный транспорт и функциональные механизмы образования SEI в электролите WIS, которые отличаются от обычных систем SIW.Во-вторых, для высокоэффективных WIS-электролитов следует принимать во внимание дальнейшие исследования соответствующих солей, особенно с высокой термодинамической стабильностью, суперионной проводимостью и хорошей совместимостью с обоими электродами при низкой стоимости, учитывая их практическое коммерческое применение. В-третьих, необходимо также найти баланс между электролитами с высокой концентрацией и низкой вязкостью и кристаллизацией.
Несмотря на огромные трудности и проблемы, мы твердо верим, что водные аккумуляторные батареи на основе электролитов WIS получат быстрое и устойчивое развитие в ближайшем будущем.Это приведет к появлению новых возможностей в области хранения энергии в будущем.
Авторские взносы
YW: формальный анализ, расследование, написание — первоначальный черновик и написание — просмотр и редактирование. XM: расследование. JS: формальный анализ и написание — просмотр и редактирование. YL: визуализация и программное обеспечение. LH: формальный анализ, исследование, концептуализация, написание — рецензирование и редактирование, а также получение финансирования. Все авторы внесли свой вклад в статью и одобрили представленную версию.
Финансирование
Эта работа была поддержана Национальным фондом естественных наук Китая (№№ 51772131, 51802119), Фондом докторантуры естественных наук провинции Шаньдун (ZR2019BEM038, ZR2019BB057) и Фондом докторантуры естественных наук Университета Цзинань (XBS1830).
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
Азов, В. А., Егорова, К. С., Сейткалиева, М. М., Кашин, А. С., Анаников, В. П. (2018). Системы «сольвент в соли» для разработки новых материалов в химии, биологии и энергетических исследованиях. Chem. Soc. Re. 47, 1250–1284. DOI: 10.1039 / c7cs00547d
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Баскар С., Мейрик Д., Калаи Селван Р. и Минакши М. (2014). Легкий и крупномасштабный синтез альфа-CoMoO4 с помощью сжигания: имитирует окислительно-восстановительное поведение батареи в водном гибридном устройстве. Chem. Англ. J. 253, 502–507. DOI: 10.1016 / j.cej.2014.05.068
CrossRef Полный текст | Google Scholar
Бойд, С., Августин, В. (2018). Оксиды переходных металлов для водного электрохимического накопления энергии иона натрия. Inorg. Chem. Передний. 5, 999–1015. DOI: 10.1039 / c8qi00148k
CrossRef Полный текст | Google Scholar
Брини, Э., Феннелл, К. Дж., Фернандес-Серра, М., Хрибар-Ли, Б., Лукшич, М., и Дилл, К. А. (2017). Как свойства воды закодированы в ее молекулярной структуре и энергии. Chem. Ред. 117, 12385–12414. DOI: 10.1021 / acs. ~ chemrev.7b00259.
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Chen, H., Zhang, Z. Y., Wei, Z. X., Chen, G., Yang, X., Wang, C.Z., et al. (2020). Использование водно-солевого электролита, чтобы избежать растворения органических материалов и улучшить кинетику водно-ионных калийных батарей. Sustain. Энергетическое топливо 4, 128–131. DOI: 10.1039 / c9se00545e
CrossRef Полный текст | Google Scholar
Кустан, Л., Загиб, К., и Беланже, Д. (2018). Новое понимание электрохимического поведения электрода из нержавеющей стали в водно-солевом электролите. J. Источники энергии 399, 299–303. DOI: 10.1016 / j.jpowsour.2018.07.114
CrossRef Полный текст | Google Scholar
Дас, С. К., Махапатра, С., и Лахан, Х. (2017). Алюминиево-ионные аккумуляторы: разработки и проблемы. J. Mater. Chem. А 5, 6347–6367. DOI: 10.1039 / c7ta00228a
CrossRef Полный текст | Google Scholar
Давут, Г., Лу, Ю., Мяо, Л.С., и Чен, Дж. (2019). Высокопроизводительные перезаряжаемые водные цинк-ионные батареи с катодом из поли (бензохинонилсульфида). Inorg. Chem. Передний. 5, 1391–1396. DOI: 10.1039 / c8qI00197a
CrossRef Полный текст | Google Scholar
Dubouis, N., Lemaire, P., Mirvaux, B., Salager, E., Deschamps, M., and Grimaud, A. (2018). Роль реакции выделения водорода на механизм межфазного образования твердых электролитов для «водно-солевых» электролитов. Energy Environ.Sci. 11, 3491–3499. DOI: 10.1039 / c8ee02456a
CrossRef Полный текст | Google Scholar
Эбие, С., Нго, Х. П. К., Лепретр, Дж. К., Йоджу, К., Куанто, Л., Бертло, Р., и др. (2017). Электролит на основе легко синтезируемой недорогой трифенолят-борогидридной соли для высокоэффективных Mg (TFSI) 2 -глимовых перезаряжаемых магниевых батарей. ACS Appl. Матер. Интерфейсы 9, 28377–28385. DOI: 10.1021 / acsami.7b06022
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хонг, С.Ю., Ким, Ю., Пак, Ю., Чой, А., Чой, Н., и Ли, К. Т. (2013). Носители заряда в аккумуляторных батареях: ионы Na против ионов Li. Energy Environ. Sci. 6, 2067–2081. DOI: 10.1039 / c3ee40811f
CrossRef Полный текст | Google Scholar
Хосака Т., Кубота К., Кодзима Х. и Комаба С. (2018). Высококонцентрированные растворы электролитов для калиево-ионных аккумуляторов класса 4 В. Chem. Comm. 54, 8387–8390. DOI: 10.1039 / c8cc04433c
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ху, П., Ян, М. Ю., Чжу, Т., Ван, X. П., Вэй, X. J., Ли, Дж. Т. и др. (2017). Zn / V 2 O 5 Водный гибридно-ионный аккумулятор с высоковольтной платформой и длительным сроком службы. ACS Appl. Матер. Интерфейсы 9, 42717–42722. DOI: 10.1021 / acsami.7b13110
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хуанг, Дж. Х., Го, З. В., Ма, Ю. Ю., Бин, Д., Ван, Ю. Г. и Ся, Ю. Г. (2019a). Недавний прогресс аккумуляторных батарей с использованием мягких водных электролитов. Малые методы 3: 1800272. DOI: 10.1002 / smtd.201800272
CrossRef Полный текст | Google Scholar
Hwang, J.-Y., Myung, S.-T., and Sun, Y.-K. (2018). Последние достижения в области перезаряжаемых калиевых батарей. Adv. Весело. Матер. 28: 1802938. DOI: 10.1002 / adfm.201802938
CrossRef Полный текст | Google Scholar
Jiang, L. W., Liu, L. L., Yue, J. M., Zhang, Q.Q., Zhou, A. X., Borodin, O., et al. (2019a). Высоковольтная водно-ионная аккумуляторная батарея с водно-солевым электролитом с инертными катионами. Adv. Матер. 32: 17. DOI: 10.1002 / adma.2017
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Jiang, L. W., Lu, Y. X., Zhao, C. L., Liu, L. L., Zhang, J. N., Zhang, Q.Q., et al. (2019b). Создание водных K-ионных аккумуляторов для хранения энергии. Nat. Энергия 4, 495–503. DOI: 10.1038 / s41560-019-0388-0
CrossRef Полный текст | Google Scholar
Кандхасами С., Пандей А. и Минакши М. (2012). Золь-гель путь с поливинилпирролидоном LiCo 1/ 3Mn 1/3 Ni 1/3 PO 4 Композитный катод для водной аккумуляторной батареи. Электрохим. Acta 60, 170–176. DOI: 10.1016 / j.electacta.2011.11.028
CrossRef Полный текст | Google Scholar
Ким, Х., Хонг, Дж., Пак, К.-Й., Ким, Х., Ким, С.-В., и Кан, К. (2014). Водные перезаряжаемые ионно-литиевые и натриевые батареи. Chem. Ред. 114, 11788–11827. DOI: 10.1021 / cr500232y
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ким, Х., Ким, Дж. К., Бьянкини, М., Сео, Д.-Х., Родригес-Гарсия, Дж., И Седер, Г.(2017). Последние достижения в области электродных материалов для K-ионных аккумуляторов. Adv. Energy Mater. 8: 1702384. DOI: 10.1002 / aenm.201702384
CrossRef Полный текст | Google Scholar
Ким С.-В., Сео Д.-Х., Ма X. Х., Седер Г. и Канг К. (2012). Электродные материалы для перезаряжаемых натриево-ионных батарей: потенциальные альтернативы существующим литий-ионным батареям. Adv. Energy Mater. 2, 710–721. DOI: 10.1002 / aenm.201200026
CrossRef Полный текст | Google Scholar
Комаба, С., Хасегава, Т., Дахби, М., и Кубота, К. (2015). Внедрение калия в графит для создания высоковольтных / мощных калий-ионных батарей и калий-ионных конденсаторов. Electrochem. Commun. 60, 172–175. DOI: 10.1016 / j.elecom.2015.09.002
CrossRef Полный текст | Google Scholar
Кюнель, Р. С., Ребер, Д., и Батталья, К. (2017). Высоковольтный водный электролит для натрий-ионных аккумуляторов. ACS Energy Lett. 2, 2005–2006. DOI: 10.1021 / acsenergylett.7b00623
CrossRef Полный текст | Google Scholar
Лапидус, С. Х., Раджпут, Н. Н., Ку, X., Чепмен, К. В., Перссон, К. А., и Чупас, П. Дж. (2014). Сольватационная структура и энергетика электролитов для хранения многовалентной энергии. Phys. Chem. Chem. Phys. 16, 21941–21945. DOI: 10.1039 / c4cp03015j
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, М. Х., Ким, С. Дж., Чанг, Д. Х., Ким, Дж. С., Мун, С., О, К. и др. (2019).К недорогой высоковольтной водно-натриевой аккумуляторной батарее. Mater. Сегодня 29, 26–36. DOI: 10.1016 / j.mattod.2019.02.004
CrossRef Полный текст | Google Scholar
Леонард, Д. П., Вэй, З. X., Чен, Г., Ду, Ф., и Цзи, X. Л. (2018). Водно-солевой электролит для калий-ионных аккумуляторов. ACS Energy Lett. 3, 373–374. DOI: 10.1021 / acsenergylett.8b00009
CrossRef Полный текст | Google Scholar
Ли, К. С., Цзи, В. К., Чен, Дж., и Тао, З. Л. (2007). Металлические алюминиевые наностержни: синтез методом осаждения из паровой фазы и применение в алюминиево-воздушных батареях. Chem. Матер. 19, 5812–5814. DOI: 10,1021 / см7018795
CrossRef Полный текст | Google Scholar
Li, X. L., Ma, L. T., Zhao, Y. W., Yang, Q., Wang, D.H., Huang, Z. D., et al. (2019). Нанопроволоки гидратированного гибридного оксида ванадия в качестве лучшего катода для водной цинковой батареи. Mater. Сегодня Энергия 14: 100361. DOI: 10.1016 / j.mtener.2019.100361
CrossRef Полный текст | Google Scholar
Li, Z., Young, D., Xiang, K., Carter, W. C., and Chiang, Y.-M. (2013). На пути к высокомощным водным натрий-ионным батареям высокой энергии: NaTi 2 (PO 4 ) 3 / Na 0,44 Система MnO 2 . Adv. Energy Mater. 3, 290–294. DOI: 10.1002 / aenm.201200598
CrossRef Полный текст | Google Scholar
Лю К., Чи, X. W., Han, Q., и Лю, Ю. (2020). Аккумулятор на водной основе с высокой плотностью энергии, достигаемый за счет двойных реакций растворения / осаждения, разделенных в кислотно-щелочном электролите. Adv. Energy Mater. 10: 1
9. DOI: 10.1002 / aenm.2019CrossRef Полный текст | Google Scholar
Лю С., Ху, Дж. Дж., Янь, Н. Ф., Пань, Г. Л., Ли, Г. Р., и Гао, Х. П. (2012). Поведение алюминия при хранении анатаза TiO 2 массивов нанотрубок в водном растворе для алюминиево-ионных аккумуляторов. Energy Environ. Sci. 5, 9743–9746. DOI: 10.1039 / c2ee22987k
CrossRef Полный текст | Google Scholar
Лукацкая М.Р., Фельдблюм Ю.I., Mackanic, D.G., Lissel, F., Michels, D.L., Cui, Y., et al. (2018). Концентрированные смешанные водно-солевые растворы ацетата катионов в качестве экологически чистых и недорогих высоковольтных электролитов для водных аккумуляторов. Energy Environ. Sci. 11, 2876–2883. DOI: 10.1039 / c8ee00833g
CrossRef Полный текст | Google Scholar
Маналастас, В. Дж., Кумар, С., Верма, В., Чжан, Л. П., Юань, Д., и Шринивасан, М. (2018). Вода в аккумуляторных поливалентных ионных батареях: электрохимический ящик Пандоры. ChemSusChem. 12, 379–396. DOI: 10.1002 / cssc.201801523
PubMed Аннотация | CrossRef Полный текст | Google Scholar
МакЭлдрю М., Гудвин З. А. Х., Корнышев А. А., Базант М. З. (2018). Теория двойного слоя в водно-солевых электролитах. J. Phys. Chem. Lett. 9, 5840–5846. DOI: 10.1021 / acs.jpclett.8b02543
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Накамото, К., Сакамото, Р., Ито, М., Китаджо, А., и Окада, С. (2017). Влияние концентрированного электролита на водную натриево-ионную батарею с катодом из гексацианоферрата марганца натрия. Electrochem. 85, 179–185. DOI: 10.5796 / электрохимия.85.179
CrossRef Полный текст | Google Scholar
Накамото, К., Сакамото, Р., Савада, Ю. К., Ито, М., и Окада, С. (2018). Водный натрий-ионный аккумулятор более 2 В с электродами типа берлинского голубого цвета. Малые методы 3: 1800220. DOI: 10.1002 / smtd.201800220
CrossRef Полный текст | Google Scholar
Накаяма, Ю., Сенда, Ю., Кавасаки, Х., Кошитани, Н., Хосой, С., Кудо, Ю. и др. (2015). Электролиты на основе сульфона для алюминиевых аккумуляторных батарей. Phys. Chem. Chem. Phys. 17, 5758–5766. DOI: 10.1039 / c4cp02183e
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пан, В. Д., Ван, Ю. Ф., Чжан, Ю. Г., Квок, Х. Ю. Х., Ву, М. Ю., Чжао, X. Л. и др. (2019). Недорогая аккумуляторная алюминий-ионная батарея без дендритов с превосходными характеристиками. J. Mater.Chem. А 7, 17420–17425. DOI: 10.1039 / c9ta05207k
CrossRef Полный текст | Google Scholar
Пэн Н., Чжао Н., Чжан З. Г., Ван Х., Линь Х., Лю М. и др. (2017). Стабилизирующий интерфейс Li / электролит с трансплантируемым защитным слоем на основе наноразмерных доменов LiF. Nano Energy 39, 662–672. DOI: 10.1016 / j.nanoen.2017.07.052
CrossRef Полный текст | Google Scholar
Расул, С., Судзуки, С., Ямагути, С., и Мияяма, М.(2012). Положительные электроды большой емкости для вторичных Mg-ионных аккумуляторов. Электрохим. Acta 82, 243–249. DOI: 10.1016 / j.electacta.2012.03.095
CrossRef Полный текст | Google Scholar
Ребер Д., Кюнель Р. С. и Батталья К. (2019). Подавление кристаллизации водно-солевых электролитов асимметричными анионами обеспечивает низкотемпературную работу высоковольтных водных аккумуляторов. ACS Materials Lett. 1, 44–51. DOI: 10.1021 / acsmaterialslett.9b00043
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Радд, Э.Дж. И Гиббонс Д. В. (1994). Алюминий / кислородный элемент с высокой плотностью энергии. J. Источники энергии 47, 329–340. DOI: 10.1016 / 0378-7753 (94) 87012-8
CrossRef Полный текст | Google Scholar
Шин, Дж., Чой, Д. С., Ли, Х. Дж., Юнг, Ю. С., и Чой, Дж. У. (2019). Гидратированная интеркаляция для высокоэффективных водных цинково-ионных батарей. Adv. Energy Mater. 9: 1
3. DOI: 10.1002 / aenm.201
3
CrossRef Полный текст | Google Scholar
Сонг, Дж., Нокед, М., Жилетт, Э., Дуай, Дж., Рублофф, Г., и Ли, С. Б. (2015). Активация катода MnO 2 водостимулированной вставкой Mg 2+ для ионно-магниевого аккумулятора. Phys. Chem. Chem. Phys. 17, 5256–5264. DOI: 10.1039 / c4cp05591h
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сонг, М., Тан, Х., Чао, Д. Л., и Фань, Х. Дж. (2018). Последние достижения в области ионно-цинковых аккумуляторов. Adv. Весело. Матер. 28: 1802564. DOI: 10.1002 / adfm.201802564
CrossRef Полный текст | Google Scholar
Су, Д. В., МакДонанг, А., Цяо, С.-, З. и Ван, Г. X. (2016). Водные ионно-калийные батареи большой емкости для крупномасштабного хранения энергии. Adv. Матер. 29: 1604007. DOI: 10.1002 / adma.201604007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сан, X. К., Даффорт, В., Мехди, Б. Л., Браунинг, Н. Д., и Назар, Л. Ф. (2016). Исследование механизма внедрения Mg в бирнессит в неводных и водных перезаряжаемых Mg-ионных батареях. Chem. Матер. 28, 534–542. DOI: 10.1021 / acs.chemmater.5b03983
CrossRef Полный текст | Google Scholar
Суо, Л. М., Бородин, О., Гао, Т., Ольгин, М., Хо, Дж., Фан, X. Л. и др. (2015). Электролит «вода в соли» позволяет получать высоковольтные водные литий-ионные химические соединения. Science 350, 938–943. DOI: 10.1126 / science.aab1595
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Суо, Л. М., Бородин, О., Сун, В., Фань, X. Л., Янг, К.Y., Wang, F., et al. (2016). Усовершенствованная высоковольтная литий-ионная аккумуляторная батарея на водной основе с использованием электролита «вода в бисолевой соли». Angew. Chem. Int. Эд. 55, 7136–7141. DOI: 10.1002 / ange.201602397
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Суо, Л. М., Бородин, О., Ван, Ю. С., Ронг, X. Х., Сан, В., Фан, X. Л. и др. (2017). Электролит «вода в соли» делает водные натриево-ионные батареи безопасными, экологичными и долговечными. Adv. Energy Mater. 7: 1701189.DOI: 10.1002 / aenm.201701189
CrossRef Полный текст | Google Scholar
Суо, Л. М., Ху, Ю. С., Ли, Х., Арманд, М., и Чен, Л. К. (2013). Новый класс сольвентного электролита для перезаряжаемых металлических литиевых батарей высокой энергии. Nat. Commun. 4: 1481. DOI: 10.1038 / ncomms2513
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ватаману, Дж., Бородин, О. (2018). Разветвления межфазной структуры вода-в-соли на заряженных электродах для электрохимической стабильности электролита. J. Phys. Chem. Lett. 8, 4362–4367. DOI: 10.1021 / acs.jpclett.7b01879
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван, Ф., Бородин, О., Гао, Т., Фань, X. Л., Сунь, В., Хан, Ф. Д. и др. (2018a). Сильно обратимый цинк-металлический анод для водных аккумуляторов. Nat. Матер. 17, 543–549. DOI: 10.1038 / s41563-018-0063-z
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван, Ф., Фань, X. Л., Гао, Т., Сунь, В., Ма, З.H., Yang, C.Y. и др. (2017). Высоковольтные водные ионно-магниевые батареи. ACS Cent. Sci. 3, 1121–1128. DOI: 10.1021 / acscentsci.7b00361
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Wang, F. X., Yu, F., Wang, X. W., Chang, Z., Fu, L.J., Zhu, Y. S., et al. (2016). Перезаряжаемый ионно-цинковый аккумулятор на водной основе с хорошими характеристиками при езде. ACS Appl. Матер. Интерфейсы 8, 9022–9029. DOI: 10.1021 / acsami.5b06142
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван, Г., Фу, Л., Чжао, Н., Ян, Л., Ву, Ю. и Ву, Х. (2007). Перезаряжаемая литиевая батарея на водной основе с хорошими характеристиками при езде на велосипеде. Angew. Chem. Int. Эд. 46, 295–297. DOI: 10.1002 / anie.200603699
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван Х., Ван М. и Тан Ю. Б. (2018b). Новый цинк-ионный гибридный суперконденсатор для долговечных и недорогих накопителей энергии. Energy Storage Mater. 13, 1–7. DOI: 10.1016 / j.ensm.2017.12.022
CrossRef Полный текст | Google Scholar
Wang, P. P., Chen, Z., Wang, H., Ji, Z. Y., Feng, Y. P., Wang, J. Q., et al. (2020). Высокоэффективная гибкая водно-ионная аккумуляторная батарея с длительным сроком службы. Energy Storage Mater. 25, 426–435. DOI: 10.1016 / j.ensm.2019.09.038
CrossRef Полный текст | Google Scholar
Ван, Ю. Г., Йи, Дж., И Ся, Ю. Г. (2012). Прогресс в области водных литий-ионных аккумуляторов. Adv. Energy Mater. 2, 830–840. DOI: 10.1002 / aenm.201200065
CrossRef Полный текст | Google Scholar
Ван, Ю. С., Лю, Дж., Ли, Б., Цяо, Р. М., Янг, З. З., Сюй, С. Ю. и др. (2015). Ti-замещенный оксид Na туннельного типа 0,44 MnO 2 в качестве отрицательного электрода для водных натрий-ионных аккумуляторов. Nat. Commun. 6. 1–10. DOI: 10.1038 / ncomms7401
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уэсселлс, К. Д., Педдада, С.В., Хаггинс Р. А., Цуй Ю. (2011). Электроды из наночастиц гексацианоферрата никеля для водных натриевых и калиевых ионных аккумуляторов. Nano Lett. 11, 5421–5425. DOI: 10.1021 / nl203193q
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Wu, X. Y., Luo, Y., Sun, M. Y., Qian, J. F., Cao, Y. L., Ai, X. P., et al. (2015). Низкодефектные нанокубцы берлинского голубого цвета в качестве катодов большой емкости и длительного срока службы для водных Na-ионных аккумуляторов. Nano Energy 13, 117–124.DOI: 10.1016 / j.nanoen.2015.02.006
CrossRef Полный текст | Google Scholar
Xie, X. S., Liang, S. Q., Gao, J. W., Guo, S., Guo, J. B., Wang, C., et al. (2020). Управление кинетикой ионного переноса и стабильностью границы раздела для высокоэффективных металлических цинковых анодов. Energy Environ. Sci. 13, 503–510. DOI: 10.1039 / C9EE03545a
CrossRef Полный текст | Google Scholar
Сюй, К. Дж., Чен, Ю. Ю., Ши, С., Ли, Дж., Кан, Ф. Ю. и Су, Д. С. (2015).Вторичные батареи с многовалентными ионами для хранения энергии. Sci. Отчет 5: 14120. DOI: 10.1038 / srep14120
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ямада Ю., Усуи К., Содеяма К., Ко С., Татэяма Ю. и Ямада А. (2016). Электролиты гидрат-расплав для водных аккумуляторов с высокой плотностью энергии. Nat. Энергия. 1: 16129. DOI: 10.1038 / nenergy.2016.129
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ян, Дж., Ван, Дж., Лю, Х., Бакенов, З., Госселинк, Д., и Чен, П. (2012). Перезаряжаемые гибридные водные батареи. J. Источники энергии 216, 222–226. DOI: 10.1016 / j.jpowsour.2012.05.063
CrossRef Полный текст | Google Scholar
Янг, К., Чен, Дж., Джи, Х., Поллард, Т. П., Лу, Х. Дж., Сан, К. Дж. И др. (2019a). Литий-ионный аккумулятор на водной основе, полученный за счет химии галогенового преобразования-интеркаляции в графите. Nature 569, 245–250. DOI: 10.1038 / s41586-019-1175-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ян, Х.К., Ли, Х. С., Ли, Дж., Сан, З. Х., Хе, К., Ченг, Х.-М. и др. (2019b). Перезаряжаемый алюминиевый аккумулятор: возможности и проблемы. Angew. Chem. Int. Эд. Англ. 58, 11978–11996. DOI: 10.1002 / anie.201814031
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ю, Х. Д., Штеренберг, И., Гофер, Ю., Гершинский, Г., Пур, Н., Аурбах, Д. (2013). Перезаряжаемые магниевые батареи: постоянная задача. Energy Environ. Sci. 6: 2265. DOI: 10.1039 / c3ee40871j
CrossRef Полный текст | Google Scholar
Zhang, C., Holoubek, J., Wu, X.Y., Daniyar, A., Zhu, L.D., Chen, C., et al. (2018). ZnCl 2 Водно-солевой электролит для обратимого металлического цинкового анода. Chem. Commun. 54, 14097–14099. DOI: 10.1039 / c8cc07730d
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжан, Дж. Й., Яо, X. Х., Мисра, Р. К., Цай, К., и Чжао, Ю. Л. (2020). Прогресс в электролитах для литий-ионных батарей. J. Mater. Sci. Technol. 44, 237–257. DOI: 10.1016 / j.jmst.2020.01.017
CrossRef Полный текст | Google Scholar
Чжан, Л. Ю., Чен, Л., Чжоу, X. Ф., и Лю, З. П. (2014). На пути к высоковольтным водным металло-ионным батареям свыше 1,5 В: система гексацианоферрата цинка / цинка. Adv. Energy Mater. 5: 1400930. DOI: 10.1002 / aenm.201400930
CrossRef Полный текст | Google Scholar
Чжао, Дж. У., Ли, Ю. К., Пэн, X., Донг, С. М., Ма, Дж., Цуй, Г. Л. и др. (2016). Высоковольтная Zn / LiMn 0,8 Fe 0,2 PO 4 водная аккумуляторная батарея на основе водно-солевого электролита. Electrochem. Commun. 69, 6–10. DOI: 10.1016 / j.elecom.2016.05.014
CrossRef Полный текст | Google Scholar
Чжао, К., Захман, М. Дж., Аль-Садат, В. И., Чжэн, Дж.

