Нужно ли доливать электролит в аккумулятор? — Иксора
Аккумуляторный электролит — это жидкое вещество, которое содержится в большинстве автомобильных аккумуляторов. Иногда его называют аккумуляторной кислотой, потому что он имеет кислотную базу. Фактически, электролит батареи состоит из смеси воды и серной кислоты.
Когда уровень электролита в вашей АКБ становится низким, вы можете задаться вопросом, чем нужно пополнить его объем. Некоторые автовладельцы ошибочно считают, что в экстренной ситуации аккумулятор можно заполнить соленой водой, пищевой содой или каким-либо другим видом электролита. Наш ответ – нет. Никогда не добавляйте какой-либо электролит в свинцово-кислотный автомобильный аккумулятор.
Если вы обнаружили низкий уровень электролита в своем АКБ, вам следует добавить только чистую воду. И только при некоторых, очень специфических обстоятельствах, в батарею можно добавить серную кислоту. Например, если аккумулятор опрокинулся и протек.
Что означает низкий уровень электролита в батарее?
Когда ваш механик или друг, который много знает об автомобилях, говорит вам, что у вас низкий уровень электролита, это означает, что уровень жидкости в одном или нескольких элементах батареи упал ниже верха свинцовых пластин. Рассмотрим эту ситуацию подробнее.
Рассмотрим эту ситуацию подробнее.
Автомобильные аккумуляторы состоят из ряда свинцовых пластин, погруженных в своеобразную ванну с водой и серной кислотой, которая действует как электролит. Очень важно, чтобы уровень жидкости никогда не опускался ниже верха пластин. Если электролит в аккумуляторе падает ниже этого уровня, пластины подвергаются воздействию воздуха, начинается химический процесс, называемый сульфатированием (сульфатацией). Этот процесс может значительно сократить срок службы батареи, поскольку он мешает нормальной работе ее элементов. При этом серная кислота в электролите поглощается свинцовыми пластинами при разрядке батареи, а затем высвобождается обратно в электролит, когда батарея заряжается.
Почему в АКБ можно добавлять только чистую воду?
Добавление в батарею чего-либо, кроме воды, может мгновенно нанести ей повреждения. Например, пищевая сода может нейтрализовать серную кислоту, присутствующую в электролите батареи.
Очевидно, что вода сама по себе не является электролитом, поэтому добавление только воды в батарею на первый взгляд может показаться плохой идеей. Электролит – смесь из воды и серной кислоты, поэтому более логичным кажется долить в батарею серную кислоту, помимо обычной воды. Однако, причина, по которой в батарею нужно добавлять только воду заключается в том, что, когда свинцово-кислотная батарея теряет воду, она не теряет серную кислоту. Вода естественным образом исчезает в процессе электролиза в результате испарения, особенно в жаркую погоду, в то время как серная кислота никуда не денется, или ее объем будет теряться с гораздо меньшей скоростью.
Электролит – смесь из воды и серной кислоты, поэтому более логичным кажется долить в батарею серную кислоту, помимо обычной воды. Однако, причина, по которой в батарею нужно добавлять только воду заключается в том, что, когда свинцово-кислотная батарея теряет воду, она не теряет серную кислоту. Вода естественным образом исчезает в процессе электролиза в результате испарения, особенно в жаркую погоду, в то время как серная кислота никуда не денется, или ее объем будет теряться с гораздо меньшей скоростью.
Простой способ понять, как это работает, — вспомнить о том, что происходит, когда вы кипятите кастрюлю с соленой водой. Вода испаряется, но соль остается. Если вы добавите в кастрюлю обычную воду, она смешается с солью, и у вас снова будет соленая вода. То же самое происходит, когда вы добавляете дистиллированную воду в свинцово-кислотную батарею. Единственное исключение — если уровень жидкости низкий из-за опрокидывания аккумулятора. Когда это происходит, весь раствор серной кислоты и воды вытекает.
Все необходимые автозапчасти можно приобрести в магазине IXORA, а подобрать подходящую деталь могут профессиональные менеджеры.
| Производитель | Номер детали | Наименование |
|---|---|---|
| HYUNDAI | 371102E000 | Аккумулятор KIA 371102E000 |
| BOSCH | 0092S50050 | Аккумулятор Bosch 0092S50050 |
| BOSCH | 0092S50130 | Аккумулятор Bosch 0092S50130 |
| BOSCH | 0092S30060 | Аккумулятор Bosch 0092S30060 |
| BOSCH | 0092S40040 | Батарея аккумуляторная Bosch 0092S40040 |
| BOSCH | 0092S40050 | Аккумулятор BOSCH 0092S40050 |
| BOSCH | 0092S40060 | Аккумулятор Bosch 0092S40060 |
| BOSCH | 0092S40080 | Аккумулятор Bosch 0092S40080 |
| BOSCH | 0092S40090 | Аккумулятор BOSCH 0092S40090 |
| BOSCH | 0092S40100 | Аккумулятор BOSCH 0092S40100 |
| BOSCH | 0092S40230 | Аккумулятор Bosch 0092S40230 |
| BOSCH | 0092S40240 | Автомобильный аккумулятор BOSCH 0092S40240 |
| 0092S40250 | Аккумулятор Bosch 0092S40250 | |
| BOSCH | 0092S40270 | Аккумулятор Bosch 0092S40270 |
| BOSCH | 0092S40280 | Аккумулятор BOSCH 0092S40280 |
* Применяемость деталей конкретно для Вашего автомобиля уточняйте у менеджеров по телефону: 8 800 555-43-85 (звонок по России бесплатный).
Полезная информация:
- Импульсные зарядные устройства для автомобильных аккумуляторов
- Как правильно «прикурить» автомобиль?
- Почему горит лампочка зарядки аккумулятора: причины и неисправности
Получить профессиональную консультацию при подборе товара и подробную информацию по всем интересующим Вас вопросам можно позвонив по телефону — 8 800 555-43-85 (звонок по России бесплатный).
сколько доливать, если его стало мало
Аккумуляторная батарея (АКБ) в автомобиле используется в качестве дополнительного источника электроэнергии. С помощью неё производится запуск двигателя, и при включённом зажигании осуществляется работа всех бортовых приборов. Зачастую многие водители совершают большую ошибку, когда думают, что можно долить электролит в аккумулятор при его понижении, ведь, возможно, причина кроется в обычном испарении воды.
Содержание
- Дистиллированная вода или электролит
- Подготовительные работы
- Техническое обслуживание аккумулятора
Дистиллированная вода или электролит
Если самостоятельно изучить техническую литературу, то можно без особого труда понять, что во время работы аккумулятора из него испаряется некая часть жидкости, благодаря чему снижается уровень электролита над пластинами, а плотность кислоты в несколько раз увеличивается.
Поэтому можно сделать вывод, что недостаточный уровень электролита в батарее при её ежедневной эксплуатации оказывает значительное влияние на состояние пластин и скоропостижно снижает срок годности. Только при постоянной поддержке необходимого уровня кислоты уменьшается негативное действие повышенной плотности на аккумуляторную батарею.
Многие опытные механики знают о том, когда можно добавить электролит в аккумулятор, но чаще всего они заливают туда дистиллированную воду, ведь кислота не имеет свойства испаряться при кипении, поэтому из аккумулятора выходит наружу лишь кислород с водородом.
Важно помнить о том, что если в аккумуляторе мало электролита из-за его потери, например, разлился при открытых крышках, то именно в этом случае можно смело заливать его в горловины.
А также бывает, что проводя проверку плотности во всех отсеках аккумулятора, замечается её пониженное значение. Из этого можно с полной уверенностью сделать вывод о том, что произошла частичная сульфатация батареи.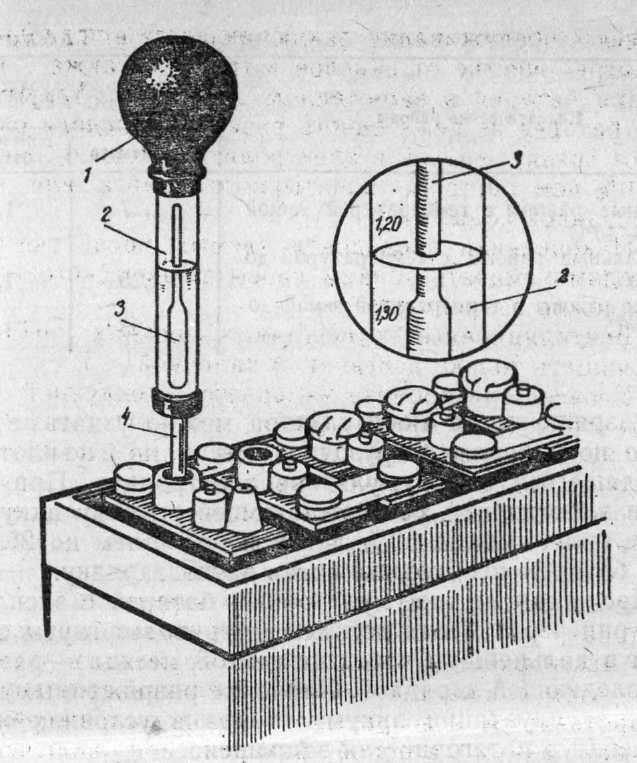 Когда количество электролита становится меньше за счёт кристаллизации серы на пластинах, то в этой ситуации аккумулятору просто необходимо срочное восстановление.
Когда количество электролита становится меньше за счёт кристаллизации серы на пластинах, то в этой ситуации аккумулятору просто необходимо срочное восстановление.
Подготовительные работы
Перед обслуживанием батареи следует изучить инструкцию, в которой полностью описано, как правильно доливать электролит в аккумулятор, а также важно прочитать инструкцию о зарядке.
Для того чтобы правильно долить электролит в аккумулятор, важно приготовить рабочее место, где будет проходить эта операция.
Также не стоит пренебрегать техникой безопасности:
- Первое, что нужно сделать — это надеть на себя спецодежду, которая включает в себя комплект штанов, куртки, прорезиненых перчаток и защитные очки.
- Поставить на верстак батарею и очистить её от различной грязи с помощью ветоши. Основное внимание нужно уделить плюсовому и минусовому контакту.

- Проверить батарею мультиметром.
- Аккуратно открыть крышки с помощью крестовой отвёртки.
Техническое обслуживание аккумулятора
После ряда этих манипуляций, обеспечивающих удобное обслуживание, специалисты проводят полную диагностику технического состояния аккумулятора. В основном они заключаются в шести пунктах:
- Перед тем как решить, что доливать в АКБ: электролит или воду, нужно обязательно полностью зарядить его специальным устройством.
- Далее произвести замер плотности во всех банках с помощью ареометра и зафиксировать все результаты в блокноте. При фиксировании показаний было бы удобнее проставить каждой банке свою цифру и напротив неё указать значение со шкалы.
- Если показания плотности у заряженного аккумулятора в некоторых банках различаются и не входят в рекомендуемую норму (1.25−1.29 г/куб. см), то это означает, что водителю нужно провести корректировку.
 Она заключается в следующем: при пониженном показании плотности нужно рассчитать, сколько доливать электролита в аккумулятор и залить его, а при повышенном залить дистиллированную воду.
Она заключается в следующем: при пониженном показании плотности нужно рассчитать, сколько доливать электролита в аккумулятор и залить его, а при повышенном залить дистиллированную воду. - Плотность каждой банки в предельных значениях, а уровень электролита по какой-то причине опускается всё ниже. Лучшим решением для этой проблемы будет банальная доливка воды.
- Иногда бывает так, что плотность в секциях ниже номинального значения (меньше 1.21 г/куб. см). Чтобы найти решение, нужно забрать с помощью специальной клизмы небольшой раствор кислоты и слить его в мерный стакан. Дальше записать показания объёма и перелить электролит в стеклянную кружку. Пользуясь технической таблицей, залить в мерный стакан нужное количество раствора серной кислоты с повышенной плотностью и с помощью клизмы влить в ту банку, из которой забирался электролит. В тех ситуациях, когда есть значительная разница в сторону уменьшения плотности, лучше всего доливать кислоту с плотностью 1.40 г/куб. см. Необходимый уровень важно достичь дистиллированной водой.

- После того как во всех банках плотность стала одинаковой, необходимо подключить аккумулятор на небольшую подзарядку. Это делается для того, чтобы недавно залитый раствор тщательно перемешался внутри. После этого снова измерить плотность, и если её уровень изменился, то провести повторную операцию.
Каждому автолюбителю нужно знать, что перед тем как перейти на зимнюю эксплуатацию автомобиля, важно повышать значения плотности в АКБ, а при переходе на летнее время — понижать.
А также ежедневно перед каждым выездом нужно проверять не только уровень масла в двигателе, но и чистоту клем батареи и надёжность крепления пробок на её корпусе.
Доливать электролит при низкой плотности
Множеству автомобилистов знакома такая проблема, как быстрая разрядка аккумулятора даже при отсутствии высокой нагрузки.
Встречаются совсем тяжёлые случаи — заряженный сегодня на 50% аккумулятор завтра же становится полностью разряженным и это обнаруживается во время попытки завести двигатель. Автомобилист заряжает аккумулятор на 100%, но завтра он снова наполовину разряжен. Как решить эту проблему? Покупка новой АКБ — это недёшево, но замена объективно требуется не в каждом случае, иногда достаточно проверки плотности и доливания электролита.
Множество автовладельцев волнует, насколько целесообразно доливание электролита в АКБ при недостаточной плотности. Возможно, лучше выполнить замену? Рассмотрим разные ситуации, чтобы выяснить, как лучше поступить в том или ином случае.
Когда доливание электролита в АКБ более целесообразно, чем замена АКБ?
Составляющими электролита любой АКБ являются кислота и дистиллированная вода. Данные жидкости образуют смесь, в составе которой преобладает вода, тогда как кислоты намного меньше. К примеру, Вам нужен электролит, плотность которого должна составлять 1,28 г/куб. см. В этом случае в 1 л дистиллированной воды необходимо влить 0,36 л кислоты. Пропорция будет составлять примерно 1:3.
см. В этом случае в 1 л дистиллированной воды необходимо влить 0,36 л кислоты. Пропорция будет составлять примерно 1:3.
Для безопасности требуется заливание кислоты в воду, но ни в коем случае не на оборот! Поскольку в противном случае имеет место высокий риск химической реакции, сопровождаемой выделением тепла и разбрызгиванием. Попадание аккумуляторной кислоты на кожу приводит к сильным ожогам. Причина этого заключается в более низкой плотности воды по сравнению с кислотой, вследствие чего эти жидкости смешиваются крайне медленно.
Объёмную пропорцию воды и кислоты выясняют с помощью ареометра. Этот прибор определяет плотность жидкости. После понижения плотности электролита до определённого значения он недостаточно хорошо удерживает заряд. При плотности немного ниже нужных 1,3 г/куб см, следует доливать электролит.
Изменение плотности электролита зависит заряда аккумулятора. По этой причине точную плотность аккумуляторной жидкости возможно только когда аккумулятор заряжен на 100%. Как правильно заряжать АКБ вы можете прочитать в отдельной статье.
Как правильно заряжать АКБ вы можете прочитать в отдельной статье.
%rtb-4%
Низкая плотность электролита — как решить проблему?
Если АКБ не держит заряд, нужна ли её замена? Целесообразно ли доливание электролита в случае недостаточной плотности? Или это всё равно не позволит восстановить работоспособность аккумулятора? Здесь всё определяется возрастом АКБ, а также показателями ареометра.
В случае, когда АКБ довольно старая (четыре года и более), потеря ею способности удерживать заряд прежде всего вызывается не недостатком плотности электролита, а разрушением пластин аккумуляторных банок. В подобной ситуации не поможет даже восстановление прежнего уровня плотности электролита. Но в случае сравнительной свежести аккумулятора решение проблемы возможно путём доливания электролита. Однако не всегда необходимо лить именно его.
Среднестатистическая плотность этой жидкости в исправном аккумуляторе — от 1,25 до 1,3 г/куб. см. Необходимо, чтобы эта величина была приблизительно одинаковой у всех аккумуляторных банок. Максимальное допустимое отклонение — 0,03. В случае, когда плотность ниже 1,25, однако выше 1,20, доливанием электролита можно будет устранить проблему.
Максимальное допустимое отклонение — 0,03. В случае, когда плотность ниже 1,25, однако выше 1,20, доливанием электролита можно будет устранить проблему.
Плотность жидкости менее 1,2 г/куб. см
Можно ли доливать электролит в данном случае?
Ответ: Да. Однако таким путём не удастся добиться восстановления работоспособности аккумулятора, поскольку при доливании электролита не выйдет довести плотность до 1,25 г/куб. см. При плотности в диапазоне 1…1,2, целесообразней долить аккумуляторную кислоту, поскольку её плотность намного выше плотности электролита.
Плотность жидкости менее 1 г/куб. см
Когда ареометр показывает плотность электролита менее 1 г/куб. см, даже доливанием кислоты решить проблему не получится. Но в случае, когда невозможно заменить аккумулятор, можно попытаться заменить электролит. Для выполнения этой операции требуется откачивание из всех аккумуляторных банок с помощью груши максимально возможного объёма жидкости с последующим укладыванием его набок. Потом высверлить в днищах всех аккумуляторных банок маленькие дырочки, диаметр каждой из которых должен составить три-пять мм. Промыть банки дистиллированной водой. После чего отверстия можно запаять (для этого подходит пластмасса, устойчивая к воздействию кислот, предварительно рекомендуется проверить её реакцию на электролит) и заливать во все банки новый электролит.
Потом высверлить в днищах всех аккумуляторных банок маленькие дырочки, диаметр каждой из которых должен составить три-пять мм. Промыть банки дистиллированной водой. После чего отверстия можно запаять (для этого подходит пластмасса, устойчивая к воздействию кислот, предварительно рекомендуется проверить её реакцию на электролит) и заливать во все банки новый электролит.
Однако даже в случае выполнения этой операции АКБ будет служить недолго, поскольку время эксплуатации определяется многими факторами. После полного сливания электролита, аккумуляторные банки в течение какого-то времени имеют контакты с кислородом, вследствие чего начинается быстрая коррозия. По этой причине долго эксплуатировать АКБ после полной замены электролита нежелательно, лучше заменить АКБ при первой появившейся возможности.
Как часто заряжать автомобильный аккумулятор?
Методики проверки уровня зарядки аккумулятора
Можно ли добавлять дистиллированную воду аккумулятор.
 Электролит или дистиллированную воду нужно доливать в аккумулятор
Электролит или дистиллированную воду нужно доливать в аккумуляторОчень часто, многие автолюбители от незнания совершают ошибку, добавляя электролит в аккумулятор, когда в нем понижается уровень жидкости. Почему делать это можно только в самом крайнем случае — мы разберем в данной статье.
Аккумуляторы теряют часть воды из электролита во время работы и заряда, при этом, происходит снижение его уровня над пластинами и увеличивается концентрация (плотность) кислоты. Соответственно, низкий уровень электролита при эксплуатации аккумулятора отрицательно влияет на ресурс батареи.
Чтобы восстановить уровень электролита, необходимо долить в аккумулятор дистиллированную воду. Если делать это своевременно, тогда снижается отрицательное воздействие повышенной плотности электролита на ресурс батареи.
Электролит доливать можно лишь в том случае, когда есть полная уверенность в том, что часть электролита была потеряна.
В процессе кипения, серная кислота почти вся остается внутри аккумулятора, выходит только лишь кислород с водородом, поэтому вместо испарившейся воды мы добавляем дистиллированную воду.
Если во всех банках полностью заряженного аккумулятора плотность не поднимается до необходимого уровня, с большой вероятностью можно предположить, что это частичная сульфатация аккумуляторной батареи. Концентрация электролита уменьшается за счет кристаллизации серы на пластинах и аккумулятору понадобится срочное восстановление. Доливка электролита здесь не поможет.
Существуют разные причины, по которым падает уровень электролита в АКБ, и каждую из них нужно рассматривать отдельно. Не всегда достаточно долить воды в банки и на этом успокоиться, но главное это то, что доливать в аккумулятор нужно только дистиллированную воду.
Электролит добавляйте лишь в крайнем случае, если причиной его низкого уровня является выплескивание. При этом важно отметить, что электролит добавляется при той же температуре и той же плотности, что и оставшийся в банках.
Правильная эксплуатация АКБ и своевременная добавка в него дистиллированной воды позволит вам избежать необходимости восстановления емкости, а также увеличит срок эксплуатации данного устройства.
Компания «4АКБ-ЮГ» предлагает большой выбор высококачественного оборудования собственной разработки для обслуживания аккумуляторных батарей различного типа и назначения. В каталоге нашего сайта представлены , а также устройства, которые вы можете купить по выгодной цене производителя.
Свинцовые автомобильные аккумуляторы накапливают энергию до тех пор, пока идет химическая реакция между электролитом и токопроводящими пластинами. При изменении плотности электролита, этот процесс нарушается. Неважно, по какой причине испортился электролит, аккумулятор не работает. Требуется замена электролита, корректировка плотности или приобретение новой АКБ. В случае если электролит приобрел черный цвет, в нем взвесь угля и окалины – аккумулятор придется менять.
Электролит представляет смесь серной кислоты с водой в определенной пропорции. О концентрации раствора узнают по плотности, измеряемой ареометром. Показатель основной, даже сотые доли влияют на способность электролита работать на накопление энергии.
Признаки негодного электролита:
Замена электролита в аккумуляторной батарее будет эффективна, когда полости банок обследованы, промыты, удален сульфатный осадок. Если разрушены пластины, осыпалось активное вещество – аккумулятор не ремонтопригоден.
В домашних условиях полная замена электролита в аккумуляторе автомобиля происходит в последовательности:
- Подготовить эмалированную или стеклянную посуду для слива электролита, средства личной защиты, место для работы, лучше, на открытом воздухе.
- Аккумулятор извлечь, из автомобиля, снять пробки или просверлить отверстия в необслуживаемом АКБ, слить жидкость в подготовленную тару, пользуясь грушей или шприцом.
- Аккумулятор промывается дистиллированной водой многократно, пока не удалится осадок. Возможно, придется удалять сульфат свинца, если есть осадок на пластинах. Нужно убедиться что активная замазка не осыпалась, угольная решетка цела.
- Медленно, с перерывами залить электролит нужной плотности в каждую банку выше пластин на 5-7 мм.
 Подождать 2-3 часа для выхода пузырьков, замерить плотность электролита, довести до нормы
Подождать 2-3 часа для выхода пузырьков, замерить плотность электролита, довести до нормы - Зарядку аккумулятора после замены электролита вести малым током 0,1 А, не допуская закипания. После набора половины емкости, зарядка ведется циклично.
- Произвести герметизацию банок.
Сколько времени заряжать аккумулятор? Заряжать аккумулятор после замены электролита нужно бережно, как после глубокой разрядки. Операция замены электролита своими руками в автомобильном аккумуляторе считается законченной, если он полностью принимает ток длительное время. Зарядка ведется осторожно, кипение в банках недопустимо.
Предлагаем посмотреть видео по правильной замене электролита в автомобильном аккумуляторе.
Почему нельзя доливать электролит в аккумулятор
Вы замерили уровень в банках аккумулятора, он ниже нормы? Это значит, что часть воды испарилась. Если это обслуживаемый аккумулятор, нужно замерить уровень в каждой банке и долить электролит до нормы водой. В необслуживаемом АКБ сквозь стенки видно зеркало залива.
В необслуживаемом АКБ сквозь стенки видно зеркало залива.
Упал уровень, значит в растворе мало воды и высокая плотность. Добавленный электролит повысит уровень, но плотность раствора останется высокой. Это пагубно для пластин АКБ, сокращается срок службы батареи. Поэтому следует электролит доводить до уровня, доливая дистиллированную воду.
Посмотрите видео о правилах замены электролита.
В каких случаях доливать электролит в аккумулятор?
Электролит в аккумулятор доливают, когда снижается емкость. При этом замеры ареометром содержимого каждой банки показывают снижение плотности. Возможно, в АКБ произошла сульфатация, связанный кислотный остаток в PbSO4 не участвует в реакции.
Если электролит, извлеченный из банок прозрачный, светлый, его можно использовать вторично, добавив корректирующий раствор, плотностью 1,4 г/см3. После снятия осадка на пластинах, батарея заливается прежним электролитом, но он низкой концентрации. Можно ли довести раствор до нужной плотности, доливая электролит? Какой состав взять, и сколько нужно долить в аккумулятор корректирующего раствора?
По технологии нужно заменить порцию слабого состава крепким. Долить и изъять электролит из банок раствор можно, воспользовавшись грушей и мерным цилиндром. Как поменять растворы, в какой пропорции видно из таблицы.
Долить и изъять электролит из банок раствор можно, воспользовавшись грушей и мерным цилиндром. Как поменять растворы, в какой пропорции видно из таблицы.
При этом следует использовать только электролит для корректировки. После операции замены, в течение получаса ведется подзарядка, чтобы жидкости смешались. Через два часа после отключения ЗУ проверяется плотность, если нужно, корректировка повторяется.
Предлагаем ознакомиться на видео, как долить электролит в аккумулятор.
Что доливать в аккумулятор, воду или электролит
При соблюдении условий эксплуатации, необслуживаемые аккумуляторы не требуют контроля плотности и уровня электролита. Обслуживаемые АКБ имеют специальные пробки – доступ к каждой банке. В них регулярно проверяются показатель качества и уровня электролита. Запас энергии батареи определяется по самому слабому элементу. Поэтому необходимо поддерживать плотность электролита во всех банках равной.
Плотность в банке может снизиться, если началась сульфатация. Тогда добавка электролита не поможет. Сильное сопротивление забитых пластин не пропускает заряд, добавленная кислота увеличит отложения. В этом случае заряд восстановит сульфатирование. Вот почему нельзя в АКБ с налетом сульфата свинца доливать электролит.
Тогда добавка электролита не поможет. Сильное сопротивление забитых пластин не пропускает заряд, добавленная кислота увеличит отложения. В этом случае заряд восстановит сульфатирование. Вот почему нельзя в АКБ с налетом сульфата свинца доливать электролит.
Доливать ли воду в аккумулятор? Если уровень электролита в банках низок, это указывает на интенсивное кипение батареи во время работы. Испаряется в основном водород. С оголенных пластин может осыпаться активная замазка, произойдет сульфатирование, коррозия. Поэтому подлить дистиллированную воду необходимо, но после этого аккумулятор нужно ставить на зарядку по полному циклу.
В период восстановления емкости частично разрушаются кристаллы свинца, происходит разбавление плотного раствора, происходит восстановление активности электролита. Доливают электролит или воду в АКБ в отверстия, прикрытые пробками, малой струей через воронку. Зарядку начинают не сразу, чтобы вышел воздух, смешались составы.
Контроль плотности следует произвести через полчаса после отключения ЗУ. При отклонениях плотности выполнить корректировку.
При отклонениях плотности выполнить корректировку.
Когда доливать в электролит, а когда воду
Вопрос, чем долить, если мало электролита в банках аккумулятора требует особого освещения. Такие жидкости, как электролит или дистиллированная вода, нужно заливать в аккумулятор правильно. Корпус и воронка должны быть чистыми, заливаемая жидкость прозрачная, без взвеси. Долить электролит водой можно, используя медицинский шприц без иглы, если корректировка требуется незначительная.
В каких случаях можно доливать воду в электролит аккумулятора? Если в одной или нескольких банках уровень электролита в АКБ низкий. Это происходит из-за кипения банок в условиях повышенной температуры или глубокого разряда. Добавлением дистиллированной воды восполняются потери объема, уменьшается плотность электролита, предотвращается скорый износ батареи.
Нужно ли заряжать аккумулятор после добавления воды, или замены электролита? Любое изменение внутреннего баланса требует выравнивания и стабилизации. После изменения концентрации жидкости необходимо провести полный цикл зарядки, убедиться, что аккумулятор не потерял емкость, стабильно напряжение на клеммах, обеспечивает пусковой ток.
После изменения концентрации жидкости необходимо провести полный цикл зарядки, убедиться, что аккумулятор не потерял емкость, стабильно напряжение на клеммах, обеспечивает пусковой ток.
Можно ли долить электролит в аккумулятор, если случайно его выплеснули? Как это случилось? Возможно, перевернули прибор. Это один из немногих случаев, когда вытекший электролит заменяют точно таким же и даже температуру подгоняют. Но все равно потребуется подзарядка и проверка плотности.
Посмотрите видео, как правильно долить электролит в аккумулятор. Вода или электролит, что доливать?
Как долить электролит в необслуживаемый аккумулятор
Все намного сложнее, если потребовалось долить воду в электролит необслуживаемого аккумулятора автомобиля. Сквозь полупрозрачные стенки можно увидеть, сколько электролита в банках. Но как проникнуть в корпус необслуживаемого аккумулятора?
Есть модели, проникнуть внутрь в которых можно отрезав болгаркой верхнюю крышку. Но такие действия нужны, если нужно удалить накипь и промыть осевший внизу шлам. Для того чтобы долить жидкость до нужного уровня сверлят отверстие в корпусе. Позже его заклеивают эпоксидным клеем.
Для того чтобы долить жидкость до нужного уровня сверлят отверстие в корпусе. Позже его заклеивают эпоксидным клеем.
Полностью необслуживаемый аккумулятор требует бережного обращения, боится глубоких разрядов и нестабильной работы бортовой АКБ. Заявленные 5-7 лет он выдерживает только в идеальных условиях.
Как разобрать необслуживаемый аккумулятор чтобы долить электролит
В современных АКБ, таких как VARTA, под декоративной наклейкой можно увидеть 6 пластинок, плотно утопленных в корпус. Если подковырнуть кружок шилом, можно под ним обнаружить пробку резиновую. Тогда появится возможность отобрать пробу электролита, провести замер плотности, откорректировать состав. Если нет пробки – в каждой банке колется отверстие тонким шилом, а вода запускается из шприца, каплями.
Но если обнаружено, что в банках на пластинах белесые полосы – это сульфатация. Чтобы очистить полости, убрать осадок внизу, потребуется вскрыть крышку распиливанием.
Посмотрите видео, как долить электролит в необслуживаемый аккумулятор.
Долить электролит в гелевый аккумулятор
Долить воду в банки аккумулятора просто. Нужно снять наклейку на корпусе, снять колпачки-клапаны и закапать в каждую банку по 1,2 мл воды. Вода должна впитаться в желеобразную массу. Нужно время. Через полчаса, если вода выше поверхности пластин батареи – извлеките ее фильтром или шприцом.
Аккумулятор является неотъемлемой составляющей практически любого современного устройства или автомобиля. Батарея, как и все узлы автомобиля, требует ухода и соблюдения рекомендаций при эксплуатации – одним из правил, которое нужно соблюдать, является, отслеживание уровня дистиллированной воды в АКБ.
Она требуется для нормального прохождения всех химических процессов, протекающих в аккумуляторе. Когда уровень падает, то можно заливать дистиллированную воду в аккумулятор самостоятельно. Как это сделать своими руками? Сколько доливать? Как отследить уровень?
В любом аккумуляторе протекают химические процессы, и воды может расходоваться по различным причинам: испарение в жаркую погоду, перезарядка, повышенные температуры в пространстве «под капотом».
Дистиллированная вода – одна из основных составляющих, для полноценной работы аккумулятора. Именно благодаря смешиванию электролита и воды, достигается оптимальная плотность раствора в 1.27 г/см 3 .
Узнай время зарядки своего аккумулятора
Электролит составляет около 35-36% от общего объёма жидкости внутри батареи, а остальное всё – вода.
Важно: если в АКБ пониженная плотность смеси, то это может привести к быстрому разряду и замерзанию раствора – значит, машина завестись не сможет. Если плотность повышенная – может привести к «обезвоживанию», что тоже негативно отразится на свойствах аккумулятора (пластины начнут разъедаться). В регионах, где сильные морозы (более -35 о С) допускается плотность смеси в 1.29 г/см 3 .
Дистиллированная вода является абсолютно чистым продуктом, без каких-либо примесей, Когда в воде имеются различные примеси (например соль, хлор), то это неизбежно приведёт к оседанию примесей внутри аккумулятора – это грозит уменьшением общей ёмкости батареи.
Почему такое соотношение
Вода при эксплуатации может испаряться, поэтому больший объём внутри батареи занимает именно она. Чтобы не попасть в ситуацию, когда необходимо долить воды, а её «под рукой» нет, рекомендуется возить с собой дистиллированную воду (хотя бы 1 литр).
Важно: уровень дистиллированной воды в аккумуляторе должен быть выше пластин (иначе им грозит перегрев и осыпание).
Сколько это в процентном соотношении? Приблизительно 65% от смеси электролита.
Как залить
Обслуживаемые
Немного долить или залить дистиллированную воду в аккумулятор (обслуживаемый) проблемой не является, и возможно осуществить процесс своими руками:
- Необходимо приобрести дистиллированную воду (лучше всего в аптеке).
- Откручиваются пробки, чтобы был виден электролит и пластины – если уровень смеси ниже пластин, то необходимо шприцом залить воду, до уровня, пока пластины не окажутся закрытыми (уровень электролита и воды должен превышать пластины на 1-1.
 5 см).
5 см). - После добавления необходимо поставить аккумулятор на зарядку.
Необслуживаемые
Можно ли долить дистиллированную воду в необслуживаемый аккумулятор? Ответ однозначен – можно, но сделать это тяжелее, чем в обслуживаемом типе АКБ (заводом производителем процесс не предусмотрен).
Прежде всего, нужно отметить, что доливать воду в АКБ необслуживаемого типа необходимо гораздо реже. Обусловлено тем, что батареи этого типа хорошо герметизированы, и внутри используется «кольцевая технология», что позволяет снизить испарение до минимума. Срок работы аккумулятора без лишних манипуляций составляет около 4-5 лет.
Процесс заливания:
- Необходимо определить уровень электролита – для этого необходимо потрясти АКБ, и по звукам определить приблизительный уровень. Когда ощущение подсказывает, что уровень в норме – возможно, произошла сульфатация пластин и заливать воду бессмысленно.
- Необходимо определить уровень пластин – если аккумулятор не прозрачный, то придётся определять «на глаз», в других батареях можно подсветить фонариком или покупать аккумуляторы в прозрачном корпусе.

- Делается отступ от пластин максимум на 2 см вверх, помечается, и сверлом (2-3 мм) делается отверстие.
- Набирается шприц с дистиллированной водой и заливается до момента, пока вода не начнёт выливаться из сделанного отверстия.
- Батарея перекладывается на другой бок, и сделанные отверстия запаиваются самым обыкновенным паяльником.
- Ставится на зарядку, и заряжается до полного уровня.
Процесс сложный, и много не точных действий, но не стоит забывать – доливание воды в необслуживаемый аккумулятор производителем не предусмотрено!
Процесс заливания дистиллированной воды в аккумулятор можно увидеть на видео.
Объём
Сколько доливать дистиллированной воды в аккумулятор? Какой уровень допустим? Доливать необходимо до момента, пока пластины не скроются, и не будут видны. Переводя значения в цифры – количество воды зависит от общей ёмкости аккумулятора, поэтому нужно ориентироваться на скрытие пластин электролитом на 1. 5-2 см. Именно при таком уровне достигается необходимая плотность электролита в 1.27 г/см 3 .
5-2 см. Именно при таком уровне достигается необходимая плотность электролита в 1.27 г/см 3 .
Важно: если при доливании воды уровень окажется превышенным, то понизится плотность, и появится возможность «замерзания» аккумулятора зимой. Когда уровень превышен – можно откачать воду, используя шприц, которым производилось доливание.
Итогом можно сказать, что доливать воду в обслуживаемые аккумуляторы – прямая необходимость. С необслуживаемыми аккумуляторами ситуация другая – зависит только от желания автовладельца. Но в любом случае необходимо помнить, что доливание воды – временная мера! Спустя некоторое время он всё равно придёт в негодность, и придётся покупать новый.
Довольно часто начинающих автомобилистов волнует вопрос о том, что такое дистиллированная вода и для чего ее следует доливать в аккумулятор автомобиля в любое время года. При этом некоторые люди указывают на то, что от дистиллята может быть больше вреда, чем пользы, хотя эта информация не доказана.
Стоит попробовать разобраться с тем, что будет с АКБ, если налить в нее обычную водопроводную воду, и сколько дистиллированной воды придется налить для правильной работы агрегата. Профессиональные водители, которые прекрасно разбираются во всех тонкостях состава электрохимических жидкостей в аккумуляторе.
Профессиональные водители, которые прекрасно разбираются во всех тонкостях состава электрохимических жидкостей в аккумуляторе.
Дистиллированная вода – часть электролита, без которой нельзя приготовить жидкость электрохимического типа, поскольку она может создать состав необходимой плотности и прибавить полезные свойства. В том случае, если не долить эту воду в АКБ, то агрегат не будет работать максимально правильно.
Дело в том, что электролит состоит из тридцатипроцентной серной кислоты и шестидесяти пяти процентов дистиллята. Конечно же, ясно, что кислота в чистом виде просто-напросто разъест пластины свинца и вывела бы из строя автомобильный аккумулятор. Именно дистиллированная вода помогает существенно снизить концентрацию серной кислоты, позволив аккумулятору работать правильно.
Узнай время зарядки своего аккумулятора
Согласно школьному курсу химии можно понять, что дистиллированная вода – чистейшее вещество, в котором не имеется никаких примесей и солей. Стоит отметить, что водопроводная вода вместо дистиллированной в аккумулятор заливаться не должна, поскольку она далека от идеала. В такой жидкости не только много примесей и солей, но и опасный элемент – хлор.
Стоит отметить, что водопроводная вода вместо дистиллированной в аккумулятор заливаться не должна, поскольку она далека от идеала. В такой жидкости не только много примесей и солей, но и опасный элемент – хлор.
В том случае, если залить водопроводную воду вместо дистиллированной, то примеси осядут на свинцовые пластинки, а емкость аккумулятора существенно понизится. Значит, вода из-под крана является губительной для АКБ, и залить ее в агрегат – значит окончательно погубить его.
Как рассчитать объем доливаемой воды
Чтобы обеспечить правильную работу автомобильного аккумулятора, стоит понять, сколько понадобиться залить дистиллированной воды. По технической документации соотношение кислоты к дистилляту составляет не более, чем 1:2. Чтобы уточнить, сколько доливать дистиллированной воды в автомобильный аккумулятор, стоит понять, сколько в нем находится кислоты.
Почему важно будет правильно рассчитывать объем доливаемой воды:
- кислоты должно быть много, поскольку расходуется она при разрядке АКБ, способствуя падению уровня электролита и появлению солей на свинцовых пластинках;
- в том случае, если аккумулятор заряжается, то уровень дистиллированной воды падает, увеличивая плотность кислоты, поэтому плотность большинства аккумуляторов составляет 1,27 г/см3;
- если же кислоты не будет столько, сколько необходимо, то электролит при пониженной уровне температуры воздуха превратится в лед;
- в том случае, если долить в домашних условиях больше кислоты, чем воды, то она разрушит пластины.

Соотношение кислоты к воде, как 1 к 2 выведено много лет назад экспериментальным путем, поэтому изменять его в любую сторону строжайше запрещено. Каждый автовладелец обязан знать, сколько дистиллированной воды в аккумуляторе, чтобы своевременно долить ее своими руками до требуемого уровня.
Правила добавления дистиллята в АКБ
Следует ознакомиться с правилами добавления дистиллята при помощи видео, чтобы долить дистиллированную воду в аккумулятор правильно и не навредить автотранспортному средству:
Для того, чтобы долить дистиллированную воду правильно, следует определить, какой уровень электролита в АКБ, при помощи специальной трубки, диаметр которой составляет не менее, чем пять миллиметров.
Чтобы добиться необходимого уровня электролита, следует набрать в двадцатикубовый шприц дистиллят и долить в каждую секцию АКБ по пять или десять миллилитров жидкости.
После того, как дистиллированная вода будет долита, аккумулятор придется зарядить, не прикрывая пробки банок, не менее четырех раз, чтобы восстановить емкость. Далее закрываются крышки, и АКБ отстаивается около двенадцати часов.
Далее закрываются крышки, и АКБ отстаивается около двенадцати часов.
Не стоит забывать, какая техника безопасности должна применять в процессе, поэтому нужно запастись защитными очками и перчатками, и не приближаться к открытым источникам огня.
Чтобы при выкипании электролита его плотность не увеличивалась в разы, необходимо своевременно доливать в аккумулятор дистиллированную воду. Как правильно долить дистиллированную воду в аккумулятор? Рассмотрим этот процесс более подробно.
Особенности заливки дистиллята
Перед тем, как приступать к процессу заливки дистиллята (электролита), аккумулятор необходимо подготовить. Его нужно отключить, вынуть, установить на ровную поверхность, очистить его от пыли и загрязнений. Очищение аккумулятора является обязательным пунктом, поскольку даже мельчайшие частицы грязи при попадании внутрь могут привести к его полному выходу из строя. Очистить аккумулятор проще всего раствором обычной пищевой соды.
Внутри источника тока есть специальные риски, указывающие на минимальный и максимальный уровень для дистиллята.
Для того, чтобы в аккумулятор не попала грязь, для заливки дистиллированной воды используйте обычный шприц. Он позволит налить жидкость не только абсолютно гигиенично, но и максимально точно.
После заливки закройте аккумулятор и установите его на место.
- Ни в коем случае не заливайте жидкость сразу после того, как вы отключили двигатель. Ему необходимо отстояться минимум шесть-восемь часов. Только после «отдыха» аккумулятор можно открыть и приступить к процессу заливки.
- После заполнения водой также нельзя сразу запускать аппарат в работу. Подождите хотя бы до утра следующего дня, иначе возможно закипание, которое приведет к фатальным последствиям.
- Дозаливка дистиллятом не сделает устройство новым, а просто немного улучшит его функционирование. Если аккумулятор уже израсходовал свой ресурс, то лучше заменить его на новый.
- Перед запуском аккумулятора в работу проверьте объем жидкости внутри. Можно начать его эксплуатацию только в том случае, если уровень воды — в пределах нормы.

- И ни в коем случае не используйте для дозаливки обычную воду, а только специальную дистиллированную, приобретенную в спец. магазинах в закрытой таре. При заливке обычной воды произойдет разрушение пластин и полный выход из строя аккумулятора.
- Заливка воды в аккумулятор должна производиться при комнатной температуре в закрытом помещении.
Дистиллированную воду или электролит: что доливать в аккумулятор
Правильный уровень электролитической жидкости во много определяет срок службы аккумулятора. Но следить нужно и за уровнем, и за плотностью раствора серной кислоты. В статье мы ответим на вопрос, что заливать, как отличить дистиллированную воду от обычной, чтобы своими действиями не сократить ресурс АКБ.
Почему АКБ нуждается в обслуживании?
Электролит — смесь серной кислоты и дистиллированной воды, которая вступает в химическую реакцию с активной массой отрицательных и положительных пластин. При разряде свинцово-кислотного аккумулятора из электролитической жидкости расходуется серная кислота и вода, в результате чего снижается плотность электролита. При обратном процессе, когда аккумулятор заряжается, количество свинца на электродах может снизиться настолько, что внутри батареи начинает преобладать процесс электролиза воды. Описанное выше «кипение» возникает при перезаряде аккумулятора, а результатом выделения газообразного водорода и кислорода становится повышение плотности электролита.
При обратном процессе, когда аккумулятор заряжается, количество свинца на электродах может снизиться настолько, что внутри батареи начинает преобладать процесс электролиза воды. Описанное выше «кипение» возникает при перезаряде аккумулятора, а результатом выделения газообразного водорода и кислорода становится повышение плотности электролита.
Перезаряд опасен не только выкипанием воды, но и взрывом образующихся внутри корпуса аккумулятора газов. Поэтому нужно следить за исправностью системы зарядки автомобиля. В случае заряда от внешнего устройства следует приоткрутить сервисные пробки и правильно выставлять ток зарядки.
Подготовленный материал главным образом относится к малосурмянистым свинцово-кислотным аккумуляторам (Sb/Sb). АКБ такого типа из-за невысокой стоимости получили наибольшее распространение, но владельцам стоит помнить о недостатках: высокий саморазряд и снижение плотности вследствие вскипания воды. Некоторые кальциевые аккумуляторные батареи (Ca/Ca) также нуждаются в плановом обслуживании, что обязательно указывает производитель в инструкции по эксплуатации.
В каких случаях следует долить электролит?
- Линейный перезаряд. Причина в неисправной системе зарядки автомобиля, вследствие чего происходит вскипание электролитической жидкости. Проверить систему зарядки можно мультиметром. Уровень заряда на холостом ходу и при перегазовках не должен превышать 14,8 В. Если вы заметили на корпусе потеки и окисление на металлических поверхностях вблизи батареи, после устранения причины неисправности обязательно проверьте уровень и плотность электролитической жидкости. Продолжительная эксплуатация АКБ при перезаряде опасна оголением пластин, вследствие чего они нагреваются и теряют активную массу, происходит реакция сульфатации. На внутренней части пробок при этом можно увидеть темный налет. Лучше не пытаться оживить батарею доливкой электролита, а заменить аккумулятор.
- Течь электролита из одной из банок вследствие повреждения корпуса. Трещины, сколы чаще всего возникают из-за механических повреждений или замерзания воды внутри корпуса в сильный мороз.
 Если степень повреждений незначительная, корпус можно отремонтировать. В таком случае следует правильно определить соотношение электролита и дистиллированной воды в аккумуляторе. Если аккумулятор был поврежден до использования, надо залить электролит с такой же плотностью, которая осталась в поврежденной банке. Если АКБ использовался в поврежденном состоянии, долейте и электролит, и воду, сравняв плотность поврежденной и соседней секций.
Если степень повреждений незначительная, корпус можно отремонтировать. В таком случае следует правильно определить соотношение электролита и дистиллированной воды в аккумуляторе. Если аккумулятор был поврежден до использования, надо залить электролит с такой же плотностью, которая осталась в поврежденной банке. Если АКБ использовался в поврежденном состоянии, долейте и электролит, и воду, сравняв плотность поврежденной и соседней секций. - Потеря электролита вследствие переворота или опрокидывания батареи.
- Ввод в эксплуатацию сухозаряженных аккумуляторов. Данная технология производства сохранила свою актуальность только для мотоциклов. Все автомобильные аккумуляторные батареи поставляются в готовом к использованию состоянии.
Измеряем плотность и уровень электролита
Чтобы понять, вашему аккумулятору нужна вода или электролит, важно правильно определить уровень жидкости и плотность внутри каждой банки. Уровень электролита не должен опускаться ниже верхней границы пластин. Для его визуальной проверки достаточно открутить сервисные пробки.
Для его визуальной проверки достаточно открутить сервисные пробки.
Шаг второй – измерение плотности. На полностью заряженном аккумуляторе плотность электролитической жидкости с температурой +20 °С должна составлять 1,27-1,29. Измерения проводятся специальным прибором – ареометром. Плотность зависит от температуры электролитической жидкости, поэтому при самостоятельной проверке в условиях, разнящихся с эталонными, следует пользоваться корректирующей таблицей. Суть диагностики в том, чтобы набрать небольшое количество электролита из каждой банки, после чего оценить плотность по шкале на поплавке.
При продолжительном простое в разряженном состоянии аккумулятор следует заряжать малым током (5-7% от емкости). Большой ток зарядки приведет к реакции сульфатации. Даже при полной зарядке АКБ больше не будет соответствовать своим пусковым и емкостным характеристикам.
При сульфатации даже в заряженном состоянии плотность может не подняться выше 1,20. Такие изменения часто вводят автовладельцев в заблуждение, заставляя доливать корректирующий электролит, что неправильно. Сначала нужно провести детацию пластин. Определить можно по белому налету на пластинах.
Такие изменения часто вводят автовладельцев в заблуждение, заставляя доливать корректирующий электролит, что неправильно. Сначала нужно провести детацию пластин. Определить можно по белому налету на пластинах.
Если реакция детации отсутствует, то показатель ниже 1,27 говорит о необходимости заливки корректирующего электролита. И наоборот, если плотность выше, следует долить в аккумулятор воды.
Выбор дистиллята
Если заправить аккумулятор обычной водой (в том числе и собранной дождевой), активная масса пластин очень быстро придет в негодность. Чтобы продлить срок эксплуатации аккумулятора, используйте только качественную дистиллированную воду. Для проверки качества учитывайте простейшие характеристики дистиллята:
- электропроводность. Дистиллированная вода, в отличие от обычной, не проводит электрический ток. Проверить воду можно путем измерения сопротивления с помощью мультиметра – у дистиллята оно будет равно бесконечности;
- отсутствие следов после вскипания.
 Для теста капните воду на чистый лист А4 либо нагрейте ее на стеклянной поверхности/кусочке фольги. После испарения дистиллята на поверхности не должно остаться ореолов и пятен.
Для теста капните воду на чистый лист А4 либо нагрейте ее на стеклянной поверхности/кусочке фольги. После испарения дистиллята на поверхности не должно остаться ореолов и пятен.
Видео:КАК ДОЛИВАТЬ ЭЛЕКТРОЛИТ ИЛИ ВОДУ В АККУМУЛЯТОР | ЧТО ДЕЛАТЬ НЕЛЬЗЯ
Соотношение электролита к воде
Чтобы получить 1 литр электролитической жидкости плотностью 1,27-1,28, следует смешать 0,772 л корректирующего электролита и 0,295 л дистиллированной воды. При нормальной эксплуатации испаряется только вода, поэтому доливать электролит вместо дистиллята нельзя. Чтобы не ошибиться с плотностью, обслуживание проводят только после полной зарядки аккумулятора.
Перелив воды, при котором плотность опускается на уровень 1,26, считается некритичным. При снижении этой границы уже необходимо откачать часть жидкости, довести плотность до заводской, долив корректирующий электролит.
Меры предосторожности
Все действия с раствором серной кислоты и воды проводят в плотных резиновых перчатках. Не допускайте попадания электролита на оголенные участки кожи и слизистые оболочки. Помните о том, что раствор крайне агрессивен и к лакокрасочному покрытию автомобиля. При попадании на ЛКП обязательно промойте участки очистителем и большим количеством воды.
Не допускайте попадания электролита на оголенные участки кожи и слизистые оболочки. Помните о том, что раствор крайне агрессивен и к лакокрасочному покрытию автомобиля. При попадании на ЛКП обязательно промойте участки очистителем и большим количеством воды.
Электролит или дистиллированная вода для аккумулятора
К таким основным частям в ТС стоит отнести аккумулятор. При нормальном раскладе такая батарея заряжается во время работы автомобиля. Но нередки случаи, когда при неисправности других устройств в машине его необходимо заряжать при помощи специального устройства. Такие условия эксплуатации влияют на быстрый износ устройства. К тому же время от времени его необходимо заправлять. Многие часто путаются, что доливать в аккумулятор: воду или электролит. Какие функции выполняет это устройство, как определить в нем уровень, как и чем правильно заправить, разберемся в этой статье.
Понятие аккумулятора
Это специальный механизм, который используется в транспортном средстве непосредственно для его запуска и дальнейшей работы. Кроме этого, такое устройство призвано оптимизировать работу пиков напряжения в момент запуска транспортного средства.
Кроме этого, такое устройство призвано оптимизировать работу пиков напряжения в момент запуска транспортного средства.
Понятие электролита
Для эффективной работоспособности аккумулятора обязательно используется электролит. Он представляет собой раствор соляной кислоты и дистиллированной воды. Здесь не должны использоваться сторонние примеси. В противном случае это изменит его плотность. Для правильной работоспособности важен также и уровень электролита в аккумуляторе. Если он будет ниже положенной нормы, то в дальнейшем это неизбежно приведет к нестабильной работе вспомогательного источника электроэнергии транспортного средства, и владелец не сможет нормально завести машину. При этом высохнут внутренние пластинки, а мощность батареи значительно снизится. Также не стоит превышать достаточный уровень жидкости в системе. В противном случае в дальнейшем это приведет к полной или частичной поломке этого механизма. Батарея станет быстрее разряжаться. Поэтому уровень электролита в аккумуляторе обязательно должен быть стабильным. Это позволит обеспечить нормальную работу транспортного средства.
Это позволит обеспечить нормальную работу транспортного средства.
Когда необходима заправка аккумулятора
Согласно мнению многих специалистов, автомобильная батарея не подлежит техническому обслуживанию. Поэтому вопрос о том, что доливать в аккумулятор: воду или электролит – некоторые мастера считают неактуальным. Но это если он используется в нормальных условиях. Если автовладелец любит путешествовать на своем транспортном средстве на дальние расстояния, то он обязательно должен учесть данный параметр. В составе электролита обязательно используется водная масса. В процессе работы устройства она может испариться. Жидкость может начать активно переходить в парообразное состояние в случае полной и частичной неисправности реле-регулятора. К основным моментам неисправности механизма обязательно надо отнести:
- Появление сильного пара из заливных отверстий.
- Появление капель электролита на корпусе АКБ.
- Большой нагрев аккумулятора в процессе работы транспортного средства.

Также стоит учитывать тип батареи. Они бывают обслуживаемыми и необслуживаемыми. В первом случае испарение будет больше, поэтому именно для них актуален вопрос о том, что доливать в аккумулятор: воду или электролит. В необслуживаемых батареях жидкость находится в герметичном корпусе. Поэтому в процессе эксплуатации жидкость все же поднимается вверх, но не выходит за границы корпуса, и впоследствии снова опускается вниз, выпадая в осадок. В таких устройствах цикл замкнутый. Такие аккумуляторы не требуют проверки в них жидкости.
Способы проверки уровня электролита
Как отмечено ранее, такой проверки требуют только обслуживаемые аккумуляторы. К первому способу проверки обязательно надо отнести визуальный осмотр. Как правило, корпус батареи устройства делается прозрачным. Здесь ставятся различные отметки. Они указывают на уровень жидкости. Поэтому визуально можно отследить количество электролита в системе.
Но не все модели обслуживаемых аккумуляторов выполняются с прозрачным корпусом. В этом случае автовладелец может воспользоваться специальной прозрачной трубочкой, которая имеет диаметр 5 мм.
В этом случае автовладелец может воспользоваться специальной прозрачной трубочкой, которая имеет диаметр 5 мм.
Для проведения проверки:
- необходимо открутить крышку батареи;
- отпустить трубку в жидкость до упора;
- пальцем плотно зажать внешнее отверстие;
- достать трубку.
Уровень электролита должен соответствовать уровню его столба в такой трубке.
Что делать при несоответствии уровня электролита
Автовладелец должен знать, что уровень высоты жидкости в трубке должен быть в пределах 15 мм. Если эта норма превышена, то следует убрать лишний раствор. Для этого понадобится резиновая груша или шприц.
При низком показателе электролита в раствор можно залить воду. Доливают ли электролит в аккумулятор? Ответ на этот вопрос можно получить, проанализировав состав раствора в батарее. Как уже отмечалось, это вода и раствор соляной кислоты. В процессе эксплуатации испаряется только вода, поэтому она и доливается во время обслуживания. Но если плотность раствора слишком мала, то для ее повышения доливается кислота. Поэтому, отвечая на вопрос о том, что доливать в аккумулятор: воду или электролит – необходимо сначала измерить плотность раствора. Сделать это можно самостоятельно.
Но если плотность раствора слишком мала, то для ее повышения доливается кислота. Поэтому, отвечая на вопрос о том, что доливать в аккумулятор: воду или электролит – необходимо сначала измерить плотность раствора. Сделать это можно самостоятельно.
Проверка плотности электролита
Автовладелец обязан знать и о том, что, кроме уровня электролита, необходимо проверять и его плотность. Поэтому перед тем, как долить дистиллированную воду в аккумулятор, стоит обязательно проверить плотность раствора.
Сделать это можно специальным прибором под названием «ареометр». Он имеет форму поплавка. Он имеет соответствующую шкалу, градуированную в единицах плотности. Сверху расположен баллон. Именно в него поступает раствор. Уровень жидкости должен обеспечивать нормальное передвижение поплавка в вертикальном положении. Показатель плотности электролита в АКБ должен оставаться в пределах 1,25-1,3 г/куб. см. Когда уровень отклоняется в большую сторону, применяется дистиллированная водная масса. Если такой уровень отклонился в меньшую сторону, то используется специальный корректирующий электролит. Он значительно повышает плотность используемой жидкости в системе.
Если такой уровень отклонился в меньшую сторону, то используется специальный корректирующий электролит. Он значительно повышает плотность используемой жидкости в системе.
Как долить дистиллированную воду в аккумулятор
Если плотность выше нормы, это свидетельствует об испарении жидкости, которую необходимо добавить. Сколько воды доливать в аккумулятор? Уровень раствора в АКБ необходимо поддерживать на 1-1,5 см выше уровня пластин. Нельзя добавлять дистиллированную воду больше разрешенной нормы. После заправки обязательно следует повторно проверить плотность жидкости, предварительно зарядив батарею.
Заключение
На основании вышеизложенного обязательно надо сделать вывод о том, что для обеспечения нормальной работоспособности транспортного средства владелец обязательно должен отслеживать уровень электролита в аккумуляторе автомобиля. В ином варианте водитель просто не заведет свое транспортное средство. Уровень не должен отклоняться в большую или меньшую сторону. В дальнейшем это обязательно приведет к неисправностям в работе системы. Кроме отслеживания уровня электролита, надо внимательно следить и за его плотностью. Если установленный показатель отклоняется, нужно совершать определенные действия по увеличению или уменьшению уровня плотности в системе. Можно ли доливать воду в аккумулятор? Да, но только в том случае, если плотность раствора в АКБ выше нормы.
В дальнейшем это обязательно приведет к неисправностям в работе системы. Кроме отслеживания уровня электролита, надо внимательно следить и за его плотностью. Если установленный показатель отклоняется, нужно совершать определенные действия по увеличению или уменьшению уровня плотности в системе. Можно ли доливать воду в аккумулятор? Да, но только в том случае, если плотность раствора в АКБ выше нормы.
Приведем наиболее часто встречающиеся нарушения правил эксплуатации
(1) Заряд током чрезмерно большой силы, превышающим нормальный в несколько раз. Перегрев электролита, коробление электродов, реже — разрушение сепараторов, осыпание активной массы и т.п. Это обычно происходит при форсированных режимах заряда с использованием мощных зарядных устройств, особенно в условиях неконтролируемого заряда.
(2) Повышенное
напряжение в бортовой сети автомобиля приводит
к систематическому перезаряду. Снижается уровень электролита, повышается его плотность. Если долить до нормального уровня электролит, а не дистиллированную воду, аккумулятор очень быстро приходит в негодность. Если ничего не доливать, то сульфатация электродов обеспечена, обнаженные элементы электродов быстро корродируют, активная масса, особенно положительных пластин, набухает, выкрашивается, теряет механическую прочность, оплывает.Аккумулятор быстро снижает емкость, электролит становится мутным. В таких ситуациях аккумулятор может стать совершенно непригодным к эксплуатации.
Если долить до нормального уровня электролит, а не дистиллированную воду, аккумулятор очень быстро приходит в негодность. Если ничего не доливать, то сульфатация электродов обеспечена, обнаженные элементы электродов быстро корродируют, активная масса, особенно положительных пластин, набухает, выкрашивается, теряет механическую прочность, оплывает.Аккумулятор быстро снижает емкость, электролит становится мутным. В таких ситуациях аккумулятор может стать совершенно непригодным к эксплуатации.
(3) Перегрев аккумулятора. Известно, что при повышении температуры электролита выше +35 градусов активизируются процессы износа электродов, а если температура повышается еще выше, то ресурс аккумулятора сокращается катастрофически быстро. Эта ситуация нередка, например когда оставили автомобиль на солнце под тентом темного цвета.
(4) Загрязнение электролита. Аккумулятор необходимо протирать чистой мягкой тряпкой, смоченной в нашатырном спирте или растворе кальцинированной соды. Если хотя бы очень небольшая часть загрязняющих веществ попадает в электролит — аккумулятор обречен.
(5) Добавление в электролит недистиллированной воды
. Это довольно частая ситуация когда нет под рукой качественной дистиллированной воды, и доливают в электролит просто чистую воду. Электроды выходят из строя, а аккумулятор идет на склад вторсырья.
(6) Еще быстрее выходит из строя новая батарея, если для нее приготовить электролит на основе технической серной кислоты.
(7) Короткое замыкание может вывести АКБ моментально. Чаще всего это происходит при неосторожном обращении с инструментом вблизи батареи, или в результате повреждения изоляции силового кабеля.
(8) Пониженное напряжение бортовой сети — весьма распространенная ситуация.Аккумуляторная батарея хронически разряжена, понижена плотность электролита. Нередки случаи запредельных разрядов, например, после пуска двигателя стартером. Снижаются основные энергетические характеристики батареи, особенно в зимний период. Систематический недозаряд может привести к переполюсовке аккумулятора при эксплуатации.
(9) Размораживание аккумуляторной батареи. Моноблок лопается, электролит вытекает после оттаивания. Это происходит в сильные морозы при снижении плотности электролита ниже допустимых значений.Обычно такое происходит, если долить дистиллированную воду в электролит и не принять ни каких мер для того, чтобы она перемешалась с электролитом, или после нескольких безуспешных попыток пуска стартером холодного двигателя, оставив на морозе глубоко разряженный АКБ.
(10) Применение мощного пускового устройства. Если применять мощный неспециализированный источник тока для пуска холодного двигателя, то можно моментально «взорвать»
аккумуляторную батарею. При подключении этого устройства к батарее сила тока заряда может быть настолько большой, что электролит бурно вскипает, и вентиляционные отверстия не в состоянии сбросить выделяющиеся газы.
(11) Запредельный разряд стартерными токами. Часто при затруднённом пуске двигателя аккумулятор разряжают до такой степени, что якорь стартера перестает проворачиваться. Такие глубокие разряды приводят к тому, что пластины очень быстро коробятся, осыпаются, и батарея выходит из строя.
Такие глубокие разряды приводят к тому, что пластины очень быстро коробятся, осыпаются, и батарея выходит из строя.
(12) Повышенная плотность электролита. По разным причинам в аккумуляторе расходуется вода, понижается уровень и повышается плотность электролита, и если не доливать дистиллированную воду аккумулятор разрушится.
Самый простой путь вывести из строя аккумулятор — долить в него обычную воду
, содержащую соли металлов и прочие примеси. Применение такой воды нарушает, во-первых, плотность, во-вторых, химический состав электролита.
Удивительно, но чаще всего, когда в аккумуляторе закипает жидкость или батарея и вовсе выходит из строя, меньше всего автовладельцы склонны винить электролит или якобы дистиллированную воду, которую недавно доливали. А ведь в большинстве случаев это — главная и единственная причина.
Как известно, дистиллят — это вода, не имеющая никаких примесей — «аш два о» и ничего больше. Дистиллированная вода — это диэлектрик. Проверить это просто: взять тестер и «прозвонить» воду на «обрыв».
Проверить это просто: взять тестер и «прозвонить» воду на «обрыв».
Чистая вода покажет бесконечное сопротивление. Попробуйте таким способом проверить пару-тройку повсеместно продающихся бутылок с якобы дистиллированной водой. Вы будет неприятно удивлены — в бутылках окажется все, что угодно, но только не дистиллированная вода. Доливать такую воду в аккумулятор — самый верный способ угробить его.
Не каждый, впрочем, может вооружиться тестером и проводить подобные контрольные замеры. Что ж, есть и более простой способ. Достаточно обратить внимание на тару и этикетку. Если перед вами неоригинальная бутылка (например, из-под «Колы» или минеральной воды) с этикеткой, на которой отсутствуют данные о производителе, вероятно, стоит насторожиться. Ведь предъявить претензии в случае покупки некачественного продукта будет некому.
Печально, но подобная ситуация на рынке и с электролитом. В большинстве случаев автовладельцу предлагаются все те же сомнительные бутылки с «анонимными» этикетками. Плотность, правда, указана. Но соответствует ли действительности эта информация? Знают ли производители таких жидкостей о существовании ГОСТ 667-83А, в котором указаны все необходимые требования к электролиту? А если и знают, соблюдают ли их? Опять же, если на этикетке отсутствуют данные о производителе, кому предъявлять претензии в случае чего?
Плотность, правда, указана. Но соответствует ли действительности эта информация? Знают ли производители таких жидкостей о существовании ГОСТ 667-83А, в котором указаны все необходимые требования к электролиту? А если и знают, соблюдают ли их? Опять же, если на этикетке отсутствуют данные о производителе, кому предъявлять претензии в случае чего?
Электролит представляет собой жидкость состоящую из серной кислоты и дистиллированной воды. В некоторых ситуациях уровень электролита в аккумуляторе падает и требуется его нормализовать. В зависимости от причин снижения уровня в батарею доливают либо электролит, либо дистиллированную воду. Как же узнать, что именно залить в АКБ?
В аккумулятор доливают электролит, если падение его уровня вызвано повреждением корпуса, либо вытеканием при наклоне. В аккумулятор доливают дистиллированную воду в тех случаях, когда произошло ее выкипание (испарение), т.к. выкипает именно вода, а не серная кислота.
Как доливать дистиллированную воду
Для доливки воды требуется именно дистиллированная вода. Сырая вода из под крана, либо кипяченная не подходит, т.к. содержит в себе примеси, которые негативно сказываются на протекании химических процессов и даже способны ухудшить состояние батареи, т.к. примеси оседают на элементах батареи. Кипячение не удаляет из воды жесткие примеси, соли и металлы, кипячением можно только убить бактерии и микробов в воде.
Сырая вода из под крана, либо кипяченная не подходит, т.к. содержит в себе примеси, которые негативно сказываются на протекании химических процессов и даже способны ухудшить состояние батареи, т.к. примеси оседают на элементах батареи. Кипячение не удаляет из воды жесткие примеси, соли и металлы, кипячением можно только убить бактерии и микробов в воде.
Марка дистиллированной воды, которую будете заливать, значения не имеет. У батареи выкручиваются пробки и аккуратно доливается вода до уровня, который нанесен на моноблоке. Если моноблок не прозрачный, то доливают столько воды, чтобы скрыть электроды полностью, а запас воды сверху составлял не менее 1 см.
После процедуры доливки воды, батарею рекомендуется зарядить на зарядном устройстве. Полностью заряженная батарея будет иметь плотность 1,26-1,28. Если плотность значительно отличается, то что-то пошло не так и вам лучше обратиться к специалистам.
Как доливать воду в необслуживаемый аккумулятор без доступа к банкам
На практике без доступа в банки делают необслуживаемые аккумуляторы по кальциевой технологии, т. е. которые не требуют доливки жидкости на протяжении всего срока службы. Но случается, что при перезаряде выкипание все же происходит. Если доступа в аккумулятор нет, а долить жидкость нужно, то придется помучатся. Рекомендуется высверлить в крышке АКБ небольшие отверстия 2-4 мм. и в них шприцом аккуратно долить дистиллированную воду.
е. которые не требуют доливки жидкости на протяжении всего срока службы. Но случается, что при перезаряде выкипание все же происходит. Если доступа в аккумулятор нет, а долить жидкость нужно, то придется помучатся. Рекомендуется высверлить в крышке АКБ небольшие отверстия 2-4 мм. и в них шприцом аккуратно долить дистиллированную воду.
Что будет, если вместо воды долить электролит
Если в батарею требуется долить дистиллированную воду, а вы дольете электролит, то после зарядки батареи его плотность превысит 1,30 и содержание серной кислоты станет запредельным. Это приведет к ускоренной сульфатации пластин батареи и выходу его из строя. Аккумуляторы с повышенной плотностью существуют и используются на крайнем севере, чтобы в батареи не образовывался лед, но при этом сам аккумулятор в таком состоянии способен отработать не более 1 года.
Как доливать электролит в аккумулятор
Перед тем, как электролит в аккумулятор заливать, его требуется сначала приготовить. В батарею можно доливать только электролит плотностью 1,26-1,29. Корректирующий электролит плотностью 1,40 можно доливать лишь в том случае, когда залили дистиллированной воды больше, чем этого требовалось и плотность даже после зарядки не поднялась для рекомендованного значения. В продаже можно найти готовый электролит, который можно сразу доливать в банки батареи. Корректирующий электролит придется разбавлять дистиллированной водой. Здесь нужно быть предельно внимательный и соблюдать строгие правила техники безопасности. Есть один серьезный нюанс – электролит (серная кислота) тяжелее воды, поэтому воду доливают в электролит, а не наоборот. В противном случае процесс разбавления будет сопровождаться брызгами, которые могут попасть на оголенные участки кожи.
Корректирующий электролит плотностью 1,40 можно доливать лишь в том случае, когда залили дистиллированной воды больше, чем этого требовалось и плотность даже после зарядки не поднялась для рекомендованного значения. В продаже можно найти готовый электролит, который можно сразу доливать в банки батареи. Корректирующий электролит придется разбавлять дистиллированной водой. Здесь нужно быть предельно внимательный и соблюдать строгие правила техники безопасности. Есть один серьезный нюанс – электролит (серная кислота) тяжелее воды, поэтому воду доливают в электролит, а не наоборот. В противном случае процесс разбавления будет сопровождаться брызгами, которые могут попасть на оголенные участки кожи.
Замена электролита в аккумуляторе
Замена электролита в аккумуляторе – процедура не только бесполезная, но и наоборот вредная. Срок службы аккумулятора подходит к концу в основном из-за оплывания активной массы – она с пластин осыпается на дно аккумулятора в виде шлама. От этого электролит темнеет, а аккумулятор теряет емкость. Темные электролит – это следствие оплывания активной массы, а не причина выхода его из строя. Смена электролита не вернет аккумулятору емкость, но при этом способна убить батарею.
Темные электролит – это следствие оплывания активной массы, а не причина выхода его из строя. Смена электролита не вернет аккумулятору емкость, но при этом способна убить батарею.
Дело в том, что шлам скапливается на дне моноблока, а при опрокидывании его для сливания электролита шлам перемещается на внутреннюю часть крышки батареи и в следствии попадает на оголенные элементы электродов, которые сверху не защищены сепараторами-изоляторами. В итоге происходит замыкание в одной или нескольких банках аккумулятора.
Электролит представляет собой жидкость состоящую из серной кислоты и дистиллированной воды. В некоторых ситуациях уровень электролита в аккумуляторе падает и требуется его нормализовать.
Емкость автомобильного аккумулятора – это способность батареи хранить определенное количество энергии. За емкость аккумулятора отвечает количество активной массы на электродах аккумуляторной батареи. Емкость аккумулятора определяется количество активной м
Напряжение аккумулятора – это физическая величина электрической цепи, которая определяется потенциалов между положительным выводом и отрицательным. Напряжение в теории физики тесно связано с ЭДС и многие автомобилисты путают их, поэтому для начала нужно
Напряжение в теории физики тесно связано с ЭДС и многие автомобилисты путают их, поэтому для начала нужно
Сегодня современный автомобиль – это не просто кусок металла с колесами. Современные автомобили буквально напичканы электроникой, о которой еще 10 лет назад могли только мечтать инженеры.
БУ-307: Как работает электролит?
Электролит служит катализатором, делающим батарею проводящей, способствуя движению ионов от катода к аноду при зарядке и обратно при разрядке. Ионы – это электрически заряженные атомы, которые потеряли или приобрели электроны. Электролит батареи состоит из растворимых солей, кислот или других оснований в жидком, гелеобразном и сухом виде. Электролит также поставляется в виде полимера, используемого в твердотельной батарее, твердой керамики и расплавленных солей, как в натрий-серной батарее.
Свинцово-кислотный использует серную кислоту . При зарядке кислота становится более плотной, так как на положительной пластине образуется оксид свинца (PbO 2 ), который при полной разрядке превращается почти в воду. Удельный вес серной кислоты измеряют ареометром. (См. также BU-903: Как измерить уровень заряда). Свинцово-кислотные батареи выпускаются в залитых и герметичных форматах, также известных как свинцово-кислотные с регулируемым клапаном (VRLA) или необслуживаемые.
Удельный вес серной кислоты измеряют ареометром. (См. также BU-903: Как измерить уровень заряда). Свинцово-кислотные батареи выпускаются в залитых и герметичных форматах, также известных как свинцово-кислотные с регулируемым клапаном (VRLA) или необслуживаемые.
Серная кислота бесцветна с легким желто-зеленым оттенком, растворима в воде и обладает высокой коррозионной активностью. Изменение цвета на коричневатый оттенок может быть вызвано ржавлением в результате анодной коррозии или попаданием воды в аккумуляторную батарею.
Свинцово-кислотные аккумуляторы имеют разный удельный вес (SG). В батареях глубокого цикла используется плотный электролит с SG до 1,330 для достижения высокой удельной энергии, стартерные батареи имеют средний SG около 1,265, а стационарные батареи имеют низкий SG около 1,225 для сдерживания коррозии и увеличения срока службы. (см. БУ-903: Как измерить уровень заряда).
Серная кислота имеет широкий спектр применений, а также входит в состав очистителей канализации и различных чистящих средств. Он также используется в переработке полезных ископаемых, производстве удобрений, переработке нефти, очистке сточных вод и химическом синтезе.
Он также используется в переработке полезных ископаемых, производстве удобрений, переработке нефти, очистке сточных вод и химическом синтезе.
| ОСТОРОЖНО | Серная кислота может вызвать серьезные повреждения при попадании на кожу и привести к необратимой слепоте при попадании в глаза. Проглатывание серной кислоты вызывает необратимые повреждения. |
Электролит в NiCd представляет собой щелочной электролит (гидроксид калия) . Большинство никель-кадмиевых аккумуляторов имеют цилиндрическую форму, в которой несколько слоев положительных и отрицательных материалов свернуты в рулон. Залитая версия NiCd используется в качестве корабельной батареи в коммерческих самолетах и в системах ИБП, работающих в жарком и холодном климате, требующих частых циклов. NiCd дороже свинцово-кислотных, но служит дольше.
NiMH использует тот же или аналогичный электролит, что и NiCd, который обычно представляет собой гидроксид калия. Электроды NiMH уникальны и состоят из никеля, кобальта, марганца, алюминия и редкоземельных металлов, которые также используются в литий-ионных батареях. NiMH доступен только в герметичных версиях.
Гидроксид калия представляет собой неорганическое соединение с формулой KOH, обычно называемое едким калием. Электролит бесцветен и имеет множество промышленных применений, например, ингредиент большинства мягких и жидких мыл. КОН вреден, если его не переварить.
Литий-ионный (Li-ion) Литий-ионный использует жидкий, гелевый или сухой полимерный электролит. Жидкая версия представляет собой легковоспламеняющийся органический, а не водный тип, раствор солей лития с органическими растворителями, подобными этиленкарбонату. Смешивание растворов с различными карбонатами обеспечивает более высокую проводимость и расширяет диапазон температур. Другие соли могут быть добавлены для уменьшения газообразования и улучшения цикличности при высоких температурах.
Другие соли могут быть добавлены для уменьшения газообразования и улучшения цикличности при высоких температурах.
Литий-ионные аккумуляторы с гелеобразными электролитами получают множество добавок для повышения проводимости, то же самое относится и к литий-полимерным аккумуляторам. Настоящий сухой полимер становится проводящим только при повышенных температурах, и эта батарея больше не используется в коммерческих целях. Добавки также вводятся для достижения долговечности и уникальных характеристик. Рецепт засекречен и у каждого производителя есть свой секрет соуса. (См. также BU-808b: Из-за чего умирает литий-ионный аккумулятор?)
Электролит должен быть стабильным, но это не относится к Li-ion. На аноде образуется пассивирующая пленка, называемая интерфейс твердого электролита (SEI) . Этот слой отделяет анод от катода, но позволяет ионам проходить через него подобно сепаратору. По сути, слой SEI должен сформироваться, чтобы батарея могла работать. Пленка стабилизирует систему и продлевает срок службы литий-ионных аккумуляторов, но снижает емкость. На катоде также происходит окисление электролита, что необратимо снижает емкость. (См. также BU-701: Как заправить батареи)
На катоде также происходит окисление электролита, что необратимо снижает емкость. (См. также BU-701: Как заправить батареи)
Чтобы пленки не становились слишком ограничительными, добавки смешивают с электролитом, который расходуется при формировании слоя SEI. Трудно, если вообще возможно, отследить их присутствие при проведении судебно-медицинской экспертизы. Это держит запатентованные добавки в коммерческой тайне, как их состав, так и используемое количество.
Хорошо известной добавкой является виниленкарбонат (VC). Это химическое вещество увеличивает срок службы литий-ионных аккумуляторов, особенно при более высоких температурах, и поддерживает низкое внутреннее сопротивление по мере использования и старения. VC также поддерживает стабильную пленку SEI на аноде без неблагоприятных побочных эффектов окисления электролита на катоде (Aurbach et al.). Говорят, что академические и исследовательские сообщества отстают от производителей клеток в знаниях и выборе добавок, отсюда и большой секрет. (См. также «Добавки и их влияние на кулоновскую эффективность» в разделе BU-808b: Что заставляет Li-ion умирать?
(См. также «Добавки и их влияние на кулоновскую эффективность» в разделе BU-808b: Что заставляет Li-ion умирать?
Для большинства коммерческих литий-ионных аккумуляторов слой SEI разрушается при температуре элемента 75–90°C (167–194°F). Тип элемента и уровень заряда (SoC) влияют на пробой при повышенной температуре. Может возникнуть самонагрев, который может привести к тепловому разгону при неправильном охлаждении. Лабораторные тесты, проведенные на ячейках 18650, показали, что такое тепловое событие может развиваться в течение двух дней.
Еще одной проблемой является воспламеняемость литий-ионного электролита, и проводятся эксперименты по получению негорючих или пониженно воспламеняющихся электролитов с помощью добавок или разработки неорганических ионных жидкостей. Также проводятся исследования по эксплуатации Li-ion при низких температурах. На момент написания ни один из этих электролитов не имел широкого коммерческого применения.
Высыхание или медленное превращение жидкого электролита в твердую форму — еще одно явление старения, снижающее производительность Li-ion. «Когда жидкость ушла, батареи разряжены», — говорит Джефф Дан, специалист по литий-ионным батареям и профессор физики. Жидкость электролита — еще один индикатор состояния, относящийся ко всем химическим веществам батареи.
«Когда жидкость ушла, батареи разряжены», — говорит Джефф Дан, специалист по литий-ионным батареям и профессор физики. Жидкость электролита — еще один индикатор состояния, относящийся ко всем химическим веществам батареи.
Аккумуляторы в портативном мире
Материал Университета аккумуляторов основан на незаменимом новом 4-м издании » Аккумуляторы в портативном мире. Справочник по перезаряжаемым батареям для не инженеров », который можно заказать на Amazon.com.
Добавление воды в аккумулятор: все, что вам нужно знать
ваше полное руководство по добавлению воды в аккумулятор
Полив аккумуляторов является основной частью нашей деятельности в Foxtron
Поэтому мы хотели передать вам наши экспертные знания
Из этой статьи вы узнаете:
- Зачем свинцово-кислотным аккумуляторам нужна вода
- Когда добавлять воду в аккумулятор
- Советы по безопасности при поливе аккумуляторов
- Как долить воду в аккумулятор, шаг за шагом
- И многое другое!
Начинаем!
Содержание
- Зачем свинцово-кислотным батареям нужна вода?
- Советы по безопасности при поливе аккумуляторов
- Когда следует добавлять воду?
- Какой тип воды следует использовать?
- Как добавить воду в свинцово-кислотный аккумулятор вилочного погрузчика: пошаговая инструкция
Зачем свинцово-кислотным аккумуляторам нужна вода?
Чтобы ответить на этот вопрос, нам сначала нужно понять, как работают свинцово-кислотные батареи.
Свинцово-кислотные аккумуляторы вырабатывают электричество в результате электрохимической реакции между свинцовыми пластинами и электролитами.
Электролиты представляют собой смесь воды и серной кислоты.
Залитые аккумуляторы производят электричество в результате реакции жидкого электролита и свинцовых пластин
И вода защищает активный материал батареи, пока она вырабатывает энергию.
Без воды активный материал окислится, и батарея потеряет мощность.
Вот почему для свинцово-кислотных аккумуляторов нужна вода.
Почему свинцово-кислотные батареи теряют воду?
Когда аккумулятор заряжается, электричество проходит через электролит.
При этом вода в электролите расщепляется на исходные элементы — водород и кислород.
Батареи теряют воду, потому что во время зарядки электричество расщепляет воду на водород и кислород. Затем выделяется некоторое количество водорода
Этот процесс называется выделением газа.
И именно из-за этого процесса выделения газа теряется вода из батареи.
Но в зависимости от того, какая кислота в аккумуляторе, поливать его может и не нужно.
Например, малообслуживаемые аккумуляторы, такие как гелевые и AGM-аккумуляторы, не нуждаются в регулярном доливе воды.
Это потому, что эти батареи запечатаны.
Герметичные батареи предотвращают потерю воды, предотвращая утечку водорода.
Герметичность позволяет атомам реформироваться, предотвращая потерю воды.
С другой стороны, вентилируемые батареи позволяют газам выходить, что приводит к потере воды.
Вентиляционные отверстия, показанные здесь на затопленной батарее, позволяют водороду выходить, что приводит к потере воды
Таким образом, вентилируемые батареи необходимо регулярно проверять на предмет утечки воды и при необходимости доливать.
Зачем вам нужно поддерживать уровень воды в аккумуляторе вилочного погрузчика?
Если уровень воды упадет слишком низко, свинцовые пластины аккумулятора могут окислиться.
И это может привести к таким симптомам низкого заряда батареи, как:
- Снижение заряда батареи
- Не заряжается полностью
- Уменьшенный срок службы батареи
Если не устранить, повреждение может стать необратимым, что сделает батарею бесполезной.
Советы по безопасности при поливе аккумуляторов
Добавление воды в свинцово-кислотный аккумулятор может быть рискованным.
Химические вещества, содержащиеся в батарее, могут привести как к травме, так и к повреждению.
Эти химические вещества представляют различные опасности, такие как:
Разбрызгивание кислоты
Коррозия
Ожоги кожи
Вдыхание токсичных газов, таких как водород
Поэтому при поливе аккумуляторов необходимо следовать определенным советам.
Носите надлежащие средства индивидуальной защиты
Прежде чем приступить к работе с аккумулятором, вам необходимо получить соответствующие средства индивидуальной защиты (СИЗ).
OSHA требует носить соответствующие СИЗ при работе с батареями
OSHA требует, чтобы те, кто работает с батареями, носили:
- Защитную маску
- Фартук
- Резиновые перчатки
Средства индивидуальной защиты уменьшат потенциальный контакт кожи с электролитом и защитят вас от опасностей, связанных с батареями вилочных погрузчиков.
Вода только в специально отведенных местах
Убедитесь, что вы поливаете батареи только в соответствующей зоне, состоящей из:
- Устойчивая и ровная поверхность
- Адекватная вентиляция
- Отсутствие предметов, создающих искру или пламя
Хотя электролит не воспламеняется, возможно возникновение искр или пламени.
Это связано с возможным остаточным газообразным водородом внутри элемента аккумулятора после процесса зарядки.
Из-за риска для свинцово-кислотных аккумуляторов для вилочных погрузчиков требуется отдельная площадка для зарядки.
Кроме того, если в зоне полива находятся посторонние, сообщите им о процессе полива (и ситуации).
Так они тоже будут осторожны.
Когда следует добавлять воду?
Время добавления воды в аккумулятор вилочного погрузчика заранее не установлено.
Но, как правило, воду следует добавлять через каждые пять-десять циклов зарядки, когда уровень электролита в аккумуляторе низкий.
Когда добавлять воду зависит от:
- Частоты зарядки аккумулятора
- Сколько воды может вместить ячейка
- Возраст и состояние аккумулятора
Таким образом, часто лучший способ определить наилучший график полива — это просто опыт.
Как проверить уровень воды в аккумуляторе
Уровень жидкости в аккумуляторе можно проверить вручную или с помощью индикатора уровня жидкости в аккумуляторе.
Вот как вручную проверить уровень воды в аккумуляторе:
Снимите крышку ячейки или вентиляционную крышку с каждой ячейки батареи
Проверьте, не покрывает ли электролит верхнюю часть защитного брызговика.
 Если да, то ему не нужна вода
Если да, то ему не нужна водаЕсли уровень электролита ниже брызговика и некоторые пластины оголены, аккумулятор нуждается в поливе
Уровень воды должен быть немного выше пластины (выделена оранжевым цветом)
Использование индикатора уровня воды на батарейках — самый простой способ проверить уровень воды.
Просто проверьте, мигает ли красный индикатор.
Зеленый индикатор на этом изображении указывает на то, что в аккумуляторе погрузчика достаточно воды
Если да, то вам нужно добавить воды.
Если он мигает зеленым, в аккумуляторе достаточно воды.
Нужно ли добавлять воду в аккумулятор до или после зарядки?
Добавляйте воду только после зарядки (после полной зарядки), чтобы учесть расширение.
Кроме того, доливать воду следует только после того, как аккумулятор остынет.
Это когда уровень воды в аккумуляторе достигает максимального значения после расширения.
И важно предусмотреть возможность расширения, так как это может помочь предотвратить кипение.
Сколько воды нужно добавить в аккумулятор?
Добавляйте воду до тех пор, пока уровень электролита не будет на 1/8 дюйма выше пластин или примерно на ¾ дюйма ниже верхней части элемента.
Что делать, если вы добавили слишком много воды в аккумулятор
Очень важно не перезаряжать аккумуляторы.
При добавлении воды в свинцово-кислотный аккумулятор необходимо оставить достаточно места для расширения жидкостей (воды и серной кислоты) во время зарядки или использования аккумулятора.
В противном случае аккумуляторы могут вздуться, переполниться и пролить раствор электролита.
И это может привести к травмам или повреждениям, если раствор попадет на кожу и другие предметы.
Последствия выкипания свинцово-кислотного аккумулятора на бетон
Кроме того, добавление слишком большого количества воды может привести к разбавлению электролита.
И это может снизить мощность батареи, что приведет к снижению производительности.
При переполнении аккумулятора может потребоваться слить часть электролита.
Поскольку это может быть опасно, мы рекомендуем обратиться за помощью к специалисту по аккумуляторам.
Какой тип воды следует использовать?
Для заправки свинцово-кислотных аккумуляторов следует использовать только чистую дистиллированную или деионизированную воду.
Кроме того, он должен находиться в пределах от 5 до 7 по шкале pH и в пределах рекомендуемого уровня загрязнения батареи.
Зачем использовать дистиллированную воду в батареях?
В аккумулятор рекомендуется добавлять дистиллированную воду.
Это потому, что дистиллированная вода очищается и не содержит дополнительных минералов, которые можно найти в водопроводной воде.
Добавляйте в аккумулятор только дистиллированную воду, а не водопроводную воду.
Не рекомендуется использовать водопроводную воду, поскольку она может нарушить химический баланс.
Как?
Водопроводная вода содержит минералы.
И эти минералы реагируют с химическими веществами батареи, превращая их в неперезаряжаемые ионы.
Эти ионы не могут принимать участие ни в каком электрическом накопителе.
Более того, водопроводная вода вступает в реакцию с электролитом, снижая производительность батареи и увеличивая осадок.
И это может повредить материалы батареи.
Где купить дистиллированную воду для аккумуляторов?
Чистая дистиллированная вода стоит немного дороже, потому что при дистилляции удаляются примеси.
Где вы берете дистиллированную воду, зависит от количества, которое вам нужно использовать.
Для более крупных операций с большим количеством аккумуляторов лучше покупать дистиллированную воду у промышленного поставщика.
Вы можете купить дистиллированную воду у промышленных поставщиков. Или вы можете сделать это сами
Однако, если вам нужно только немного дистиллированной воды и у вас ограниченный бюджет, вы можете сделать это самостоятельно.
Сделать это довольно просто и требует только устройства деминерализации или нескольких кастрюль и сковородок.
Не добавляйте кислоту в аккумулятор!
Добавление кислоты в аккумулятор ускоряет его износ.
Почему?
При нормальной работе аккумуляторы потребляют только воду, а не кислоту.
А если добавить кислоту, то нарушится электролитный баланс.
Еще одна причина не добавлять кислоту — это просто опасно.
Поэтому, если уровень электролита ниже необходимого, залейте в аккумулятор только воду.
Но если электролит пролит и вам нужно добавить кислоту, обратитесь за этой услугой к специалисту по аккумуляторам.
Как добавить воду в свинцово-кислотный аккумулятор вилочного погрузчика: шаг за шагом
Добавление воды в элементы свинцово-кислотного аккумулятора — это простой процесс, если выполнять его осторожно.
Всего есть два способа сделать это:
- Добавление воды вручную (напрямую) в отдельные элементы с помощью пистолета для заливки аккумуляторов или насадки
- Автоматическое добавление воды с помощью аккумуляторной системы полива
Добавление воды с помощью ручного пистолета для заполнения
Сначала необходимо приобрести аккумуляторный пистолет отдельно от аккумулятора вилочного погрузчика.
Вам понадобится ручной заправочный пистолет, который продается отдельно от аккумулятора
Затем, вот как заполнить аккумулятор водой непосредственно через поливочный пистолет или насадку:
Убедитесь, что аккумулятор полностью заряжен и остыл
Наденьте СИЗ
Откройте вентиляционные крышки каждой ячейки
Подсоедините пистолет для орошения аккумулятора к стандартному водяному шлангу или деионизатору воды
Правильно отрегулируйте водяной пистолет для конкретного аккумулятора
Налейте достаточное количество воды, чтобы покрыть верх тарелок. Вставьте наконечник пистолета в аккумуляторную ячейку, пока он не коснется защитной пластины
.Активируйте поток воды на вашем устройстве. Вы можете сделать это, сжав ручку **
Повторяйте процесс, пока все клетки не будут залиты водой. Продолжайте регулировать индикатор глубины до тех пор, пока каждый элемент батареи не будет поливать водой до одинакового уровня
.
После этого закройте и замените или затяните все крышки аккумуляторных батарей.
** Примечание: Конструкция этих устройств позволяет перекрывать поток воды при противодавлении. Это означает, что поток автоматически отключится, когда уровень воды достигнет наконечника пистолета или сопла. Это ваш индикатор для перехода к следующей ячейке.
Добавление воды с помощью системы полива батареи
Системы полива автоматизируют процесс полива, чтобы ускорить его и свести к минимуму опасности в процессе полива батареи.
Аккумуляторная система полива, установленная на аккумуляторе вилочного погрузчика, видна с черными шлангами
Существуют аккумуляторные системы полива различных марок, но все они работают одинаково.
Процесс полива батарей выглядит так:
Снимите пылезащитный колпачок с оборудованной системы полива
Прикрепите оборудованную систему полива к источнику воды.
 Или подсоедините входной шланг к разливочной машине
Или подсоедините входной шланг к разливочной машинеВключите разливочную машину и активируйте поток воды
Следите за индикатором потока в вашей системе полива. Он отключится, когда каждая ячейка будет заполнена соответствующим количеством воды
.Вы также можете дождаться остановки машины и отсоединить поливочный шланг
После этого закройте и замените или затяните все крышки аккумуляторных батарей **
Когда вы закончите полив, уберите любые разливы вокруг элементов батареи
** Примечание: Хотя системы полива рассчитаны на то, чтобы достигать и наполнять каждую ячейку, мы рекомендуем после этого дважды проверять каждую ячейку. Это поможет убедиться, что все ячейки находятся на адекватном и равном уровне над пластинами.
Вывод
Вот и все: полное руководство по добавлению воды в аккумулятор.
Теперь мы хотели бы услышать от вас.
Что вы узнали о разрядке аккумулятора из этой статьи?
У вас есть дополнительные вопросы?
Пожалуйста, сообщите нам об этом в разделе комментариев!
Аккумуляторный электролит — что это такое и как это работает?
Будь то игрушки для детей, беспроводные электроинструменты или электромобили, аккумуляторы становятся стандартной частью нашей повседневной жизни. Ключевым компонентом батареи является внутренний электролит батареи.
Сегодня мы изучаем, что такое электролит для батареи Lifepo4 12 В 42 Ач и как он может продлить срок службы вашей батареи Lifepo4 12 В 42 Ач. Давайте погрузимся!
Что такое аккумуляторный электролит? Электролит батареи представляет собой раствор внутри батареи. На самом деле, это зависит от типа батареи, так как это может быть жидкость или пастообразная субстанция. Однако роль электролита одинакова независимо от типа аккумулятора: он переносит положительно заряженные ионы между катодом и анодом.
Аккумуляторы состоят из трех основных компонентов: отрицательного электрода, анода и электролита, разделяющего два терминала. Электролит — это химическое вещество, которое позволяет электрическому заряду проходить между двумя клеммами. Электролит приводит химические вещества, необходимые для реакции, в контакт с анодом и катодом, тем самым преобразуя накопленную энергию в пригодную для использования электрическую энергию. Этот ответ приводит в действие подключенное устройство, будь то свет, пылесос или электромобиль.
Из чего состоит электролит батареи? На самом деле, разные типы батарей зависят от разных типов электролитов и их химических реакций. Например, в свинцово-кислотных батареях для получения желаемой реакции часто используется серная кислота. Воздушно-цинковые батареи основаны на реакции оксида цинка с кислородом. Гидроксид калия является электролитом в обычных бытовых щелочных батареях. Наиболее часто используемый электролит в литиевых батареях – это гексафторфосфат лития (LiPF6) и другие растворы солей лития.
Наиболее часто используемый электролит в литиевых батареях – это гексафторфосфат лития (LiPF6) и другие растворы солей лития.
Если вы вспомните уроки химии в старшей школе, возможно, вы помните, что при работе с химическими веществами нужно надевать защитные очки и другое защитное снаряжение. Химические вещества, используемые для проведения химических реакций в батареях, обычно опасны, поэтому при обращении с батареями и их электролитами соблюдайте соответствующие меры предосторожности.
Можно ли добавить электролит в батарею?Да, вы можете доливать электролит в аккумулятор, но только если это негерметичный мокрый аккумулятор. Проверка заряда мокрой батареи — это стандартное техническое обслуживание, которое следует выполнять на регулярной основе.
Хотя электролит содержит воду и серную кислоту, в литий-полимерный аккумулятор нельзя добавлять ничего, кроме дистиллированной воды. При нормальной работе влажная литий-полимерная батарея потребляет только воду.
Если ваша литий-полимерная батарея герметична или не потребляет электролит при разрядке, вы не можете добавить электролит. Вам это тоже не нужно. Отсутствие выхлопных газов является одним из больших преимуществ выбора литий-ионных аккумуляторов или AGM, поскольку они требуют минимального обслуживания во время использования.
Это влажные аккумуляторы. Когда эти батареи необходимы для добавления новой кислоты, новой кислоты и когда они используются, они требуют регулярного добавления воды.
Какие компоненты литиевых батарей?Состав электролита литиевой батареи зависит от типа литиевой батареи и ее химического состава реакции. В большинстве литиевых аккумуляторов используются жидкие электролиты в органических растворителях, таких как LiPF6, LiBF4 или LiClO4.
Но последние разработки позволили создать твердые керамические электролиты, такие как оксиды лития и металлического лития, и вариант для батарей. Самым большим преимуществом твердых электролитов является устранение риска утечки и воспламеняемости аккумуляторов с жидким электролитом, что является риском для безопасности аккумуляторов с жидким электролитом.
Гексафторфосфат лития (LiPF6) является наиболее часто используемой литиевой солью в литий-ионных батареях. Это решение создает невероятно стабильную среду для Li-ion во время зарядки и разрядки аккумулятора.
Как работают литиевые батареи?В литий-ионных батареях используются заряженные ионы лития для создания потенциала между положительным и отрицательным электродами. Тонкий слой изолятора, который мы назвали сепаратором, расположен в растворе электролита между сторонами батареи. Сепаратор позволяет ионам лития проходить, блокируя электроны, что удерживает два электрода разделенными. В процессе зарядки ионы лития перемещаются от положительного электрода к отрицательному через сепаратор. При разряде ионы движутся в противоположном направлении.
Движение ионов лития создает разность потенциалов, называемую «напряжением». Когда вы подключаете электронное устройство к аккумулятору, электроны (не ионно-литиевые) проходят через устройство и питают его.
Честно говоря, можно смело сказать, что электролит в литиевых батареях безопасен. Однако в первые годы существования литиевых батарей литиевые батареи иногда загорались, что также известно как тепловой разгон. Однако пожары в основном вызываются перегревом, проколом или перезарядкой растворителя в литиевой батарее.
Как наиболее легковоспламеняющийся компонент литий-ионных аккумуляторов, электролит всегда считался тесно связанным с его безопасностью. Всем производителям аккумуляторов необходимо оптимизировать электролит, поскольку это лучший способ повысить безопасность литий-ионных аккумуляторов.
По мере развития технологий появляются новые возможности, которые можно использовать для повышения безопасности литиевых батарей. Например, запатентованная Maxworld Power система управления батареями (BMS) отключает батарею при обнаружении небезопасного состояния. Можно сказать, что это один из самых безопасных аккумуляторов на рынке.
В целом аккумуляторный электролит является наиболее важным компонентом всех типов аккумуляторов, и в большинстве случаев вы можете никогда его не учитывать. Однако это зависит от типа батареи, которую вы используете. Знание того, как работает электролит в батарее, может значительно продлить срок ее службы.
К счастью, когда вы инвестируете в такие продукты, как аккумуляторы Maxworld Power, требуется гораздо меньше работ по техническому обслуживанию, и вы можете полностью игнорировать аккумуляторный электролит.
Поделиться сейчас
Похожие сообщения
Новый аккумуляторный электролит может расширить модельный ряд электромобилей
Автор Марк Шварц
Новый электролит на основе лития, изобретенный учеными Стэнфордского университета, может проложить путь к следующему поколению электромобилей с батарейным питанием.
В исследовании, опубликованном 22 июня в журнале Nature Energy , исследователи из Стэнфорда демонстрируют, как их новая конструкция электролита повышает производительность литий-металлических батарей, многообещающей технологии для питания электромобилей, ноутбуков и других устройств.
Обычный (прозрачный) электролит слева и новый Стэнфордский электролит
справа. (Изображение предоставлено Чжао Ю)
«Большинство электромобилей работают на литий-ионных батареях, которые быстро приближаются к своему теоретическому пределу плотности энергии», — сказал соавтор исследования И Цуй, профессор материаловедения и инженерии, а также фотонной науки. в Национальной ускорительной лаборатории SLAC. «Наше исследование было сосредоточено на литий-металлических батареях, которые легче литий-ионных батарей и потенциально могут обеспечивать больше энергии на единицу веса и объема».
Литий-ионный против металлического лития
Литий-ионные аккумуляторы, используемые во всем, от смартфонов до электромобилей, имеют два электрода — положительно заряженный катод, содержащий литий, и отрицательно заряженный анод, обычно сделанный из графита. Раствор электролита позволяет ионам лития перемещаться туда и обратно между анодом и катодом, когда батарея используется и когда она перезаряжается.
Литий-металлическая батарея может удерживать в два раза больше электроэнергии на килограмм, чем современная обычная литий-ионная батарея. Литий-металлические батареи делают это, заменяя графитовый анод металлическим литием, который может хранить значительно больше энергии.
«Литий-металлические батареи очень перспективны для электромобилей, где вес и объем имеют большое значение», — сказал соавтор исследования Чжэнан Бао, K.K. Ли Профессор инженерной школы. «Но во время работы литий-металлический анод реагирует с жидким электролитом. Это вызывает рост литиевых микроструктур, называемых дендритами, на поверхности анода, что может привести к возгоранию и выходу батареи из строя».
Исследователи десятилетиями пытались решить проблему дендритов.
«Электролит был ахиллесовой пятой литий-металлических аккумуляторов», — сказал соавтор Чжао Юй, аспирант по химии. «В нашем исследовании мы используем органическую химию для рационального проектирования и создания новых стабильных электролитов для этих батарей».
Новый электролит
В ходе исследования Ю и его коллеги изучили, могут ли они решить проблемы стабильности с помощью обычного имеющегося в продаже жидкого электролита.
«Мы предположили, что добавление атомов фтора в молекулу электролита сделает жидкость более стабильной, — сказал Юй. «Фтор — широко используемый элемент в электролитах для литиевых аккумуляторов. Мы использовали его способность притягивать электроны для создания новой молекулы, которая позволяет металлическому литиевому аноду хорошо функционировать в электролите».
Результатом стало новое синтетическое соединение, сокращенно FDMB, которое можно легко производить в больших количествах.
«Конструкции электролитов становятся очень экзотичными, — сказал Бао. «Некоторые из них подали хорошие надежды, но их производство очень дорого. Молекулу FDMB, которую придумал Чжао, легко производить в больших количествах, и она довольно дешевая».
«Невероятная производительность»
Стэнфордская команда протестировала новый электролит в литий-металлическом аккумуляторе.
Результаты были потрясающими. Опытная батарея сохранила 90 процентов от первоначального заряда после 420 циклов зарядки и разрядки. В лабораториях типичные литий-металлические батареи перестают работать примерно через 30 циклов.
Кандидаты в доктора наук и ведущие авторы Хансен Ван (слева) и Чжао Ю (справа) тестируют
экспериментальную клетку в своей лаборатории. (Изображение предоставлено Hongxia Wang.)
Исследователи также измерили, насколько эффективно ионы лития переносятся между анодом и катодом во время зарядки и разрядки, свойство, известное как «кулоновская эффективность».
«Если вы зарядите 1000 ионов лития, сколько вы получите обратно после разрядки?» — сказал Цуй. «В идеале вам нужно 1000 из 1000 для кулоновской эффективности 100 процентов. Чтобы быть коммерчески жизнеспособным, элемент батареи должен иметь кулоновский КПД не менее 99,9%. В нашем исследовании мы получили 99,52% в полуячейках и 99,98% в полных ячейках; невероятное выступление».
Аккумулятор без анода
Для потенциального использования в бытовой электронике команда из Стэнфорда также протестировала электролит FDMB в безанодных литий-металлических мешочных элементах — имеющихся в продаже батареях с катодами, которые подают литий к аноду.
«Идея состоит в том, чтобы использовать литий только на стороне катода для снижения веса», — сказал соавтор Хансен Ван, аспирант в области материаловедения и инженерии. «Безанодная батарея проработала 100 циклов, прежде чем ее емкость упала до 80 процентов — не так хорошо, как эквивалентная литий-ионная батарея, которая может работать от 500 до 1000 циклов, но все же одна из самых эффективных безанодных элементов».
«Эти результаты обнадеживают для широкого спектра устройств», — добавил Бао. «Легкие безанодные аккумуляторы станут привлекательной чертой для дронов и многих других потребительских электронных устройств».
Battery500
Министерство энергетики США (DOE) финансирует большой исследовательский консорциум под названием Battery500, чтобы сделать литий-металлические батареи жизнеспособными, что позволит производителям автомобилей создавать более легкие электромобили, которые могут преодолевать гораздо большие расстояния между зарядками. Это исследование было частично поддержано грантом консорциума, в который входят Стэнфорд и SLAC.
Это исследование было частично поддержано грантом консорциума, в который входят Стэнфорд и SLAC.
Улучшая аноды, электролиты и другие компоненты, Battery500 стремится почти втрое увеличить количество электроэнергии, которую может обеспечить литий-металлическая батарея, со 180 ватт-часов на килограмм, когда программа была запущена в 2016 году, до 500 ватт-часов на килограмм. Более высокое отношение энергии к весу, или «удельная энергия», является ключом к решению проблем с запасом хода, которые часто возникают у потенциальных покупателей электромобилей.
«Безанодная батарея в нашей лаборатории достигла удельной энергии около 325 ватт-часов на килограмм, приличное число», — сказал Цуй. «Нашим следующим шагом может быть совместная работа с другими исследователями из Battery500 для создания элементов, которые приближаются к цели консорциума в 500 ватт-часов на килограмм».
В дополнение к более длительному сроку службы и лучшей стабильности, электролит FDMB также гораздо менее воспламеняем, чем обычные электролиты, как показали исследователи во встроенном видео.
«Наше исследование, по сути, представляет собой принцип проектирования, который люди могут применять для создания лучших электролитов», — добавил Бао. «Мы только что показали один пример, но есть много других возможностей».
Другие соавторы из Стэнфорда: Цзянь Цинь , доцент кафедры химического машиностроения; ученые с докторской степенью Сянь Конг, Кеченг Ван, Вэньсяо Хуан, Снехашис Чоудхури и Чибуезе Аманчукву; аспиранты Уильям Хуан, Ючи Цао, Дэвид Макканик, Ю Чжэн и Саманта Хунг; и студенты Ютинг Ма и Эдер Ломели. Синьчан Ван из Сямэньского университета также является соавтором. Чжэнань Бао и И Цуй — старшие научные сотрудники Стэнфордского университета 9.0011 Предварительный суд Института энергетики . Цуй также является главным исследователем Стэнфордского института материаловедения и энергетики , совместной исследовательской программы SLAC/Стэнфорда.
Эта работа также поддерживалась Программой исследований аккумуляторных материалов Управления автомобильных технологий Министерства энергетики США. Двое соавторов поддерживаются Программой стипендий для аспирантов Национального научного фонда и Постдокторской стипендией Центра TomKat в области устойчивой энергетики в Стэнфорде. Оборудование, используемое в Стэнфорде, поддерживается Национальным научным фондом.
Двое соавторов поддерживаются Программой стипендий для аспирантов Национального научного фонда и Постдокторской стипендией Центра TomKat в области устойчивой энергетики в Стэнфорде. Оборудование, используемое в Стэнфорде, поддерживается Национальным научным фондом.
Машины для наполнения электролитом литий-ионных аккумуляторов
Какие материалы используются в батареях?
Для литий-ионных аккумуляторов в первую очередь используется ресурс лития. Другие — кобальт, никель, манган и графит.
Какова функция электролита в элементе литий-ионного аккумулятора?
Электролиты — это вещества (в основном жидкости) внутри аккумуляторной батареи, которые обладают проводимостью благодаря ионным молекулам. Таким образом, электролит обеспечивает поток энергии между электродами. Часто добавляют добавки, такие как проводящая соль или добавки для лучшего смачивания и качества батареи. Заливка электролитом является важной частью сборки аккумуляторной батареи. Машины, предоставляемые IP PowerSystems, способны заполнять все типы аккумуляторных элементов жидким электролитом.
Заливка электролитом является важной частью сборки аккумуляторной батареи. Машины, предоставляемые IP PowerSystems, способны заполнять все типы аккумуляторных элементов жидким электролитом.
Как добавить электролит в элемент литий-ионного аккумулятора?
Заливка электролита происходит в сухом помещении, в перчаточном боксе или с герметически закрытой ячейкой. Электролит заливают в аккумуляторную ячейку дозирующей иглой или форсунками. Мы предлагаем инновационные процессы для быстрого и однородного смачивания без образования пены или загрязнения электролитом. Наши машины могут работать полностью автоматически, имеют вакуумную камеру с коротким временем вакуумирования, функцию обратной откачки и промывки, а также пульсацию и предварительный нагрев электролита. Чтобы сократить расходы на большие сухие помещения, мы изобрели инновацию в области интеллектуальных аккумуляторов: технологию портов для наполнения, формования и дегазации литий-ионных ячеек.
Как работает машина для розлива электролита?
Машины для заливки электролита используются для заливки электролита в элемент литий-ионного аккумулятора. Ассортимент продукции простирается от крупных производственных предприятий до небольшого научно-исследовательского и лабораторного оборудования. Наши машины относятся ко второму типу, поскольку они обеспечивают заправочные модули для прототипирования и небольшие серии для собственных исследовательских линий. Заполнение либ электролитом на нашем оборудовании очень точное, прослеживаемое и документируемое.
Как вы производите ионно-литиевые аккумуляторы?
Производство литий-ионных аккумуляторов требует множества различных рабочих операций и ресурсов.
Сначала изготавливаются электроды: различные материалы смешиваются в пасту (суспензию) для анода и катода. Эта смесь наносится на металлическую фольгу, примеряется и затем сжимается, разрезается и разрезается по размеру.
После этого происходит сборка аккумуляторных элементов: анод, сепаратор и катод укладываются друг за другом по очереди в стопку или обертку. Далее фиксируются выступы и стопка ячеек помещается в корпус. Теперь ячейки заполнены электролитом.
Готовые аккумуляторные элементы можно объединять в модули или аккумуляторные блоки, которые используются в качестве мощных литий-ионных аккумуляторов для электромобилей.
Что такое карманная батарея?
Аккумуляторная батарея в сумке не имеет жесткой конструкции, а имеет ламинированную алюминиевую или пластиковую внешнюю оболочку. Таким образом, он может быть изготовлен в различных формах или размерах (часто призматических) и является более экономичным и энергоэффективным при меньшем весе. Однако производство литий-ионных аккумуляторных батарей является более сложной задачей. Вот почему мы изобрели инновацию в области интеллектуальных аккумуляторов — новую технологию портов для заполнения электролитом аккумуляторных батарей без сухого помещения и менее опасных отходов.
Как работают литий-ионные аккумуляторы?
Когда мы используем литий-ионные батареи или аккумуляторы, происходит следующее: отрицательные электроны высвобождаются на аноде и переносятся на катод. Во время этого процесса химическая энергия преобразуется в электронную энергию, которую мы можем использовать для наших устройств. Во время зарядки электроны снова переносятся на анод, а литий проходит через сепаратор к аноду с графитовым слоем. Аккумулятор снова заряжается.
Где мы используем литий-ионные аккумуляторы, также известные как lib?
Литий-ионные аккумуляторы присутствуют в нашей повседневной жизни. Меньшие можно найти в смартфонах, небольших электронных устройствах и инструментах, большие — в электронных велосипедах или электромобилях, в более крупных электронных или садовых инструментах.
Почему мы используем литий-ионные аккумуляторы?
Литий-ионные аккумуляторы имеют много преимуществ по сравнению с обычными аккумуляторными элементами: они перезаряжаемы, имеют длительный срок службы и высокую скорость разряда. Кроме того, литий-ионные батареи обеспечивают большую плотность энергии и проводимость, несмотря на маленькие ячейки. Следовательно, мы можем использовать мобильные электронные устройства в течение длительного периода времени и просто перезаряжать их, если это необходимо.
Кроме того, литий-ионные батареи обеспечивают большую плотность энергии и проводимость, несмотря на маленькие ячейки. Следовательно, мы можем использовать мобильные электронные устройства в течение длительного периода времени и просто перезаряжать их, если это необходимо.
Батарейки | Бесплатный полнотекстовый | Концентрация добавки к электролиту для максимального накопления энергии в свинцово-кислотных батареях
1. Введение
Добавление химической добавки в электролит свинцово-кислотной батареи может изменить удельную энергию, которую батарея может хранить. Этот факт был известен с момента изобретения батареи и в настоящее время представляет большой интерес для аккумуляторной промышленности. В этой статье представлен общий метод оценки влияния добавок к электролиту на энергоемкость свинцово-кислотной батареи и определения наилучшей концентрации добавок для использования. Рассматриваемая здесь добавка к электролиту носит довольно общий характер. Это может быть химическое соединение или смесь химических веществ; суспензия или гель, используемые для иммобилизации электролита. Единственным ограничением является то, что добавка — что бы это ни было — должна находиться в химическом равновесии и иметь низкую реакционную способность по отношению к другим компонентам батареи.
Это может быть химическое соединение или смесь химических веществ; суспензия или гель, используемые для иммобилизации электролита. Единственным ограничением является то, что добавка — что бы это ни было — должна находиться в химическом равновесии и иметь низкую реакционную способность по отношению к другим компонентам батареи.
Добавки также добавляют в электролит батареи по целому ряду других причин, например, для продления срока службы батареи, уменьшения коррозии электродов, улучшения проводимости, уменьшения газовыделения на электродах, защиты от перезарядки или глубокой разрядки и т. д. полезное в одних отношениях может быть вредным в других. Таким образом, выбор и концентрация добавки всегда должны оцениваться с точки зрения побочных эффектов, которые она вызывает. Это означает, в частности, что добавка, повышающая энергоемкость батареи, может оказаться нежизнеспособной, по крайней мере, при определенных концентрациях, из-за других нежелательных эффектов, которые она вызывает.
Существуют сотни статей, книг и патентов, посвященных добавкам к электролиту и их влиянию на свинцово-кислотные аккумуляторы. Полный обзор литературы вышел бы за рамки настоящей статьи. Глава 3 книги Павлова [1] содержит сравнительно краткий обзор основной литературы по теме примерно до 2011 года. Речь идет о классических неорганических добавках (фосфорная кислота, борная кислота, лимонная кислота, сульфат стронция, сульфат натрия), углеродных суспензиях, и эмульсии органических полимеров. В настоящее время активно изучается большой потенциал ионных жидкостей в качестве добавок к электролитам [2] благодаря способности этих солей расширять электрохимическое окно воды [3,4,5]. Кроме того, большой практический интерес представляет изучение добавок, образующих гелеобразные электролиты, в связи с их применением в области электродвижения [6,7,8]. Интересное исследование добавления добавки в гелеобразный электролит недавно было представлено в [9].].
Разнообразие доступных добавок делает невозможным дать общие правила в отношении наилучшей добавки и наилучшей концентрации для использования в данной цели. Поэтому настоящая статья по необходимости должна быть несколько ограничена по объему. По этой причине, игнорируя другие эффекты, в данной статье основное внимание уделяется влиянию добавок на энергоемкость аккумулятора. Представленный анализ обеспечивает общий способ оценки влияния любой добавки к электролиту в отношении этой емкости. Он также показывает, как концентрация добавки, которая максимизирует эту способность, может быть определена на основе небольшого количества основных экспериментальных данных. Конечно, положительная оценка добавки в отношении энергоемкости батареи не исключает необходимости выяснить, вызывает ли добавка нежелательные побочные эффекты и в какой степени. Однако при поиске наилучших добавок для увеличения энергоемкости батареи результаты настоящей статьи могут помочь быстро отказаться от неэффективных добавок, что значительно упростит процесс выбора.
Поэтому настоящая статья по необходимости должна быть несколько ограничена по объему. По этой причине, игнорируя другие эффекты, в данной статье основное внимание уделяется влиянию добавок на энергоемкость аккумулятора. Представленный анализ обеспечивает общий способ оценки влияния любой добавки к электролиту в отношении этой емкости. Он также показывает, как концентрация добавки, которая максимизирует эту способность, может быть определена на основе небольшого количества основных экспериментальных данных. Конечно, положительная оценка добавки в отношении энергоемкости батареи не исключает необходимости выяснить, вызывает ли добавка нежелательные побочные эффекты и в какой степени. Однако при поиске наилучших добавок для увеличения энергоемкости батареи результаты настоящей статьи могут помочь быстро отказаться от неэффективных добавок, что значительно упростит процесс выбора.
Центральное место в анализе этой статьи занимает наблюдение, что при любой конечной температуре внутренняя энергия любой системы конечного объема должна быть конечной. Это следствие принципа сохранения энергии или первого закона термодинамики. При довольно широких предположениях, которым удовлетворяет большинство природных систем, и в частности растворы электролитов, это наблюдение вместе со вторым законом термодинамики подразумевает ограничение удельной свободной энергии, которую электролит может запасать и отдавать изотермически. Этот вопрос обсуждается в разделе 3. Подобный анализ ранее применялся в [10] для определения максимальной энергоемкости живой клетки — задачи, концептуально аналогичной рассматриваемой здесь.
Это следствие принципа сохранения энергии или первого закона термодинамики. При довольно широких предположениях, которым удовлетворяет большинство природных систем, и в частности растворы электролитов, это наблюдение вместе со вторым законом термодинамики подразумевает ограничение удельной свободной энергии, которую электролит может запасать и отдавать изотермически. Этот вопрос обсуждается в разделе 3. Подобный анализ ранее применялся в [10] для определения максимальной энергоемкости живой клетки — задачи, концептуально аналогичной рассматриваемой здесь.
Настоящий подход приводит к определению предельной кривой батареи (раздел 4). Эта кривая определяет предельную концентрацию компонентов электролита, при превышении которой в аккумуляторе происходят необратимые изменения или повреждения, что может привести к сокращению срока службы аккумулятора. В случае свинцово-кислотного аккумулятора это повреждение проявляется в образовании O 2 на положительном электроде при избыточном заряде или в необратимом сульфатировании отрицательного электрода при избыточном разряде. Упомянутая предельная кривая служит инструментом не только для определения значения максимального увеличения энергоемкости батареи, которое может быть достигнуто при использовании данной добавки к электролиту, но и для определения значения концентрации добавки, обеспечивающей это максимальное увеличение. . Это также приводит к установлению теоретических пределов заряда, в пределах которых батарея может работать без необратимых изменений. Практический пример применения полученных результатов приведен в разделе 5.9.0004
Упомянутая предельная кривая служит инструментом не только для определения значения максимального увеличения энергоемкости батареи, которое может быть достигнуто при использовании данной добавки к электролиту, но и для определения значения концентрации добавки, обеспечивающей это максимальное увеличение. . Это также приводит к установлению теоретических пределов заряда, в пределах которых батарея может работать без необратимых изменений. Практический пример применения полученных результатов приведен в разделе 5.9.0004
2. Свободная энергия аккумуляторных электролитов с добавками
Свободная энергия раствора или смеси представляет собой сумму свободных энергий ее компонентов. Так, если nh3O, nh3SO4 и n j (j = 1, 2, …, k) обозначают соответственно моли воды, серной кислоты и примесей, то свободная энергия Гиббса атома Pb — кислотный аккумуляторный электролит при давлении р и абсолютной температуре Т определяется по формуле:
Здесь µh3O, µh3SO4 и µ j — парциальные молярные свободные энергии Гиббса или химические потенциалы воды, серной кислоты и добавок соответственно, а C — произвольная константа. Химический потенциал любого компонента раствора или смеси всегда можно выразить в виде:
Химический потенциал любого компонента раствора или смеси всегда можно выразить в виде:
В этом уравнении μ o – химический потенциал рассматриваемого компонента в стандартном состоянии при давлении p o и температуре T, а V¯ – парциальный молярный объем того же компонента, R – универсальный газ константа, Δp означает p − p o и, наконец, a – активность или эффективная концентрация рассматриваемого компонента.
Далее молярное соотношение:
принимается за меру концентрации растворителя, а концентрации серной кислоты и добавок измеряются в моляльностях (моль на кг H 2 O) и обозначаются bh3SO4 и b j соответственно. То есть:
а также:
где M H 2 O = 18,015 × 10 −3 кг·моль −1 – молярная масса воды. В этих обозначениях активности компонентов электролита можно выразить как:
а также:
где γh3O, γh3SO4 и γ j – соответствующие коэффициенты активности, которые в общем случае зависят от nh3O, nh3SO4 и n j , кроме Т и с. Выражая µh3O, µh3SO4 и µ j в уравнении (2) и используя уравнения (6)–(8), мы можем записать уравнение (1) в виде:
Выражая µh3O, µh3SO4 и µ j в уравнении (2) и используя уравнения (6)–(8), мы можем записать уравнение (1) в виде:
При написании этого уравнения мы использовали следующее уравнение:
которая связывает парциальные молярные объемы V¯h3O, V¯h3SO4 и V¯j компонентов электролита с объемом электролита, V. известное уравнение:
Отсюда и из уравнения (9) получается свободная энергия Гельмгольца электролита:
Приведенные выше формулы являются стандартными. Однако, как видно из уравнения (7), введенный выше коэффициент активности γh3SO4 относится к общей концентрации серной кислоты. Этот коэффициент следует отличать от среднего коэффициента активности ионов серной кислоты, который может быть обозначен как γh3SO4± и обычно рассматривается в электрохимии (хотя и реже при работе со свинцово-кислотными батареями). Использование γh3SO4 вместо γh3SO4± упрощает последующие формулы, поскольку детали диссоциации серной кислоты на ионы не играют явной роли в данном подходе. Соотношение между двумя коэффициентами активности:
Соотношение между двумя коэффициентами активности:
Это можно получить из уравнения (7), если ah3SO4 выразить как функцию γh3SO4± в соответствии со стандартными формулами для ионных растворенных веществ (см., например, раздел 7.4 в [11]). Как γh3SO4, так и γh3SO4± зависят от bh3SO4 и лучше всего определяются из эксперимента.
Важное упрощение уравнения (12) достигается введением следующего уравнения:
доказательство которого в несколько измененном виде дано в [10]. В этом уравнении мы устанавливаем:
а также:
где символ Π обозначает произведение последовательности, т. е.:
Переписывая правую часть уравнения (12) как сумму двух частей и используя уравнение (14), свободную энергию Гельмгольца электролита можно в общем случае выразить как:
где функции Ψ′ и Ψ″ задаются формулой:
а также:
соответственно. Как обсуждается в следующем разделе, Ψ″ — это часть Ψ, которая определяет допустимый диапазон электролита. Таким образом, что касается определения этого диапазона, уравнение (20) позволяет нам заменить все добавки к электролиту одной-единственной фиктивной добавкой в количестве n добавить и коэффициент активности γ добавить . Такая добавка будет называться эквивалентной добавкой.
Как обсуждается в следующем разделе, Ψ″ — это часть Ψ, которая определяет допустимый диапазон электролита. Таким образом, что касается определения этого диапазона, уравнение (20) позволяет нам заменить все добавки к электролиту одной-единственной фиктивной добавкой в количестве n добавить и коэффициент активности γ добавить . Такая добавка будет называться эквивалентной добавкой.
Уравнение (20) достаточно общее. Это относится к любой комбинации добавок, будь то жидкости, твердые суспензии, коллоиды или любая их смесь. Независимо от количества и вида добавок, значения n add и γ add можно определить экспериментально, используя тот факт, что, как обсуждается в следующем разделе, существует ограничение на максимальное количество свободной энергии, которое любая конечная система может храниться в изотермических условиях. Детали соответствующей экспериментальной процедуры приведены в разделе 5.9.0004
3. Предел свободной энергии раствора электролита
При любой данной конечной температуре количество нетепловой энергии, которое конечная система может хранить или поставлять, конечно. Это прямое следствие первого закона термодинамики. Это подразумевает предел максимальной энергии, которую система может хранить. При рассмотрении в свете второго закона термодинамики предел максимальной энергии влечет за собой ограничение на состояния, которых система может достичь, не претерпевая необратимых изменений своих конститутивных свойств. При достаточно общих предположениях такое ограничение определяет область всех состояний, в которые система может попасть без необратимых изменений своих свойств. Эта область является (термодинамически) допустимым диапазоном системы. Его границы являются предельной поверхностью системы. Частный случай решений, который нас интересует в этой статье, подробно обсуждается в [10]. Систематическое введение по этому вопросу, включая общие системы, содержится в [12].
Это прямое следствие первого закона термодинамики. Это подразумевает предел максимальной энергии, которую система может хранить. При рассмотрении в свете второго закона термодинамики предел максимальной энергии влечет за собой ограничение на состояния, которых система может достичь, не претерпевая необратимых изменений своих конститутивных свойств. При достаточно общих предположениях такое ограничение определяет область всех состояний, в которые система может попасть без необратимых изменений своих свойств. Эта область является (термодинамически) допустимым диапазоном системы. Его границы являются предельной поверхностью системы. Частный случай решений, который нас интересует в этой статье, подробно обсуждается в [10]. Систематическое введение по этому вопросу, включая общие системы, содержится в [12].
Из классической термодинамики мы знаем, что при постоянной температуре количество нетепловой энергии, которую система может хранить или отдавать, равно изменению свободной энергии Гельмгольца системы. Однако не вся свободная энергия системы подвергается термодинамическому ограничению. Например, любая чисто механическая часть свободной энергии системы, например потенциальная энергия, обусловленная весом системы, не ограничивается термодинамикой. Поэтому при поиске допустимого диапазона системы следует пренебречь той частью свободной энергии системы, которая не ограничена термодинамикой.
Однако не вся свободная энергия системы подвергается термодинамическому ограничению. Например, любая чисто механическая часть свободной энергии системы, например потенциальная энергия, обусловленная весом системы, не ограничивается термодинамикой. Поэтому при поиске допустимого диапазона системы следует пренебречь той частью свободной энергии системы, которая не ограничена термодинамикой.
В данном случае часть свободной энергии электролита, не связанная термодинамикой, равна Ψ′. Это видно из уравнения (19), поскольку Ψ′ равно сумме свободных энергий компонентов электролита в их стандартном состоянии. Таким образом, Ψ′ зависит от количеств этих компонентов (nh3O, nh3SO4, n1, n2, …, nk) независимо от того, находятся ли они в растворе или отделены друг от друга. Поскольку не существует термодинамического предела для количества материала, которое можно соединить для образования системы, нет термодинамического предела для значений, которые может принимать Ψ′. Ситуация совершенно иная для Ψ″. Как следует из уравнений (6)–(8) и (20), Ψ″ зависит от концентрации вышеуказанных компонентов. Таким образом, это относится к энергии, которую эти компоненты имеют в результате их взаимного взаимодействия после их смешивания. Следовательно, любое термодинамическое ограничение энергии раствора электролита должно быть ограничением Ψ″, хотя полная свободная энергия раствора представляет собой сумму Ψ″ плюс часть энергии Ψ′, которую несет каждый компонент независимо от присутствия других компонентов.
Как следует из уравнений (6)–(8) и (20), Ψ″ зависит от концентрации вышеуказанных компонентов. Таким образом, это относится к энергии, которую эти компоненты имеют в результате их взаимного взаимодействия после их смешивания. Следовательно, любое термодинамическое ограничение энергии раствора электролита должно быть ограничением Ψ″, хотя полная свободная энергия раствора представляет собой сумму Ψ″ плюс часть энергии Ψ′, которую несет каждый компонент независимо от присутствия других компонентов.
На самом деле можно проверить, что Ψ″ — это лишь небольшая часть Ψ. Самая большая часть общей свободной энергии, которую батарея может накапливать или отдавать, связана с Ψ′ и происходит от изменений nh3O и nh3SO4, возникающих в результате химических реакций, происходящих в электролите. Однако при всей своей малости Ψ″ определяет допустимый диапазон электролита. Как следствие, Ψ″ устанавливает предел общей свободной энергии батареи, Ψ, поскольку ограничивает диапазон изменения nh3O и nh3SO4. Аналогичная ситуация может иметь место и для растворов, содержащих химически реагирующие компоненты. Например, в случае живой клетки та часть свободной энергии цитозоля, которая определяет допустимый диапазон клетки, составляет лишь долю полной свободной энергии цитозоля [10]. И в этом случае малая часть полной свободной энергии цитозоля ограничивает количество компонентов раствора, тем самым ограничивая энергию, которую живая клетка может запасать или выделять, а значит, и ее работоспособность.
Аналогичная ситуация может иметь место и для растворов, содержащих химически реагирующие компоненты. Например, в случае живой клетки та часть свободной энергии цитозоля, которая определяет допустимый диапазон клетки, составляет лишь долю полной свободной энергии цитозоля [10]. И в этом случае малая часть полной свободной энергии цитозоля ограничивает количество компонентов раствора, тем самым ограничивая энергию, которую живая клетка может запасать или выделять, а значит, и ее работоспособность.
Чтобы следующий анализ не зависел от количества электролита, удобно ссылаться на молярную концентрацию Ψ″ на кг растворителя. Эта концентрация энергии обозначается ψ″ и получается путем деления обеих частей уравнения (20) на nh3OMh3O (т. е. на вес в килограммах воды, содержащейся в электролите):
где V¯ – объем электролита на моль растворителя:
В обоих приведенных выше уравнениях nh3O является переменной, поскольку количество молей воды в электролите меняется по мере зарядки или разрядки аккумулятора.
В дальнейшем температура считается постоянной. Кроме того, зависимость свободной энергии от р будет игнорироваться, как это обычно делается в отсутствие газообразных фаз, а также при работе при постоянном или близком к нему давлении. Таким образом, если ψmax″ является значением, которое ψ″ достигает на термодинамическом пределе, упомянутом выше, следующее соотношение:
относится ко всем состояниям, которых может достичь электролит при рассматриваемой температуре. Вместе с уравнением (21) уравнение (23) определяет допустимый диапазон электролита в пространстве переменных nh3O, nh3SO4, nadd. Предельная поверхность электролита является границей этого диапазона:
Следовательно, она эквипотенциальна для ψ″ или Ψ″ (однако одна и та же поверхность не является эквипотенциальной для полной свободной энергии системы или ее части Ψ′, как уравнения (18) и (19 ) показывать).
Несмотря на то, что V¯ является переменной величиной, она претерпевает незначительные изменения (менее 0,3%) при нормальной работе от батареи. Что касается настоящего анализа, член p° V¯/Mh3O, фигурирующий в уравнении (21), можно рассматривать как константу. Как следствие, его вкладом в ψ″ и ψmax″ можно в хорошем приближении пренебречь при применении уравнений (23) и (24), поскольку добавление или вычитание постоянного члена к обеим частям этих соотношений несущественно. Соответственно, при определении допустимого диапазона и предельной поверхности электролита или предельной кривой батареи в дальнейшем мы будем игнорировать член −p° V¯/Mh3O в правой части уравнения (21). С этой оговоркой допустимый диапазон электролита может быть выражен как:
Что касается настоящего анализа, член p° V¯/Mh3O, фигурирующий в уравнении (21), можно рассматривать как константу. Как следствие, его вкладом в ψ″ и ψmax″ можно в хорошем приближении пренебречь при применении уравнений (23) и (24), поскольку добавление или вычитание постоянного члена к обеим частям этих соотношений несущественно. Соответственно, при определении допустимого диапазона и предельной поверхности электролита или предельной кривой батареи в дальнейшем мы будем игнорировать член −p° V¯/Mh3O в правой части уравнения (21). С этой оговоркой допустимый диапазон электролита может быть выражен как:
В трехмерном пространстве (nh3O, nh3SO4, n добавить ) это соотношение определяет область всех состояний, которых может достичь электролит без необратимых изменений. Границей этой области является предельная поверхность электролита:
и представляет собой поверхность в упомянутом выше трехмерном пространстве.
4. Допустимый диапазон батареи и предельная кривая
Не все состояния допустимого диапазона из уравнения (25) доступны для электролита внутри батареи. В нормальных условиях эксплуатации батарея не обменивается веществом с окружающей средой. В этих условиях общее количество молекул воды и серной кислоты внутри аккумулятора остается постоянным. Это прямое следствие известной общей реакции, управляющей работой батареи:
Реакция идет слева направо во время разрядки аккумулятора. Это производит две молекулы воды на каждые две молекулы серной кислоты, которые потребляются. Зарядка батареи запускает реакцию в противоположном направлении, таким образом производя две молекулы серной кислоты на каждые две молекулы потребляемой воды. В обоих случаях сумма nh3O и nh3SO4 остается постоянной. Таким образом, в любой момент процесса зарядки или разрядки аккумулятора мы имеем:
где n¯ — константа. Значение этой константы зависит от подготовки батареи и может быть определено по значениям nh3O и nh3SO4 в любой момент срока службы батареи. В частности, пусть nh3Oo и nh3SO4o — значения nh3O и nh3SO4 электролита, который необходимо ввести в батарею. Они совпадают со значениями nh3O и nh3SO4 электролита внутри батареи, поскольку батарея начинает работать после заполнения. Следовательно, должно выполняться следующее уравнение:
Значение этой константы зависит от подготовки батареи и может быть определено по значениям nh3O и nh3SO4 в любой момент срока службы батареи. В частности, пусть nh3Oo и nh3SO4o — значения nh3O и nh3SO4 электролита, который необходимо ввести в батарею. Они совпадают со значениями nh3O и nh3SO4 электролита внутри батареи, поскольку батарея начинает работать после заполнения. Следовательно, должно выполняться следующее уравнение:
который фиксирует n¯.
Уравнение (28) можно использовать для исключения переменной nh3O из уравнений (25) и (26). Это уменьшает количество независимых переменных, появляющихся в этих уравнениях, тем самым еще больше ограничивая диапазон состояний, которые может достичь электролит. Более явно, вводя уравнение (28) в уравнение (25), мы получаем допустимый диапазон батареи:
Это область плоскости (nh3SO4, n добавить ), которая содержит все состояния, которые электролит может достичь при нормальной работе батареи без необратимых изменений. Его границей является предельная кривая батареи. Его получают, взяв знак равенства в уравнении (30):
Его границей является предельная кривая батареи. Его получают, взяв знак равенства в уравнении (30):
Эта кривая на плоскости (nh3SO4, n add ) ограничивает область всех состояний, которых электролит может достичь обратимо при работе внутри батареи.
Уравнения (27)–(31) применимы к свинцово-кислотным батареям, содержащим нереагирующие добавки к электролиту, т. е. добавки, которые не вступают в химическую реакцию между собой или с другими компонентами батареи. Нереагирующие добавки обычно используются в коммерческих батареях. Как указывалось ранее, это единственные добавки, о которых мы говорим в этой статье. Те же уравнения применимы, в частности, и при отсутствии добавок к электролиту, когда n add = 0.
Типичная предельная кривая ψ″ = ψmax″ и, таким образом, сдвигает состояние батареи вверх, т. е. по линии AB на рис. 1. Допустимый диапазон батареи — заштрихованная область внутри кривой. Количество добавки в электролите остается постоянным во время заряда и разряда, так как добавка химически неактивна. Таким образом, зарядка или разрядка батареи в этом диапазоне смещает состояние батареи вверх и вниз по вертикальной линии, n добавить = постоянное, в плоскости рисунка 1. В электролите происходят необратимые изменения, если предельная кривая батареи превышен. В частности, зарядка аккумулятора увеличивает nh3SO4 и, таким образом, сдвигает состояние аккумулятора вверх, т. е. по линии АВ на рис. 1.
Таким образом, зарядка или разрядка батареи в этом диапазоне смещает состояние батареи вверх и вниз по вертикальной линии, n добавить = постоянное, в плоскости рисунка 1. В электролите происходят необратимые изменения, если предельная кривая батареи превышен. В частности, зарядка аккумулятора увеличивает nh3SO4 и, таким образом, сдвигает состояние аккумулятора вверх, т. е. по линии АВ на рис. 1.
Процесс обратим, пока состояние батареи остается в пределах сегмента AB. Однако при превышении точки А на положительном электроде происходит выделение кислорода, что делает процесс необратимым. Аналогичная ситуация возникает при разрядке. В этом случае в процессе разрядки расходуется серная кислота, и состояние батареи движется вниз по линии AB. Точка B на предельной кривой батареи — это предел обратимого разряда. За пределами этой точки напряжение батареи становится ниже напряжения, необходимого для поддержания реакции отрицательного электрода:
в химическом равновесии. Это приводит к необратимому протеканию реакции вправо. Это явление происходит сравнительно быстро и известно как сульфатация. Это приводит к образованию нерастворимых кристаллов PbSO 2 на отрицательном электроде с сопутствующим выделением водорода. Выделение кислорода и водорода в пределах допустимого диапазона связано с электрохимическими окнами воды. Читатель может обратиться к соответствующей литературе за подробностями о химических реакциях, которые регулируют электрохимическую стабильность воды в водных электролитах (см., например, ([13,14,15,16,17])).
Это приводит к необратимому протеканию реакции вправо. Это явление происходит сравнительно быстро и известно как сульфатация. Это приводит к образованию нерастворимых кристаллов PbSO 2 на отрицательном электроде с сопутствующим выделением водорода. Выделение кислорода и водорода в пределах допустимого диапазона связано с электрохимическими окнами воды. Читатель может обратиться к соответствующей литературе за подробностями о химических реакциях, которые регулируют электрохимическую стабильность воды в водных электролитах (см., например, ([13,14,15,16,17])).
Ширина допустимого диапазона вдоль вертикальной линии через n добавить обозначена как Δnh3SO4 на рисунке 1. Эта ширина представляет собой максимальное количество серной кислоты, которое на килограмм воды-растворителя может обратимо реагировать в соответствии с уравнением (27 ). Таким образом, чем больше эта ширина, тем большее количество энергии аккумулятор может хранить и производить без ухудшения качества электролита. Максимальное значение Δnh3SO4 достигается при n add = nadd∗ и обозначено на рисунке выше как Δnh3SO4∗. Поскольку количество воды-растворителя зависит от состояния заряда батареи, может быть удобно определять концентрацию добавки относительно фиксированного состояния заряда батареи. Это будет считаться гипотетическим состоянием полного разряда, которого батарея достигнет, когда вся серная кислота в электролите будет израсходована в соответствии с уравнением (27). В этом состоянии количество воды в электролите будет n h3O= n¯, согласно уравнению (28). Следовательно, применительно к этому гипотетическому состоянию молярная концентрация добавки к электролиту, соответствующая nadd∗, определяется выражением:
Максимальное значение Δnh3SO4 достигается при n add = nadd∗ и обозначено на рисунке выше как Δnh3SO4∗. Поскольку количество воды-растворителя зависит от состояния заряда батареи, может быть удобно определять концентрацию добавки относительно фиксированного состояния заряда батареи. Это будет считаться гипотетическим состоянием полного разряда, которого батарея достигнет, когда вся серная кислота в электролите будет израсходована в соответствии с уравнением (27). В этом состоянии количество воды в электролите будет n h3O= n¯, согласно уравнению (28). Следовательно, применительно к этому гипотетическому состоянию молярная концентрация добавки к электролиту, соответствующая nadd∗, определяется выражением:
Это можно рассматривать как номинальную молярность добавки, которая требуется для обеспечения максимальной емкости накопления энергии в батарее.
Пусть Δnh3SO4o будет значением Δnh3SO4, когда электролит батареи не содержит добавок (см. рис. 1). Поскольку энергия, которую батарея может накапливать или отдавать, пропорциональна количеству молей серной кислоты, которые подчиняются уравнению (27), соотношение:
рис. 1). Поскольку энергия, которую батарея может накапливать или отдавать, пропорциональна количеству молей серной кислоты, которые подчиняются уравнению (27), соотношение:
представляет собой наибольшее относительное увеличение максимальной емкости накопления энергии, которое может быть получено от данной добавки к электролиту. Конечно, η max зависит от используемой добавки из-за зависимости от добавки предельной кривой батареи.
5. Экспериментальное определение предельной кривой
Для определения предельной кривой батареи нам необходимо знать значения ψmax″ и γ добавить , которые необходимо ввести в уравнение (31). Эти значения могут быть определены экспериментально следующим образом: Начнем с наблюдения того, что уравнение (31) верно, в частности, когда электролит не содержит добавок. В этом случае № добавить = 0 и уравнение (31) сводится к:
Это уравнение применимо к пределу допустимого диапазона батареи. Появляющаяся здесь величина n¯ определяется уравнением (29). Это зависит от подготовки батареи, но не от наличия добавок к электролиту. Таким образом, работая на аккумуляторе, лишенном добавки к электролиту, мы увеличиваем состояние заряда аккумулятора до тех пор, пока не достигнем предельной точки, за которой начинает выделяться кислород на положительном электроде в условиях разомкнутой цепи (точка A° на рис. 1). Появление этого необратимого явления свидетельствует о том, что состояние батареи достигло предельной кривой. Мы определяем значение nh3SO4 на этом пределе и подставляем его в уравнение (35). Таким образом, мы можем вычислить ψmax″.
Появляющаяся здесь величина n¯ определяется уравнением (29). Это зависит от подготовки батареи, но не от наличия добавок к электролиту. Таким образом, работая на аккумуляторе, лишенном добавки к электролиту, мы увеличиваем состояние заряда аккумулятора до тех пор, пока не достигнем предельной точки, за которой начинает выделяться кислород на положительном электроде в условиях разомкнутой цепи (точка A° на рис. 1). Появление этого необратимого явления свидетельствует о том, что состояние батареи достигло предельной кривой. Мы определяем значение nh3SO4 на этом пределе и подставляем его в уравнение (35). Таким образом, мы можем вычислить ψmax″.
Как известно, концентрация серной кислоты и напряжение батареи связаны друг с другом (см., например, [18,19,20,21]). Следовательно, вместо того, чтобы определять предельное значение nh3SO4, мы можем определить максимальное напряжение холостого хода, при котором батарея поддерживает свой заряд без образования кислорода на положительном электроде. Это напряжение значительно выше стандартного напряжения (1,229 В) электролиза воды [22] из-за перенапряжения, возникающего на электродах батареи. Степень перенапряжения зависит от свойства поверхности электродов и наличия в электродах небольших количеств различных добавок, вводимых при их изготовлении. Как видно из уравнений (20) и (21), функции Ψ″ и ψ″ не зависят от свободной энергии электродов. Однако перенапряжение, создаваемое электродами, влияет на допустимый диапазон батареи и предельную характеристику, поскольку влияет на предельное значение nh3SO4 и, следовательно, на значение ψmax″. Это делает допустимый диапазон батареи и предельную кривую зависящими от свойств батареи в целом, а не только от свойств ее электролита.
Это напряжение значительно выше стандартного напряжения (1,229 В) электролиза воды [22] из-за перенапряжения, возникающего на электродах батареи. Степень перенапряжения зависит от свойства поверхности электродов и наличия в электродах небольших количеств различных добавок, вводимых при их изготовлении. Как видно из уравнений (20) и (21), функции Ψ″ и ψ″ не зависят от свободной энергии электродов. Однако перенапряжение, создаваемое электродами, влияет на допустимый диапазон батареи и предельную характеристику, поскольку влияет на предельное значение nh3SO4 и, следовательно, на значение ψmax″. Это делает допустимый диапазон батареи и предельную кривую зависящими от свойств батареи в целом, а не только от свойств ее электролита.
Процедура определения γ add аналогична процедуре определения ψmax″. Однако в этом случае электролит батареи должен содержать известное количество добавки. Снова заряжаем аккумулятор до предела, при котором на положительном электроде выделяется кислород в условиях разомкнутой цепи. Определяем соответствующее значение nh3SO4 и подставляем его вместе с рассматриваемым значением n и добавляем в уравнение (31). Поскольку ψmax″ уже определено, единственным неизвестным в этом уравнении является γ добавить , что можно, таким образом, определить. Из-за наличия трансцендентных членов значение γ add лучше всего вычислять графически или численно.
Определяем соответствующее значение nh3SO4 и подставляем его вместе с рассматриваемым значением n и добавляем в уравнение (31). Поскольку ψmax″ уже определено, единственным неизвестным в этом уравнении является γ добавить , что можно, таким образом, определить. Из-за наличия трансцендентных членов значение γ add лучше всего вычислять графически или численно.
Для примера возьмем обычный автомобильный аккумулятор при комнатной температуре (T = 25 °C = 298,15 K). Мы предполагаем, что на момент изготовления электролит в аккумуляторе содержит 1 кг воды с молярной концентрацией серной кислоты bh3SO4o = 6 моль/кг. Это означает, что nh3Oo = 55,51 моль и nh3SO4o = 6 моль. Таким образом, n¯ = 55,51 + 6 = 61,51 моль, как следует из уравнения (29). Оставив электролит без присадок, зарядим батарею и найдем, что bh3SO4 = 7,25 моль/кг — это наибольшая концентрация серной кислоты, которую батарея может поддерживать в условиях разомкнутой цепи без образования кислорода на своем положительном электроде (эта концентрация соответствует напряжению 2,16 В — или 12,96 В для шестиэлементной батареи — по имеющимся в литературе данным [19]). Как видно, заряд и разряд батареи происходят при постоянном n¯. Таким образом, с учетом уравнения (28) находим, что приведенное выше значение bh3SO4 = 7,25 моль/кг означает nh3SO4 = 7,10 моль и nh3O = 54,41 моль в электролите батареи. Вводя в уравнение (35) значения γh3O и γh3SO4, соответствующие этому значению bh3SO4, доступные из литературы и приведенные в Приложении, и учитывая, что R = 8,3143 Дж·К −1 ·моль −1 и Mh3O = 18,015 × 10 −3 кг·моль −1 , вычисляем, что для рассматриваемой батареи ψmax″ = −20,25 Дж·кг −1 .
Как видно, заряд и разряд батареи происходят при постоянном n¯. Таким образом, с учетом уравнения (28) находим, что приведенное выше значение bh3SO4 = 7,25 моль/кг означает nh3SO4 = 7,10 моль и nh3O = 54,41 моль в электролите батареи. Вводя в уравнение (35) значения γh3O и γh3SO4, соответствующие этому значению bh3SO4, доступные из литературы и приведенные в Приложении, и учитывая, что R = 8,3143 Дж·К −1 ·моль −1 и Mh3O = 18,015 × 10 −3 кг·моль −1 , вычисляем, что для рассматриваемой батареи ψmax″ = −20,25 Дж·кг −1 .
Для определения γ добавить , добавляем произвольное количество рассматриваемой добавки в электролит аккумулятора. Пусть n добавляет, например, = 5 моль. Эксплуатируя модифицированную таким образом батарею, мы находим, что предел разомкнутой цепи для выделения кислорода на положительном электроде наступает, когда заряд батареи соответствует количеству серной кислоты, скажем, nh3SO4 = 6,74 моль. Подставляя это значение nh3SO4 в уравнение (35), мы вычисляем, что γ добавить = 0,64, что можно проверить из того же уравнения, если установить n добавить = 5 моль, n¯ = 61,51 моль и ψmax″ = -20,25 Дж·кг -1 .
Подставляя это значение nh3SO4 в уравнение (35), мы вычисляем, что γ добавить = 0,64, что можно проверить из того же уравнения, если установить n добавить = 5 моль, n¯ = 61,51 моль и ψmax″ = -20,25 Дж·кг -1 .
Наконец, подставляя эти значения n¯, ψmax″ и γ , добавляя в уравнение (35) и используя выражения γh3O и γh3SO4, приведенные в Приложении, мы получаем аналитическое выражение предельной кривой рассматриваемого аккумулятора. Эта кривая представлена на рис. 2. Из этого же рисунка находим, что Δnh3SO4o = 5,48 моль и Δnh3SO4∗ = 6,14 моль. Отсюда следует, что η max = 0,12 согласно уравнению (34). Таким образом, рассматриваемая в данном примере добавка к электролиту может увеличить энергоемкость батареи до 12 %. Как показано на рисунке, количество добавки, необходимое для получения максимальной емкости накопления энергии, составляет nadd∗ = 1,48 моль. Соответствующая номинальная молярность добавки равна badd* = 1,34 моль/кг согласно уравнению (33).
Различные добавки могут по-разному влиять на батарею. Например, для того же аккумулятора, рассмотренного в приведенном выше примере, добавка с γ добавить = 0,3 может увеличить емкость аккумулятора на 25%. Это можно легко проверить из уравнения (35), построив предельную кривую для γ add = 0,3 и тех же значений n¯ и ψmax″, что и выше. В этом случае количество добавки, создающей максимальную энергоаккумулирующую способность, будет nadd* = 3,23 моль, что означает badd* = 2,91 моль/кг.
В приведенном выше анализе мы рассматривали γ add как константу, пренебрегая, таким образом, любой возможной зависимостью γ добавить по концентрации присадки. Это может быть приемлемым, если концентрация добавки умеренно низкая (как это имеет место во многих приложениях) или если мы ограничиваем наше внимание достаточно небольшим участком предельной кривой. Если требуется более высокая точность, описанную выше процедуру определения γ add можно повторить несколько раз для необходимого количества различных значений n add . Полученные таким образом значения γ add можно использовать для определения функции γ добавить (n добавить ), который можно заменить на γ добавить в уравнение (35), если приближение γ добавить = const. оказывается неадекватным.
Полученные таким образом значения γ add можно использовать для определения функции γ добавить (n добавить ), который можно заменить на γ добавить в уравнение (35), если приближение γ добавить = const. оказывается неадекватным.
Вместо того, чтобы заряжать аккумулятор до предела выделения кислорода, представленного точкой A° на рисунке 1, мы могли бы, в принципе, определить ψmax″, разрядив аккумулятор без добавок до точки B° на том же рисунке. Это точка предельной поверхности батареи, в которой начинается сульфатация отрицательного электрода. Как только определена концентрация серной кислоты, соответствующая этому нижнему пределу, можно определить предельную кривую, как описано выше. Обе процедуры должны давать одно и то же значение ψmax″, поскольку и A°, и B° принадлежат одной и той же кривой ψ″=ψmax″. Однако ссылка на предел выделения кислорода представляется более практичной, так как сульфатирование — довольно медленное явление.
6. Выводы
Известно, что на энергоемкость свинцово-кислотного аккумулятора может влиять наличие добавок в его электролите. Понятие эквивалентной добавки, определенное в данной работе, помогает анализировать влияние химически инертных добавок и смесей таких добавок на энергоемкость батареи. Это может быть применено для определения целой области концентраций электролита, называемой допустимым диапазоном батареи, в пределах которой не происходит необратимых изменений в батарее во время заряда или разряда. Границей этой области является предельная кривая батареи. Это соответствует концентрациям серной кислоты и, следовательно, диапазону напряжений холостого хода, превышение которых не может привести к необратимым изменениям в аккумуляторе. Предельная кривая батареи может быть построена из нескольких экспериментов, в которых батарея заряжается (или разряжается) при различных концентрациях добавок. Это дает полезную информацию об эффективности добавки для увеличения энергоемкости батареи и о наилучшей концентрации добавки для этой цели. Практические последствия выбора наилучшей добавки для использования очевидны. Однако следует иметь в виду, что добавка также может вызывать нежелательные побочные эффекты, которые не рассматриваются в настоящей работе и требуют надлежащего изучения, прежде чем любое улучшение энергоемкости батареи в результате добавки может считаться практически целесообразным.
Практические последствия выбора наилучшей добавки для использования очевидны. Однако следует иметь в виду, что добавка также может вызывать нежелательные побочные эффекты, которые не рассматриваются в настоящей работе и требуют надлежащего изучения, прежде чем любое улучшение энергоемкости батареи в результате добавки может считаться практически целесообразным.
Конфликт интересов
Автор заявляет об отсутствии конфликта интересов.
Приложение. Коэффициенты активности воды и серной кислоты в растворе
При выражении в молялях концентрация растворенного вещества не зависит от присутствия других растворенных веществ в том же растворе. Более того, если концентрация растворенных веществ достаточно мала, на коэффициент активности каждого растворенного вещества лишь незначительно влияет присутствие других растворенных веществ в том же растворе. По этой причине из-за отсутствия более точных данных о влиянии аддиктивных веществ на коэффициенты активности электролита коэффициент активности серной кислоты (γh3SO4) принимается равным γh3SO4o=γh3SO4o(bh3SO4), что и предполагает отсутствие добавок. Другими словами:
Другими словами:
где функция γh3SO4(nh3O,nh3SO4) получается из γh3SO4o(bh3SO4) после подстановки уравнения (4).
С другой стороны, коэффициент активности растворителя зависит от его мольного соотношения. В рассматриваемом случае растворителем является вода, и ее мольное соотношение xh3O зависит от количества серной кислоты и добавок, содержащихся в электролите, что видно из уравнения (3). Однако анализ настоящей статьи касается нереакционноспособных добавок при сравнительно низкой концентрации. В этих условиях можно ожидать, что влияние добавок на коэффициент активности растворителя γh3O будет иметь второстепенное значение. По этой причине, а также ввиду уже упомянутой скудости экспериментальных данных, значения γh3O электролита с добавками считаются совпадающими со значениями электролита без добавок, γh3Oo=γh3Oo(xh3Oo). Введенное здесь количество xh3Oo представляет собой мольную долю растворителя, когда n добавить = 0. То есть:
То есть:
Это предположение о γh3O означает, таким образом:
Экспериментальные значения, полученные функциями γh3SO4o(bh3SO4) и γh3Oo(xh3Oo) для широкого диапазона концентраций, описаны во многих статьях и книгах. Для критического обзора этих экспериментальных данных читатель может обратиться к [23,24]. На основе этих данных предполагается, что уравнение (A1) аппроксимируется выражением:
представлено графически на следующем рисунке A1.
Рисунок A1. График уравнения (A4), показывающий зависимость γh3SO4 от моляльности серной кислоты в водных растворах. Экспериментальные значения ( ) γh3SO4o взяты из работы Буллока [24].
Рисунок A1. График уравнения (A4), показывающий зависимость γh3SO4 от моляльности серной кислоты в водных растворах. Экспериментальные значения ( ) γh3SO4o взяты из работы Буллока [24].
Что касается растворителя, следующая полиномиальная аппроксимация обеспечивает хорошее приближение к хорошо установленным экспериментальным данным ([23,24]) относительно активности воды в водных растворах серной кислоты при 0,4 Это уравнение представлено на рис. A2 вместе со значениями γh3Oo, полученными из данных, представленных в [24]. Уравнения (A4) и (A5) использовались для определения предельной кривой батареи в примере, представленном в Разделе 5. Рисунок A2. Кривая уравнения (A5), показывающая зависимость γh3O от xh3O для водных растворов серной кислоты. Значения ( ) γh3Oo рассчитаны на основе экспериментальных данных, приведенных в обзоре Bullock [24]. Рисунок A2. Кривая уравнения (A5), показывающая зависимость γh3O от xh3O для водных растворов серной кислоты. Значения ( ) γh3Oo рассчитаны на основе экспериментальных данных, приведенных в обзоре Bullock [24].
Ссылки
 Р. Влияние кислых ионных жидкостей в качестве добавки к электролиту на электрохимическое и коррозионное поведение свинцово-кислотных аккумуляторов. J. Твердотельная электрохимия. 2011 , 15, 421–430. [Google Scholar] [CrossRef]
Р. Влияние кислых ионных жидкостей в качестве добавки к электролиту на электрохимическое и коррозионное поведение свинцово-кислотных аккумуляторов. J. Твердотельная электрохимия. 2011 , 15, 421–430. [Google Scholar] [CrossRef] ; Research Studies Press: Baldock, UK, 2003. [Google Scholar]
; Research Studies Press: Baldock, UK, 2003. [Google Scholar]
