Приготовление электролита для аккумуляторов своими руками
В настоящее время выбор аккумуляторных батарей огромен — в продаже можно найти уже готовые к использованию источники питания, а также сухозаряженные батареи, которые требуют осуществить приготовление электролита и его заливку до начала эксплуатации. Дальнейшее обслуживание аккумуляторов многие часто осуществляют в сервисах. По разным причинам может возникнуть необходимость самостоятельно приготовить раствор. Чтобы это мероприятие увенчалось успехом, следует знать, как сделать электролит в домашних условиях.
Содержание:
- 1 Что такое электролит?
- 2 Концентрация серной кислоты в АКБ
- 3 Отличия электролитов для разных типов аккумуляторов
- 3.1 Щелочные АКБ
- 3.2 Кислотные АКБ
- 4 Другие виды АКБ: можно ли приготовить электролит для них самостоятельно?
- 4.1 Кадмиевоникелевые и железоникелевые аккумуляторы
- 5 Как правильно приготовить электролит в домашних условиях: техника безопасности
- 5.
 1 Оборудование
1 Оборудование - 5.2 Последовательность процесса: делаем электролит для кислотно-свинцового источника питания
- 5.
- 6 Способ развести электролит для щелочного источника питания
Что такое электролит?
Электролит — электропроводящий раствор, содержащий в своём составе дистиллированную воду и серную кислоту, едкий калий или натрий в зависимости от типа источника питания.
Концентрация серной кислоты в АКБ
Этот показатель кислотности напрямую зависит от необходимой плотности электролита. Изначально средняя концентрация этого раствора в автомобильном аккумуляторе — около 40% в зависимости от температуры и климата, в которых используется источник питания. Во время эксплуатации концентрация кислоты падает до 10–20%, что сказывается на работоспособности АКБ.
Вместе с тем стоит понимать, что аккумуляторная серная составляющая — наичистейшая жидкость, которая на 93% состоит непосредственно из кислоты остальные 7% — примеси. На территории России производство этого химиката строго регламентировано — продукция должна соответствовать требованиям ГОСТ.
Отличия электролитов для разных типов аккумуляторов
Несмотря на то что принцип работы раствора одинаков для разных источников питания, следует знать о некоторых различиях составов. В зависимости от состава принято выделять щелочной и кислотный электролиты.
Щелочные АКБ
Этот вид источников питания характеризуется наличием гидроокиси никеля, окиси бария и графита. Электролит в этом виде аккумуляторов представляет собой 20% раствор едкого калия. Традиционно используется добавка моногидрата лития, которая позволяет продлить срок эксплуатации АКБ.
Щелочные источники питания отличаются отсутствием взаимодействия калийного раствора с веществами, образуемыми во время работы аккумулятора, что способствует аксимальному уменьшению расхода.
Кислотные АКБ
Этот вид источников питания является одним из самых традиционных, поэтому и раствор в них знаком многим — смесь дистиллированной воды и серного раствора. Концентрат электролита для свинцово-кислотных аккумуляторов дешёво стоит и характеризуется способностью проводить ток большой величины. Плотность жидкости должна соответствовать климатическим показателям.
Плотность жидкости должна соответствовать климатическим показателям.
Таблица 1. Рекомендуемая плотность электролита
Другие виды АКБ: можно ли приготовить электролит для них самостоятельно?
Отдельно хотелось бы обратить внимание на современные свинцово-кислотные источники питания — гелевые и AGM. Они также могут быть заправлены собственноручно приготовленным раствором, который в них находится в специфической форме — в виде геля или внутри сепараторов. Для заправки гелевых аккумуляторов понадобится ещё один химический компонент — силикагель, который загустит кислотный раствор.
Кадмиевоникелевые и железоникелевые аккумуляторы
В отличие от свинцовых источников питания, кадмиево- и железоникелевые заливаются щелочным растовром, который является смесью дистиллированной воды и едкого калия или натрия. Гидроксид лития, входящий в состав этого раствора для определённых температурных режимов, позволяет увеличить срок службы АКБ.
Таблица 2.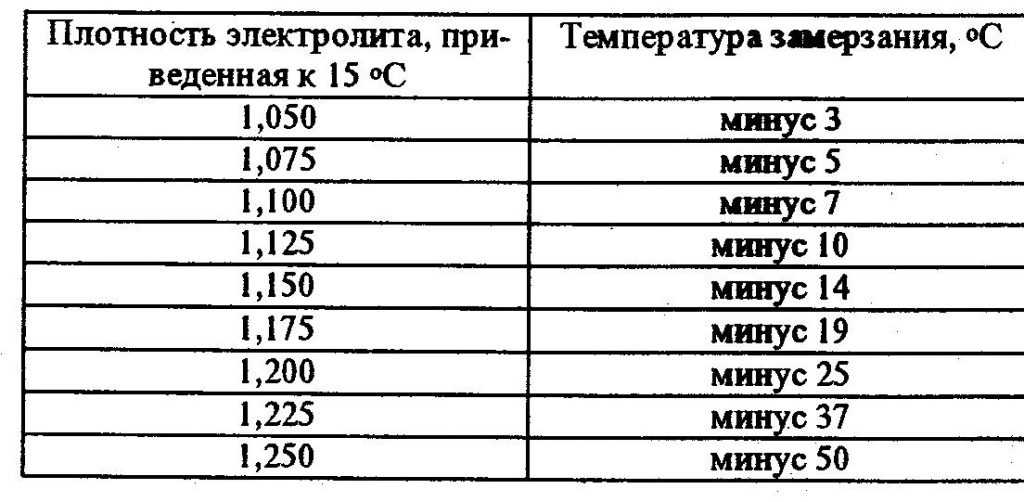 Состав и плотность электролита для кадмиево- и железоникелевых и аккумуляторов.
Состав и плотность электролита для кадмиево- и железоникелевых и аккумуляторов.
Железоникелевые источники питания рекомендуется эксплуатировать в тех же условиях, что и кадмиево-никелевые. Однако стоит отметить, что они более восприимчивы к низким температурам. Поэтому их следует использовать до минус 20 градусов.
Как правильно приготовить электролит в домашних условиях: техника безопасности
Приготовление раствора — работа с кислотами и щелочами, поэтому соблюдение мер предосторожности необходимо для самых опытных людей. Перед началом действия подготовьте средства защиты:
- резиновые перчатки
- одежду и фартук, устойчивый химическим веществам;
- защитные очки;
- нашатырный спирт, кальцинированную соду или борный раствор, чтобы нейтрализовать кислоту и щёлочь.
Оборудование
Для приготовления аккумуляторного электролита помимо самого источника питания потребуются следующие предметы:
- ёмкость и палочка, устойчивые к воздействию кислот и щелочей;
- дистиллированная вода;
- инструменты для измерения уровня, плотности и температуры раствора;
- аккумуляторная серная жидкость — для кислотной АКБ, твёрдые или жидкие щелочи, литий — для соответствующих видов АКБ, силикагель — для гелевых аккумуляторов.
Последовательность процесса: делаем электролит для кислотно-свинцового источника питания
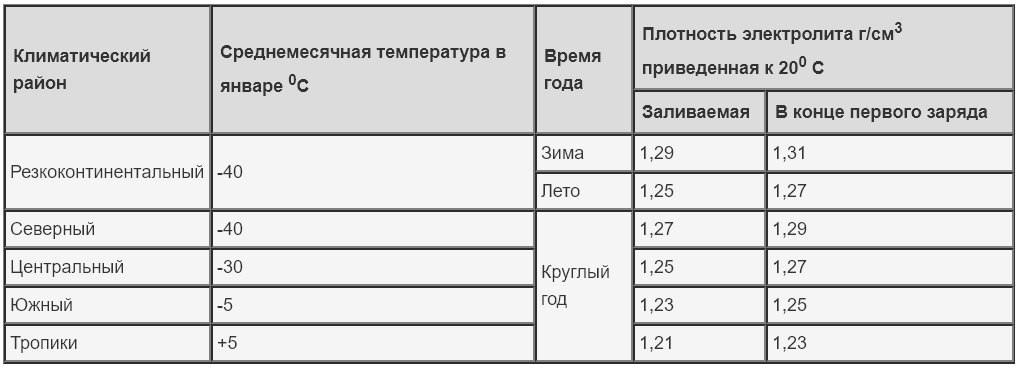
Перед началом работ ознакомьтесь с информацией, приведённой в таблице 3. Она позволит выбрать необходимый объем жидкостей. В аккумуляторах залито от 2,6 до 3,7 литра кислотного раствора. Мы рекомендуем разводить примерно 4л электролита.
Таблица 3. Пропорции воды и серной кислоты.
- В ёмкость, устойчивую к едким веществам, налейте нужный объем воды.
- Разбавлять воду кислотой следует постепенно.
- По окончании процесса вливания замеряйте плотность получившегося электролита с помощью ареометра.
- Дайте составу отстояться около 12 часов.
Таблица 4. Плотность электролита для разных климатов.
Концентрация кислотного раствора должна соотноситься с минимальной температурой, при которой эксплуатируется аккумулятор. Если жидкость получилась слишком концентрированной, её необходимо разбавить дистиллированной водой.
Смотрите видео, как измерить плотность электролита.
Внимание! Вливать воду в кислоту нельзя! В результате этой химической реакции может возникнуть закипание состава, что приведёт к его расплескиванию и возможности получить кислотные ожоги!
Обращаем ваше внимание, что во время смешивания компонентов выделяется тепло. В подготовленный аккумулятор следует заливать остывший раствор.
Способ развести электролит для щелочного источника питания
Плотность и количество электролита в таких аккумуляторах указана в инструкции по эксплуатации источника питания или на сайте компании-производителя.
Необходимая плотность раствора | Количество твёрдой щелочи равняется количеству электролита, разделенному на |
1,17–1,19 г/см³ | 5 |
1,19–1,21 г/см³ | 3 |
1,25–1,27 г/см³ | 2 |
- Влейте в посуду дистиллированную воду.

- Добавьте щелочь.
- Смешайте раствор, герметично его закройте и дайте настояться в течение 6 часов.
- По истечении времени слейте образовавшийся светлый раствор — электролит готов.
При появлении осадка следует его перемешивать. Если к концу отстаивания он остаётся, слейте электролит так, чтобы осадок не попал в аккумулятор — это приведёт к уменьшению срока его эксплуатации.
Внимание! Во время работ температура щелочного раствора не должна превышать 25 градусов по Цельсию. Если жидкость чрезмерно нагревается, охладите её.
После приведения раствора к комнатной температуре и его заливке в аккумулятор, источник питания необходимо полностью зарядить током, составляющим 10% от ёмкости АКБ (60Ач — 6А).
Как видите, приготовление раствора электролита не такое сложное дело. Главное, следует чётко определиться с необходимым количеством ингредиентов и помнить о безопасности. Вы пробовали развести электролит своими руками? Поделитесь опытом с нашими читателями в комментариях.
Виды, Составы и Как приготовить
Без электролитов невозможна работа перезаряжаемых источников электроэнергии. Существует несколько основных типов таких веществ, которые наиболее часто используются в современных устройствах этого типа. О том, какие существуют виды электролитов, а также каким образом можно приготовить смесь для заливки в аккумуляторную батарею, будет подробно рассказано в этой статье.
Содрежание
Что такое электролит и для чего он нужен
Электролит представляет собой кислотный или щелочной раствор, который принимает участие в химической реакции. Во время зарядки батареи, плотность токопроводящей жидкости повышается, поэтому по этому параметру можно довольно точно судить о степени заряженности аккумулятора.
Важно не только наличие токопроводящей жидкости в батарее, но также и качество смеси. Если приготовление раствора серной кислоты или щёлочи с водой производилось с нарушением технологии, то аккумулятор будет работать нестабильно либо полностью выйдет из строя в течение непродолжительного времени.
Виды электролита
Электролиты бывают двух основных видов:
- Кислотный.
- Щелочной.
Кислотные смеси с дистиллированной водой применяются в основном в аккумуляторах, применяемых для запуска двигателя автомобиля. Такие вещества можно приобрести в специализированных магазинах либо приготовить самостоятельно. На заводе такие смеси делают по ГОСТу, в домашних условиях также можно довольно точно соблюсти необходимые пропорции при смешивании кислоты с водой.
Щелочная смесь может быть приготовлена с использованием различных активных веществ, но наиболее часто применяется кальциево-литиевая основа, которая разводится необходимым количеством дистиллированной воды.
Кислотный электролит
Кислотную токопроводящую жидкость можно готовить самому из концентрированной серной кислоты.
Состав. В состав кислотного электролита входят два вещества:
- Кислота.
- Дистиллированная вода.
В качестве основного вещества чаще используется серная кислота, которая практически не имеет запаха, не испаряется при комнатной температуре. По электропроводимости и другим важнейшим характеристикам этот элемент также наиболее подходит для заливки в свинцовые аккумуляторные батареи.
По электропроводимости и другим важнейшим характеристикам этот элемент также наиболее подходит для заливки в свинцовые аккумуляторные батареи.
Особенности химических свойств. Основной характеристикой кислотного аккумулятора является его плотность. Этот параметр может существенно отличаться в зависимости от степени заряженности батареи, но не должен быть ниже 1,26 и выше 1,30 г/мм3.
Температура замерзания аккумуляторной жидкости напрямую зависит от её плотности, но если этот показатель опустится ниже минус 75 градусов Цельсия, то токопроводящая жидкость даже в полностью заряженном аккумуляторе превратится в лёд.
Серная кислота является едким веществом, поэтому при работе с этим веществом, следует использовать индивидуальные средства защиты. Как минимум, следует применять защитные очки и резиновые перчатки.
Применение. Кислотный электролит применяется, в основном, в свинцовых аккумуляторах. Такие источники тока используются в качестве стартерных батарей в легковом и грузовом транспорте.
Как приготовить. Чтобы приготовить самостоятельно потребуется следующие материалы и инструменты:
- Устойчивую к воздействую кислоты посуду и лопатку для помешивания раствора.
- Дистиллированную воду.
- Аккумуляторную серную кислоту.
Перед выполнением работы следует позаботиться о безопасности. Чтобы защититься от возможного негативного воздействия необходимо подготовить:
- Защитные очки.
- Устойчивый к кислоте фартук.
- Резиновые перчатки.
- Соду для нейтрализации действия кислоты.
Процесс приготовления осуществляется в такой последовательности:
- В ёмкость наливают необходимое количество воды.
- Тонкой струйкой добавляют концентрированную кислоту.
- Перемешать стеклянной или пластиковой лопаткой получившийся раствор.
- Дать отстояться смеси в течение 12 часов.
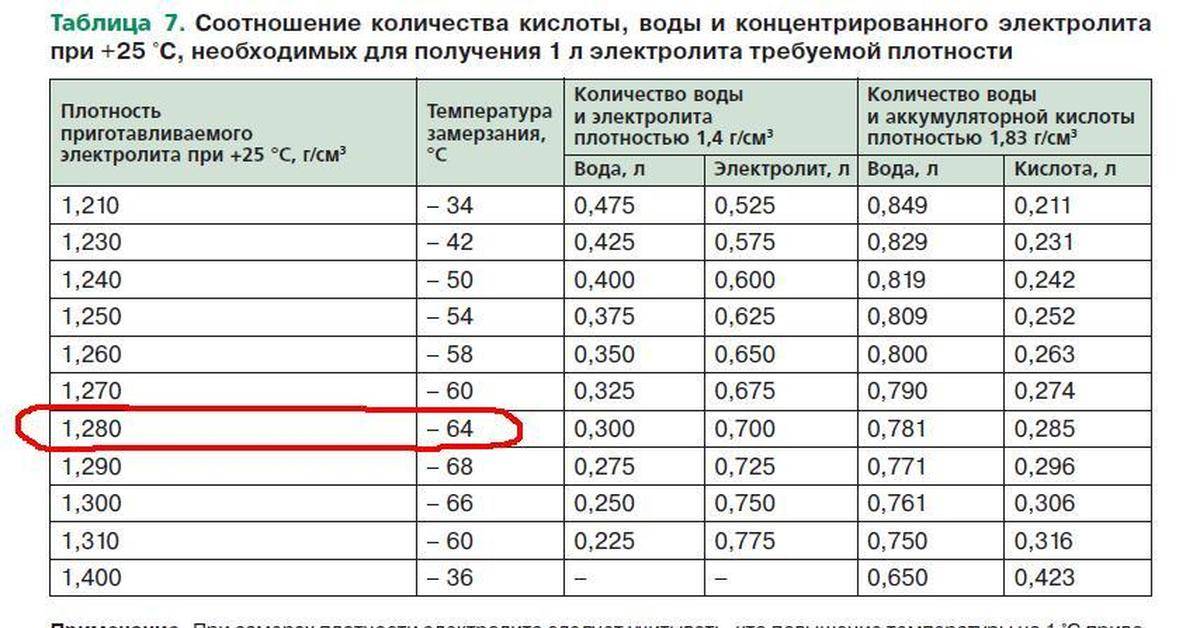
Для приготовления 1 литра смеси необходимой плотности потребуется 0,781 л воды и 0,285 л серной кислоты.
Щелочной электролит
Щелочной электролит имеет свои преимущества и недостатки, но такой состав также широко используется в качестве токопроводящей жидкости в портативных источниках питания.
Состав. В состав аккумуляторного электролита щелочного типа могут использоваться едкий калий или едкий натрий. Для улучшения эксплуатационных характеристик к щелочной основе добавляют также литиевые соединения. Для придания смеси текучести её разбавляют дистиллированной водой.
Особенности химических свойств. Все щелочные аккумуляторные жидкости – это сильные основания, которые активны по отношению к многим металлам и кислотам.
В результате химических реакций с кислотами образуются соль и вода. Растворы щелочей также подвергаются гидролизу. Перечисленные химические свойства позволяют использовать этот тип электропроводящей жидкости для накопления электроэнергии в аккумуляторе.
Применение. Применение щелочных растворов сводится в основном к заправке аккумуляторных батарей. Такие источники электрического тока используются в различных приборах, электропогрузчиках, а также в качестве стартерных батарей для военных машин.
Такие источники электрического тока используются в различных приборах, электропогрузчиках, а также в качестве стартерных батарей для военных машин.
Как приготовить. Чтобы приготовить следует придерживаться определённых правил. Прежде всего, необходима вместительная посуда, изготовленная из устойчивого к щелочи материала. Процесс приготовления следующий:
- В ёмкость заливается необходимое количество дистиллированной воды.
- В жидкость аккуратно всыпается сухая щёлочь. Затем смесь помешивают с помощью пластмассовой лопатки.
- Производится анализ плотности. При необходимости добавить сухую смесь или воду.
- Отстаивается раствор в течение 3 часов.
- Переливается электролит в другую ёмкость, стараясь не допустить поднятия осадка со дна ёмкости.
Если вся работа была произведена по инструкции, то можно получить качественный электролит, который заливают затем в аккумуляторы подходящего типа.
Корректирующий электролит
В процессе эксплуатации обслуживаемых аккумуляторов в банки может быть случайно добавлено слишком большое количество дистиллированной воды, что приведёт к падению плотности токопроводящей жидкости ниже допустимого уровня.
Решается эта проблема приготовлением и заливкой корректирующего электролита повышенной плотности.
Состав. Состав корректирующего раствора не отличается от основного электролита. Например, дли свинцово кислотных АКБ необходимо также развести серную кислоту в дистиллированной воде, но пропорции будет немного отличаться (для получения 1 литра электролита необходимо придерживаться соотношения 0,650 л воды и 0,423 кислоты).
Особенности химических свойств. Химические свойства корректирующего электролита практически не отличаются от основной токопроводящей жидкости. Физические параметры могут незначительно отличаться (более низкая температура замерзания).
Применение. Единственное применение корректирующего электролита – это восстановление оптимальной концентрации кислоты или щёлочи внутри банок аккумулятора.
Как приготовить. Для приготовления корректирующего состава необходимо разбавить чистое основное вещество в дистиллированной воде, но добавлять его необходимо немного больше, чем при производстве обычного электролита.
Последовательность операции также не отличается от стандартной схемы работы с едкими веществами для приготовления токопроводящей жидкости для аккумулятора.
Какой электролит в какой аккумулятор заливается
Если залить в аккумулятор неподходящий электролит, то АКБ будет полностью выведена из строя. Тип аккумулятора, как правило, указан на корпусе изделия, поэтому совершенно несложно установить принадлежность источника питания к определённой категории.
Если этикетка отсутствует, то можно взять небольшое количество электролита и с помощью тестов определить его состав. В свинцово-кислотные аккумуляторы заливаются электролиты на основе серной кислоты. Для щелочных источников питания можно использовать растворы KOH и NaOH.
При добавлении электролита в щелочные устройства следует также точно определить химическую формулу применяемого основания. Отличить одну щёлочь от другой можно по цвету пламени. Если добавить в костёр KOH то цвет огня изменится на красно-фиолетовый, NaOH – горит жёлтым свечением.
Остались вопросы или есть что добавить? Тогда напишите нам об этом в комментариях, это позволит сделает материал более полным и точным.
Литий-ионные аккумуляторы, Часть 5: Электролиты
Электролит часто является недооцененным компонентом литий-ионных (Li-ion) аккумуляторов. Они просто обеспечивают электрический путь между анодом и катодом, который поддерживает ток (на самом деле, ионный) поток. Но электролиты являются ключом к характеристикам аккумуляторов, и ожидается, что достижения в области химии электролитов станут важным событием, ведущим к созданию высокоэффективных, безопасных и недорогих литий-ионных аккумуляторов для будущих поколений электромобилей, хранения энергии в масштабе сети и другие крупные системы. В зависимости от конструкции аккумулятора это может быть жидкий или пастообразный материал. Твердые электролиты могли бы повысить плотность энергии и безопасность ионов лития, но они еще не готовы к коммерциализации. В этом разделе часто задаваемых вопросов рассматриваются электролиты, широко используемые в настоящее время, и рассматриваются усовершенствованные электролиты, находящиеся в стадии разработки, включая твердотельные и гибридные твердотельные электролиты.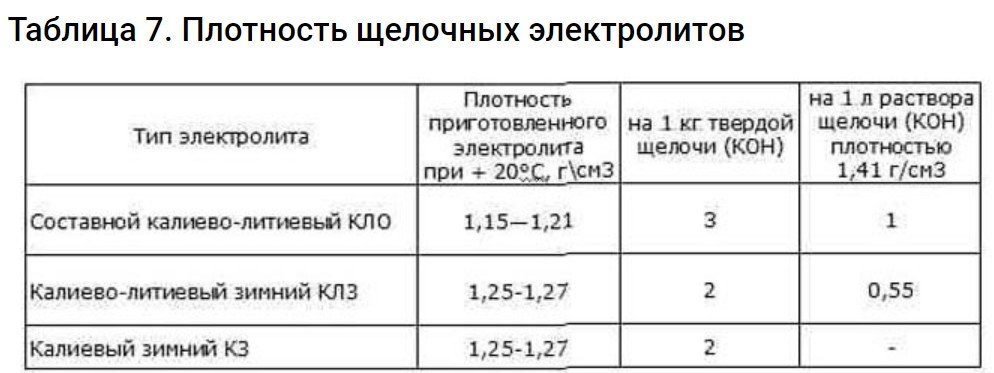
Литий-ионные аккумуляторы состоят из анода и катода на основе различных окислительно-восстановительных химических пар с электролитом и сепаратором между ними. Электролит проводит ионы, а не электроны, через сепаратор и между анодом и катодом (рис. 1) . Электролиты могут принимать различные формы, причем растворенные соли являются наиболее распространенной формой. Растворитель является ключевым компонентом электролита. Водные электролиты имеют высокую проводимость (σ), обычно σ = ~1 Симен/см (См/см), но имеют относительно небольшие окна электрохимической стабильности около 1,25 В. Электролиты на основе неорганических растворителей имеют меньшую электропроводность с σ < 100 мСм/см, но предлагают более широкие окна стабильности 4 В и более. Кроме того, органические растворители более дороги по сравнению с водными растворами. Иногда используют твердый неорганический или полимерный электролит, но с гораздо меньшей электропроводностью; σ <0,1 мСм/см при комнатной температуре.
Рисунок 1: Электролит переносит положительно заряженные ионы через сепаратор между катодом и анодом. (Изображение: Dragonfly Energy)
Различные химические составы первичных (неперезаряжаемых) и вторичных (перезаряжаемых) батарей основаны на разных электролитах. Серная кислота служит электролитом в большинстве свинцово-кислотных аккумуляторов. Обычные щелочные первичные элементы используют гидроксид калия в качестве электролита. Соли, такие как гексафторфосфат лития (LiPF6), обычно используются в качестве электролитов в литий-ионах.
Твердые электролиты для твердых литий-ионных аккумуляторов
Твердые электролиты, изготовленные из керамики, такой как оксиды лития и металла, обещают более высокую плотность энергии и не воспламеняются, что повышает безопасность по сравнению с жидкими электролитами. Помимо риска возгорания, жидкие электролиты могут быть очень реакционноспособными, что приводит к побочным реакциям с электродами, что приводит к снижению емкости батареи с течением времени, что называется снижением емкости. Ожидается, что батареи с твердотельными электролитами не будут испытывать снижения емкости. Также ожидается, что твердотельные электролиты позволят создать литий-металлический анод большой емкости, который значительно повысит удельную энергию и мощность, а также срок службы ионов лития. Разработка твердотельных электролитов сложна и требует материала с рядом эксплуатационных характеристик:
Ожидается, что батареи с твердотельными электролитами не будут испытывать снижения емкости. Также ожидается, что твердотельные электролиты позволят создать литий-металлический анод большой емкости, который значительно повысит удельную энергию и мощность, а также срок службы ионов лития. Разработка твердотельных электролитов сложна и требует материала с рядом эксплуатационных характеристик:
#1 Высокая ионная проводимость в сочетании с высокой устойчивостью к электронам
#2 Высокая способность переноса катионов для поддержки высоких уровней мощности
#3 Широкий диапазон электрохимической стабильности для надежной работы
#4 Высокая термическая стабильность и высокая механическая прочность
#5 Easy и низкая себестоимость производства
Коммерчески жизнеспособный материал еще предстоит разработать: Твердотельные электролиты на основе неорганических материалов обладают высокой ионной проводимостью и хорошей механической прочностью. Полимерные электролиты гибкие, их легче обрабатывать, они сохраняют хороший контакт с электродами, снижая межфазное сопротивление. Но у каждого подхода есть свои проблемы: неорганические твердотельные электролиты могут иметь плохой контакт с электродами (так называемое сопротивление границ зерен), не обладать химической и электрохимической стабильностью, иметь тенденцию быть относительно дорогими и хрупкими. Хрупкость представляет собой серьезную проблему, поскольку неорганические твердотельные электролиты не могут компенсировать изменения объема электродов во время заряда и разряда. Полимерные твердотельные электролиты могут устранить многие ограничения производительности неорганических твердотельных электролитов. Тем не менее, они имеют очень низкую ионную проводимость, что делает их неспособными поддерживать скорости заряда и разряда, необходимые для практических литий-ионных конструкций.
Но у каждого подхода есть свои проблемы: неорганические твердотельные электролиты могут иметь плохой контакт с электродами (так называемое сопротивление границ зерен), не обладать химической и электрохимической стабильностью, иметь тенденцию быть относительно дорогими и хрупкими. Хрупкость представляет собой серьезную проблему, поскольку неорганические твердотельные электролиты не могут компенсировать изменения объема электродов во время заряда и разряда. Полимерные твердотельные электролиты могут устранить многие ограничения производительности неорганических твердотельных электролитов. Тем не менее, они имеют очень низкую ионную проводимость, что делает их неспособными поддерживать скорости заряда и разряда, необходимые для практических литий-ионных конструкций.
Пока выбор лучшего твердотельного электролита не сужен; ведутся исследования десятков вариантов твердотельных электролитов, включая сульфиды, оксиды, фосфаты, полиэфиры, полиэфиры, полиуретаны и многие другие. В настоящее время полимеры легче обрабатывать, чем керамику, и их производство дешевле. Керамика может работать при более высоких температурах и больше подходит для суровых условий окружающей среды.
Керамика может работать при более высоких температурах и больше подходит для суровых условий окружающей среды.
Ожидается, что ионы лития, использующие твердотельные электролиты, будут иметь очень низкую скорость саморазряда, что позволит хранить энергию в течение многих лет с незначительными потерями. Однако срок службы современных материалов составляет всего около трех лет, что делает их непрактичными практически во всех областях применения. Исследования продолжаются из-за большой выгоды, ожидаемой от разработки жизнеспособного твердотельного электролита:
Плотность энергии будет выше, поскольку твердотельные батареи более чем на 80% тоньше и имеют более высокое напряжение разложения, чем современные литий-ионные. Высокая плотность энергии позволит электромобилям (EV) преодолевать большие расстояния и сократит количество зарядных станций, необходимых для обеспечения работы электромобилей.
Так как твердотельные батареи не имеют жидкого электролита, который нагревается во время быстрой зарядки, поэтому возможна более быстрая зарядка. Ожидается, что быстрая зарядка в сочетании с более высокой плотностью энергии повысит конкурентоспособность будущих поколений электромобилей.
Ожидается, что быстрая зарядка в сочетании с более высокой плотностью энергии повысит конкурентоспособность будущих поколений электромобилей.
Твердотельные электролиты обеспечивают безопасную работу . Современные жидкие электролиты легко воспламеняются и требуют многочисленных мер безопасности для обеспечения надежной работы. Твердотельные аккумуляторы по своей природе безопасны с очень низким риском возгорания, и их можно эксплуатировать при более высоких температурах по сравнению с литий-ионными на основе жидких электролитов.
Снижение стоимости возможно при использовании твердотельных батарей. Жидкие литий-ионные аккумуляторы стоят около 220 долларов за кВтч. Хотя ожидается, что она будет продолжать снижаться, темпы снижения затрат ограничены зависимостью от использования дефицитных материалов, таких как кобальт. Ожидается, что в твердотельных батареях не будут использоваться дефицитные или редкие материалы. Использование твердотельного электролита устранит компонент сепаратора, что еще больше упростит конструкцию аккумуляторов, снизит стоимость литий-ионных аккумуляторов и сделает их более привлекательными для использования в электромобилях и крупномасштабных системах хранения энергии.
Твердые варианты
Один многообещающий твердотельный электролит изготовлен из лития, скандия, индия и хлора (рис. 2) . Он имеет высокую ионную проводимость и низкую электронную проводимость. Он имеет окно с высокой электрохимической стабильностью, которое может поддерживать разработку твердотельного литий-иона, который может работать без значительной потери емкости в течение более ста циклов при высоком напряжении (выше 4 В) и тысяч циклов при более низком напряжении. Хлоридные характеристики этого электролита позволяют ему работать при напряжении более 4 В, что делает его пригодным для использования с наиболее распространенными катодными материалами, используемыми в современных литий-ионных конструкциях.
Рис. 2: Электролиты на основе хлора могут улучшить характеристики твердотельных ионов лития. (Изображение: Аргоннская национальная лаборатория)
Большинство предыдущих разработок твердотельных электролитов были сосредоточены на сульфидах, с которыми легче работать, но они имеют более низкий диапазон электрохимической стабильности и разлагаются при напряжении выше 2,5 В. Для работы при более высоких напряжениях сульфиды требуют изолирующего покрытия. на катоде, что снижает проводимость системы. Замена сульфида хлоридом устраняет эту проблему.
Для работы при более высоких напряжениях сульфиды требуют изолирующего покрытия. на катоде, что снижает проводимость системы. Замена сульфида хлоридом устраняет эту проблему.
В дополнение к оптимизации характеристик твердотельного электролита важным фактором является оптимизация интерфейса между электролитом и слоями анода и катода. Один из подходов заключается в использовании специальных покрытий, что увеличивает технологические процессы и стоимость.
Был предложен альтернативный метод, требующий удаления всего углекислого газа (CO2), присутствующего при спекании материалов батареи. Поскольку твердотельный электролит, анод и катод изготовлены из различной керамики, присутствие даже небольшого количества СО2 может значительно снизить производительность интерфейсов между электролитом и анодом и катодом. Работа продолжается в различных аспектах составов и изготовления твердотельных электролитов. Гибридные электролиты могут стать краткосрочной альтернативой.
Гибридные электролиты
Недавно предложенный способ устранения ограничений производительности неорганических и полимерных твердотельных электролитов заключается в гибридизации двух или более элементов. Разработка коммерчески жизнеспособного гибридного твердотельного электролита (HSE) могла бы преодолеть недостатки как неорганических, так и полимерных технологий, сочетая сильные стороны каждой технологии (рис. 3) .
Разработка коммерчески жизнеспособного гибридного твердотельного электролита (HSE) могла бы преодолеть недостатки как неорганических, так и полимерных технологий, сочетая сильные стороны каждой технологии (рис. 3) .
Рисунок 3: Сравнение производительности полимерных, неорганических и гибридных твердых электролитов. (Изображение: Frontiers in Energy Research)
Как и в случае со всеми твердотельными электролитами, разработка HSE является сложной задачей, и коммерческое решение еще впереди. HSE имеют лучшую ионную проводимость, чем большинство полимерных электролитов, но она все же слишком низкая. Кроме того, HSE страдают плохой межфазной стабильностью (снижение надежности) и высоким межфазным сопротивлением (снижение скорости заряда/разряда), что значительно ограничивает производительность литий-ионных аккумуляторов на основе HSE.
Краткое описание
Литий-ионные аккумуляторы с различными жидкими электролитами обеспечивают хорошее сочетание производительности и безопасности. Но стоят они относительно дорого. Новые типы электролитов потребуются для улучшения производительности литий-ионных аккумуляторов, снижения затрат и повышения безопасности. В настоящее время предпринимаются многочисленные усилия по разработке твердотельных электролитов, которые обещают литий-ионы с более высокой плотностью энергии, более быстрой зарядкой, более безопасной работой и более низкой стоимостью. Появление HSE обещает ускорить разработку твердотельных литий-ионных аккумуляторов.
Но стоят они относительно дорого. Новые типы электролитов потребуются для улучшения производительности литий-ионных аккумуляторов, снижения затрат и повышения безопасности. В настоящее время предпринимаются многочисленные усилия по разработке твердотельных электролитов, которые обещают литий-ионы с более высокой плотностью энергии, более быстрой зарядкой, более безопасной работой и более низкой стоимостью. Появление HSE обещает ускорить разработку твердотельных литий-ионных аккумуляторов.
Ссылки
Предотвращение выбросов CO2 повышает термическую стабильность на границе электролита Li7La3Zr2O12 со слоистыми оксидными катодами, передовые энергетические материалы Разработки и вызовы в области гибридных твердых электролитов для литий-ионных аккумуляторов, передовые позиции в исследованиях в области энергетики
Ученые открыли новый электролит для твердотельных литий-ионных аккумуляторов, Аргоннская национальная лаборатория
Что такое аккумуляторный электролит и как он работает?, Dragonfly Energy
Влияние состава электролита на параметры аккумуляторов полиимидно-литиевой системы
Фрибе, К.
 , Лекс-Бальдуччи, А., и Шуберт, США, Устойчивое хранение энергии: последние тенденции и разработки в области полностью органических батарей, Chem. Сус. хим. , 2019, том. 12, с. 4093.
, Лекс-Бальдуччи, А., и Шуберт, США, Устойчивое хранение энергии: последние тенденции и разработки в области полностью органических батарей, Chem. Сус. хим. , 2019, том. 12, с. 4093.Артикул КАС Google Scholar
Оубаха, Х., Гохи, Дж.-Ф., и Мелинте, С., Материалы с π-сопряжением на основе карбонила: от синтеза до применения в литий-ионных батареях,
КАС пабмед Google Scholar
Хауплер, Б., Уайлд, А., и Шуберт, США, Карбонилы: мощные органические материалы для вторичных батарей, Adv. Энергия Матер ., 2015, т. 1, с. 5, с. 1402034.
Артикул Google Scholar
Сонг З., Чжан Х. и Чжоу Ю., Полиимиды: перспективные материалы для хранения энергии, Angew. хим., межд.
 изд., , 2010, т. 1, с. 49, с. 8444.
изд., , 2010, т. 1, с. 49, с. 8444.Артикул КАС Google Scholar
Луо, Дж., Чжу, Ю.Н., Ян, К., Лонг, X.-Y., Лу, С., Лю, С.-П., и Ге, М.-К., Подготовка органополимерные катодные материалы для амидного анода литий-ионного аккумулятора и их электрохимические характеристики, Акта Полим. Грех. , 2017, том. 4, с. 633.
Google Scholar
Райнер, Б.Р., Фоксман, Б.М., и Уэйд, К.Р., Электрохимическое и структурное исследование взаимодействий между диимидами нафталина и катионами металлов, Dalton T. , 2017, vol. 46, вып. 29, с. 9472.
Артикул КАС Google Scholar
Шон, Т.Б., Тилли, А.Дж., Кинастон, Э.Л., и Сеферос, Д.С., Трехмерные каркасы из арилендиимида для высокостабильных литий-ионных аккумуляторов, Приложение ACS Матер.
 Интерфейсы, 2017, вып. 9, № 18, с. 15631.
Интерфейсы, 2017, вып. 9, № 18, с. 15631.Артикул КАС Google Scholar
Sharma, P., Damien, D., Nagarajan, K., Shaijumon, M.M., and Hariharan, M., Органические электродные материалы на основе периленполиимида для перезаряжаемых литиевых батарей, J. Phys. хим. Lett., 2013, vol. 4, с. 3192.
Артикул КАС Google Scholar
Чен, К., Чжао, X., Ли, Х.-Б., Ган, Ф., Чжан, Дж., Донг, Дж., и Чжан, К., Производные полиимида на основе нафталина в качестве органических электродные материалы для литий-ионных аккумуляторов, Электрохим. Acta , 2017, том. 229, с. 387.
Артикул КАС Google Scholar
Chen, L., Li, W., Wang, Y., Wang, C. и Xia, Y., Полиимид в качестве материала анодного электрода для перезаряжаемых натриевых батарей, РСК Адв .
 , 2014, т. 1, с. 4, с. 25369.
, 2014, т. 1, с. 4, с. 25369.Артикул КАС Google Scholar
Донг, X., Ю, Х., Ма, Ю., Бао, Дж., Трухлар, Д.Г., Ван, Ю. и Ся, Ю., Полностью органическая перезаряжаемая батарея с обратимостью, поддерживаемая «водой». электролит «в соли», Хим. Евро. Ж., 2017, том. 23, с. 2560.
Артикул КАС Google Scholar
Сун, З., Сюй, Т., Гордин, М.Л., Цзян, Ю.Б., Бэ, И.Т., Сяо, К., Чжан, Х., Лю, Дж. и Ван, Д., Полимер-графен нанокомпозиты в качестве катодов для сверхбыстрой зарядки и разрядки литиевых аккумуляторов, Нано Летт. , 2012, том. 12, с. 2205.
Артикул КАС Google Scholar
Chen, L., Bao, J.L., Dong, X., Truhlar, D.G., Wang, Y., Wang, C., and Xia, Y., Mg-ионная батарея на водной основе на основе полиимидного анода и берлинской лазури катод, ACS Energy Lett.
 , 2017, vol. 2, с. 1115.
, 2017, vol. 2, с. 1115.Артикул КАС Google Scholar
Гейтани С., Лян Ю., Ву Ф., Цзин Ю., Донг Х., Рао К.К., Чи Х., Фанг Ф. и Яо Ю. Ан водная ионно-кальциевая батарея, Доп. наук, 2017, т. 1, с. 4, с. 1700465.
Артикул Google Scholar
Хуанг, Ю., Ли, К., Лю, Дж., Чжун, X., Дуань, X., Шакир, И., и Сюй, Ю., Трехмерный графен/полиимидный композитный гибкий материал высокопроизводительный органический катод для перезаряжаемых литиевых и натриевых аккумуляторов, J. Mater. хим. А, 2017, том. 5, с. 2710.
Артикул КАС Google Scholar
Шестаков А.Ф., Ярмоленко О.В., Игнатова А.А., Мумятов А.В., Стивенсон К.Дж., Трошин П.А. Структурные причины снижения емкости литий-полимидной батареи. J. Mater. хим. А, 2017, том.
 5, с. 6532.
5, с. 6532.Артикул КАС Google Scholar
Шестаков А.Ф., Романюк О.Е., Мумятов А.В., Лучкин С.Ю., Слесаренко А.А., Ярмоленко О.В., Стивенсон К.Дж., Трошин П.А. Теоретические и экспериментальные доказательства необратимого литирования конформационно гибких полиимид: влияние на производительность батареи, Дж. Электроанал. хим. , 2019, том. 836, с. 143.
Артикул КАС Google Scholar
Ярмоленко О.В., Романюк О.Е., Слесаренко А.А., Баймуратова Г.Р., Шувалова Н.И., Мумятов А.В., Трошин П.А., Шестаков А.Ф. Характеристики литий-полимидного аккумулятора с электролитами различных типов, Рус. Дж. Электрохим. , 2019, том. 55, с. 254.
Артикул Google Scholar
Лян Ю., Чжан П. и Чен Дж., Функционально-ориентированный дизайн электродов на основе сопряженных карбонильных соединений для высокоэнергетических литиевых батарей, Chem.
 наук, 2013, т. 1, с. 4, с. 1330.
наук, 2013, т. 1, с. 4, с. 1330.Артикул КАС Google Scholar
Lv, M., Zhang, F., Wu, Y., Chen, M., Yao, C., Nan, J., Shu, D., Zeng, R., Zeng, H. и Чоу, С.-Л., Гетероароматическое органическое соединение с сопряженным мультикарбонилом в качестве катодного материала для перезаряжаемых литиевых батарей, Науч. Респ., 2016, т. 1, с. 6, с. 23515.
Артикул КАС Google Scholar
Hernández, G., Casado, N., Coste, R., Shanmukaraj, D., Rubatat, L., Armand, M. и Mecerreyes, D., Редокс-активные полиимид-полиэфирные блок-сополимеры в качестве электрода материалы для литиевых аккумуляторов, РСК Прод., 2015, т. 1, с. 5, с. 17096.
Артикул Google Scholar
Xu, Z., Ye, H., Li, H., Xu, Y., Wang, C., Yin, J. и Zhu, H., Улучшенные характеристики хранения ионов лития дубильной кислоты в электролите LiTFSI, САУ Омега, 2017, вып.


 1 Оборудование
1 Оборудование